
����Ŀ�����ӹ�ҵ����30%��FeCl3��Һ��ʴ���ھ�Ե���ϵ�ͭ��������ӡˢ��·�塣
�ٰ�FeO��Fe2O3������������ϡ�����С���ͨ�����������������ȡFeCl3��Һ��FeO��Fe2O3����������ϡ�����У���������Һ��ͨ������������ʱ�����ķ�Ӧ����������ʽΪ ____________________����Ҫ������Һ��Fe3+����Ӧѡ�õ��Լ���_____________________��
��д��FeCl3��Һ�����ͭ������Ӧ�Ļ�ѧ����ʽ___________________________________����ת�Ƶ�����Ϊ6.02��1024ʱ�������������ʵ�����Ϊ_______________
���𰸡� FeO+2HCl=FeCl2+H2O��Fe2O3+6HCl=2FeCl3+3H2O��2Fe2++Cl2=2Fe3++2Cl�� KSCN��Һ Cu+2FeCl3=2FeCl2+CuCl2 320g
�����������������������ᷴӦ�����Ȼ��������Ȼ�������������Ӧ�����Ȼ��������ӷ���ʽ��FeO+2H+=Fe2++H2O��2Fe2++Cl2=2Fe3++2Cl-�������������ᷴӦ�����Ȼ��������ӷ���ʽ��Fe2O3+6H+=2Fe3++3H2O�����������������������������Ѫ��ɫ����������KSCN��Һ�������������ӵĴ��ڣ��ʴ�Ϊ��FeO+2H+=Fe2++H2O��Fe2O3+6H+=2Fe3++3H2O��2Fe2++Cl2=2Fe3++2Cl-�� KSCN��Һ��
���Ȼ�����ͭ��Ӧ�����Ȼ��������Ȼ�ͭ����Ӧ�Ļ�ѧ����ʽΪ��Cu+2FeCl3=2FeCl2+CuCl2�����ݷ���ʽ��Cu+2FeCl3=2FeCl2+CuCl2����֪ת��2mol���ӱ�������ͭ������Ϊ64g����ת�Ƶ�����Ϊ6.02��1024ʱ�������ʵ���Ϊ10molʱ����������ͭ������Ϊ64g/mol��![]() =320g���ʴ�Ϊ��2Fe3++Cu=2Fe2++Cu2+��320g��
=320g���ʴ�Ϊ��2Fe3++Cu=2Fe2++Cu2+��320g��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ� ��
A. 1 mol CO2 ������Ϊ44g/mol
B. CO2��Ħ������Ϊ44g
C. NA��CO2��������CO2����Է�����������ֵ����ͬ
D. CO2��Ħ����������CO2����Է�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��ij��Һ�еμ�Ba(OH)2 ��Һʱ�����������ʵ�����Ba(OH)2 �����ʵ����ı仯��ϵ������Һ�ijɷֿ�����
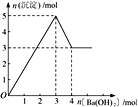
A. MgSO4 B. Al2 (SO4 )3 C. Fe2 (SO4 )3 D. NaAlO2
���𰸡�B
��������A��������þ����������������Һ���������������ټ�����������Һ�����������䣬A����B����ͼ��֪�ܽ�����������Ҫ1mol������������Al(OH)3��OH��===AlO2����2H2O��֪������Al(OH)3Ϊ2mol����Al2(SO4)3Ϊ1mol������3mol���������������������ᱵ3mol��n��Al3+����n��OH-��=2mol��6mol=1��3��������ӦAl3����3OH��===Al(OH)3�������Եõ�2molAl(OH)3������Ϊ3mol+2mol=5mol��B��ȷ��C��������������������Һ��Ӧ����������������������������������������������������ټ�����������Һ�������������䣬��ͼ��һ�£�C����D��ƫ��������������������Ӧ�����ܲ���������D����ѡB��
�㾦��������ͼ��Ϊ���忼��þ������������ʣ���ȷ�����Ļ�ѧ��Ӧ�ǽ��Ĺؼ�����Ӧ�������Ⱥ�˳����ѧ������е��ѵ㣬ע��ͼ�������ϵ��ע���������������ص㡣
�����͡���ѡ��
��������
15
����Ŀ����ͼ��ʾ����MgCl2��AlCl3�Ļ����Һ�м���NaOH��Һ������ʱ���������ʵ���y mol�����NaOH��Һ����������x mL�Ĺ�ϵͼ������ͼʾ�жϣ����н����в���ȷ����
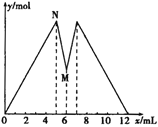
A. N��ʱ��Һ�е�����ֻ��NaCl
B. ԭ�����Һ��c (MgCl2)��c (AlCl3)=1��2
C. c (NaOH)=c (HCl)
D. M��֮ǰ�������NaOH��Һ��M��֮������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�з�Ӧ��Cu2O+2H+=Cu+Cu2++H2O�������������������ԭCuO���õĺ�ɫ�������Ƿ�Cu2O���Լ���(����)
A.ϡ����B.ϡ����C.����D.Ũ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������м������ӷ�Ӧ��
�� Cr2O![]() ��14H����6Cl��===2Cr3����3Cl2����7H2O
��14H����6Cl��===2Cr3����3Cl2����7H2O
�� 2Fe2����Br2===2Fe3����2Br�� �� 2Br����Cl2=== Br2��2Cl��
�� 2Fe3����SO2��2H2O===2Fe2����SO![]() ��4H��
��4H��
�����й����ʵıȽ�����ȷ����(�� ��)��
A. ��������Cr2O![]() >Cl2>Fe3�� B. ��������Cl2>Br2>Cr2O
>Cl2>Fe3�� B. ��������Cl2>Br2>Cr2O![]()
C. ��ԭ����SO2<Fe2��<Br�� D. ��ԭ����Cl��>Cr3��>Fe2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ���ڲ������з��뻹ԭ���ۺ�ʯ���Ļ������Ȳ�ͨ��ˮ���������Թ��ռ������ľ������ˮ�����������������ȼ��
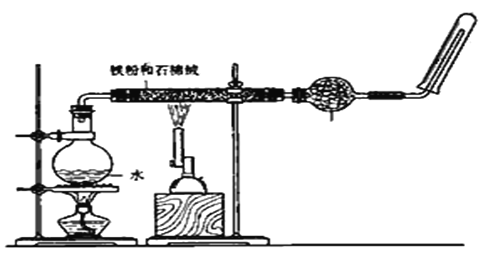
��1��д���÷�Ӧ�Ļ�ѧ����ʽ___________________________________________ ��������������_________________________�������������ǡ���ԭ�������� ��
��2��������ƿ��������__________________________________________________��
��3����ƿ�ײ����˼�Ƭ���Ƭ����������__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Aͼ�ǿα��С����ֻ�����Ӧ������������ԭ��Ӧ�Ĺ�ϵ��ͼ��Aͼ����I��IV��Ӱ���ֱ�ʾ��Ӧ������������ȷ����
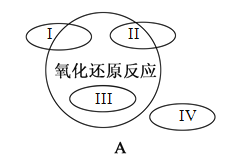
A. �ֹ��ᴿ��Si(��)��3HCl![]() SiHCl3��H2 �������������I��II
SiHCl3��H2 �������������I��II
B. �������ڿ�����ȼ�գ�2 Na �� O2 ![]() Na2O2 ����������һ����III
Na2O2 ����������һ����III
C. ʵ������ȡ������4HCl(Ũ)+MnO2![]() MnCl2+Cl2��+2H2O���������������III
MnCl2+Cl2��+2H2O���������������III
D. �����ƼNa2CO3+Ca(OH)2=2NaOH+CaCO3�� ����������һ����IV
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������͵����������Ǵ�������Ҫ��Ⱦ���ֹ��������Ի�������Ⱦ�ǵ�ǰ������������Ҫ�о�����֮һ��
��1��һ�������£�������Ӧ2SO2��g��+O2��g��2SO3��g������2L�ܱ�������ͨ��2mol SO2��g����1mol O2��g����0.2mol SO3��g����2min��Ӧ�ﵽƽ��ʱ�����SO2�����ʵ���Ϊ1mol����ÿ��淴Ӧ��ƽ�ⳣ��K=�������£������������ټ���2mol SO2��g���������´ﵽƽ��ʱSO2����ת���� 0%�����������������=������
��2����һ�ܱ������з�����Ӧ2NO22NO+O2��H��0����Ӧ������NO2��Ũ����ʱ��仯�������ͼ��ʾ��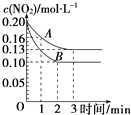
��ش�
��������A����Ӧ��ǰ3min��������ƽ����Ӧ����Ϊ ��
��������A��B�ֱ��ʾ���Ǹ÷�Ӧ��ij��ͬ�����µķ�Ӧ���������������������Ũ�ȡ�����ѹǿ�������¶ȡ�����������
��3��һ���¶��£����ܱ�������N2O5�ɷ������з�Ӧ��
��2N2O5��g��4NO2��g��+O2��g��
��2NO2��g��2NO��g��+O2��g��
����ƽ��ʱ��c��NO2��=0.4molL��1 �� c��O2��=1.3molL��1 �� ��Ӧ����NO2��ת����Ϊ �� N2O5��g������ʼŨ��Ӧ������ molL��1 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ӦNa2CO3+2HCl=2NaCl+H2O + CO2�������ӷ���ʽ��
A. CO32-+2H+ = H2O+CO2��B. CO32-+H+=H2O+CO2��
C. CO32-+2HCl=2Cl-+H2O+CO2��D. Na2CO3+2H+=2Na++H2O+CO2��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com