

| HBr |
| H2O2 |
| 40% |
| 12 |
| 6.7% |
| 1 |
| 53.3% |
| 16 |
| 0.45 |
| 0.005 |
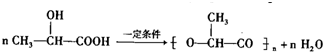
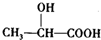 ,B与A反应生成C,C在稀硫酸或稀氢氧化钠溶液中均能反应,则C含有酯基,而B转化生成的D能发生银镜反应,故B中含有-OH,B与A含有相同碳原子数目,且含有一个官能团,故B为CH3CH2CH2OH,C为CH3CH(OH)COOH2CH2CH3,D为CH3CH2CHO,由B→E→F转化,且F为高聚物,则B发生消去反应生成E,E发生加聚反应生成F,故E为CH3CH=CH2,F为
,B与A反应生成C,C在稀硫酸或稀氢氧化钠溶液中均能反应,则C含有酯基,而B转化生成的D能发生银镜反应,故B中含有-OH,B与A含有相同碳原子数目,且含有一个官能团,故B为CH3CH2CH2OH,C为CH3CH(OH)COOH2CH2CH3,D为CH3CH2CHO,由B→E→F转化,且F为高聚物,则B发生消去反应生成E,E发生加聚反应生成F,故E为CH3CH=CH2,F为 ,据此解答.
,据此解答.| 40% |
| 12 |
| 6.7% |
| 1 |
| 53.3% |
| 16 |
| 0.45 |
| 0.005 |
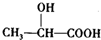 ,B与A反应生成C,C在稀硫酸或稀氢氧化钠溶液中均能反应,则C含有酯基,而B转化生成的D能发生银镜反应,故B中含有-OH,B与A含有相同碳原子数目,且含有一个官能团,故B为CH3CH2CH2OH,C为CH3CH(OH)COOH2CH2CH3,D为CH3CH2CHO,由B→E→F转化,且F为高聚物,则B发生消去反应生成E,E发生加聚反应生成F,故E为CH3CH=CH2,F为
,B与A反应生成C,C在稀硫酸或稀氢氧化钠溶液中均能反应,则C含有酯基,而B转化生成的D能发生银镜反应,故B中含有-OH,B与A含有相同碳原子数目,且含有一个官能团,故B为CH3CH2CH2OH,C为CH3CH(OH)COOH2CH2CH3,D为CH3CH2CHO,由B→E→F转化,且F为高聚物,则B发生消去反应生成E,E发生加聚反应生成F,故E为CH3CH=CH2,F为 ,
,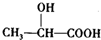 ,故答案为:C3H6O3;
,故答案为:C3H6O3;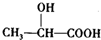 ;
;| Cu |
| △ |
 ,
,| Cu |
| △ |
 ;
;| HBr |
| H2O2 |
| HBr |
| H2O2 |
| 水 |
| △ |
| HBr |
| H2O2 |
| 水 |
| △ |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、X、Y、Z简单离子的半径依次增大 |
| B、将M溶液加热蒸干并灼烧,最后可得Y的氧化物 |
| C、Y的最高价氧化物为碱性氧化物 |
| D、将少量X单质投入到M溶液中,会置换出Y单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mn2O3 |
| B、Mn2+ |
| C、MnO2 |
| D、K2MnO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
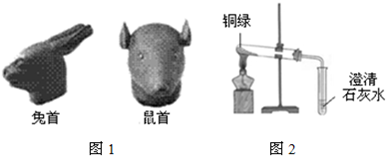
| 操作步骤 | 预期现象及结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:
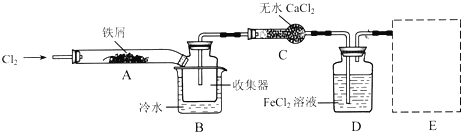
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
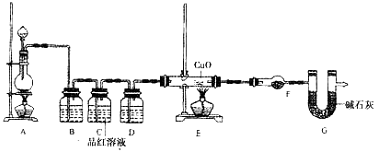
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com