
����Ŀ��![]() ��
��![]() ��
��![]() �ڹ�ҵ����������Ҫ��Ӧ�á�
�ڹ�ҵ����������Ҫ��Ӧ�á�
��1����![]() ���������е�
���������е�![]() ������
������![]() ��
��![]() ���ֵ��ʡ��ڸ÷�Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ_________________________��
���ֵ��ʡ��ڸ÷�Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ_________________________��
��2������![]() ������
������![]() ��Ⱦ���䷴ӦΪ
��Ⱦ���䷴ӦΪ![]() ����ͬ�¶��£���װ������
����ͬ�¶��£���װ������![]() �����
�����![]() �����ܱ�������ͨ��
�����ܱ�������ͨ��![]() �����
�����![]() ������������
������������![]() ��ʱ��
��ʱ��![]() �ı仯������ͼ��ʾ��
�ı仯������ͼ��ʾ��

���¶�ΪT2ʱ��![]() �ڣ�
�ڣ�![]() ��ƽ����Ӧ����
��ƽ����Ӧ����![]() _____________________��
_____________________��
�ڸ÷�Ӧ��![]() ________0������>����<������=�������жϵ�������_________________��
________0������>����<������=�������жϵ�������_________________��
��3�������£���֪![]() �ĵ���ƽ�ⳣ��
�ĵ���ƽ�ⳣ��![]() ��
��![]() ��ͨ������ɵ�
��ͨ������ɵ�![]() ��
��![]() ��Һ
��Һ![]() ___________��
___________��
��4��Ϊ��ȷ��![]() �������ʷ���ʽ
�������ʷ���ʽ![]() ��
��![]() ��ֵ��ȡ����������������Ӧʵ�顣���ܽ�
��ֵ��ȡ����������������Ӧʵ�顣���ܽ�![]() ��Ũ��Ϊ
��Ũ��Ϊ![]() ʱ��
ʱ��![]() �����ʣ�
�����ʣ�![]() ����ֵ�Ĺ�ϵ���±���ʾ����
����ֵ�Ĺ�ϵ���±���ʾ����![]() _______��
_______��
| 3.65 | 7.30 | 10.95 | 14.60 |
| 10.2 | 40.80 | 91.80 | 163.20 |
��5��ij��ҵ��ˮ�к���![]() ��
��![]() �����ӡ�ȡһ�����ĸù�ҵ��ˮ�������еμ�
�����ӡ�ȡһ�����ĸù�ҵ��ˮ�������еμ�![]() ��Һ����
��Һ����![]() ��ʼ����ʱ����Һ��
��ʼ����ʱ����Һ�� _______��������λ��Ч���֣�������֪��25��ʱ��
_______��������λ��Ч���֣�������֪��25��ʱ�� ��
��![]() ��
��
���𰸡�1:5 ![]() < ��ͼ���֪
< ��ͼ���֪![]() �������¶�
�������¶�![]() ��С��ƽ�������ƶ���������ӦΪ���ȷ�Ӧ��
��С��ƽ�������ƶ���������ӦΪ���ȷ�Ӧ��![]() 10 2
10 2 ![]()
��������
��1����Ӧ������������������������![]() �����ӣ���������ԭ����ʧȥ2�����ӣ����������������ˣ�
�����ӣ���������ԭ����ʧȥ2�����ӣ����������������ˣ�
��2�����ݷ���ʽ���Կ�������һ����Ӧǰ�������������ȵķ�Ӧ����˿��Ը���һ����̼��Ũ���������������Ũ�������㣻
��3������![]() �����㣬ע��Ҫ��
�����㣬ע��Ҫ��![]() �����㣻
�����㣻
��4���������ݲ��ѿ�������Ũ������2��ʱ����������4����m����ֵ��ȻΪ2��
��5����Ȼ��ͬһ����Һ�У�![]() ����ͬ�ģ���˴Ӷ��ߵ�
����ͬ�ģ���˴Ӷ��ߵ�![]() ����ʽ�����л��ɣ�
����ʽ�����л��ɣ�
��1����![]() ������ˮ�е�
������ˮ�е�![]() ���������ֵ���
���������ֵ���![]() ��
��![]() ��������Ӧ�Ļ�ѧ����ʽΪ
��������Ӧ�Ļ�ѧ����ʽΪ![]() ��������Ϊ
��������Ϊ![]() ����ԭ��Ϊ
����ԭ��Ϊ![]() ��������������ԭ�������ʵ���֮��Ϊ1:5��
��������������ԭ�������ʵ���֮��Ϊ1:5��
��2���ٸ÷�Ӧ���������������ķ�Ӧ����ʼʱ![]() ��Ũ��Ϊ
��Ũ��Ϊ![]() ���������Ũ��ʼ�ղ��䡣
���������Ũ��ʼ�ղ��䡣![]() ʱ��
ʱ��![]() ��Ũ��Ϊ
��Ũ��Ϊ![]() �����
�����![]() ������������
������������![]() =30%�����
=30%�����![]() ��
��
����ͼ�������![]() ����
����![]() ����
����![]() ��
��![]() ���������¶ȣ�
���������¶ȣ�![]() ��С���������¶�ƽ�������ƶ���������ӦΪ���ȷ�Ӧ��
��С���������¶�ƽ�������ƶ���������ӦΪ���ȷ�Ӧ��
��3��������֪������![]() ��
��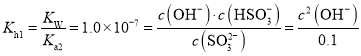 ������ɵ�
������ɵ�![]() ��
��![]() ��
��
��4���۲�����е����ݣ�ÿ��![]() ��Ϊ2������Ӧ������
��Ϊ2������Ӧ������![]() ���DZ�Ϊ4������˸÷�Ӧ������
���DZ�Ϊ4������˸÷�Ӧ������![]() ��ƽ�������ȣ���mΪ2��
��ƽ�������ȣ���mΪ2��
��5����Һ��![]() ��ͬ����˸���
��ͬ����˸���![]() �ı���ʽ��
�ı���ʽ��![]() =
=![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������������һ�����õĴ˾����ݲݸ˾���ɱ�������ϳ�һ�ֶ����������������ķ�����ͼ1��

��0.45g��2-���������������0.500g�Ķ����������������뵽50mL���У����������ˮ6Сʱ��ˮԡ�����ܼ��������ᆳ�ؽᾧ�õ���ɫ��״���塣
�����ʵ��ܽ��Ա�
���� | ˮ | �� | �Ҵ� |
2-�������������� | ���� | ���� | ���� |
�������������� | ���� | ���� | ���� |
�������������� | ���� | ���� | ���� |
�ش��������⣺
��1��������������___�����ˮ��Ϊ___��
��2��ʵ�鲻ʹ��������ʹ��ĥ�ڲ�����ӵ�ԭ����___��
��3����ˮ�����ң��м�����ˮ���ӽ�֧�ܴ���ʹ�����ܻ�����Һ���е�ˮ���������ˮ����ˮ������ʱ�ɴ�ˮ�������ų����л������ܶ�С��λ��ˮ���Ϸ����ӷ�ˮ��֧�ܻ�������ƿ����ʵ��ѡ�õķ�ˮ����������__�����ţ�
A������Ч�ذ�ˮ���뷴Ӧ��ϵ���ٽ�ƽ��������Ӧ�����ƶ�
B����ͨ���۲�ˮ��߶Ȳ��ٱ仯�������жϷ�Ӧ������ʱ��
C�������л��ܼ���ˮ
D����Ҫ�������ܼ�������
��4���������������ķ�����__��
��5�����������IJ����Ҫ���ؽᾧ�ᴿ��ѡ�õ��ᴿ�Լ���__�����ţ�
A��ˮ B���Ҵ� C����
��6���ؽᾧ�ᴿ�������Ϊ0.670g����������������������IJ���ԼΪ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ߴ���������Ϊ�ϳ���������Ԫ�������ϵ�ԭ�ϣ���ҵ�Ͽ�����Ȼ�������̷������̿���Fe��Al��Mg��Zn��Ni��Si��Ԫ�أ��Ʊ�����������ͼ��ʾ���ش��������⣺
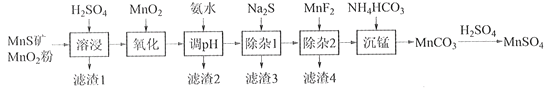
��ؽ�������[c0(Mn+)=0.1 mol��L1]�γ��������������pH��Χ���£�
�������� | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
��ʼ������pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
������ȫ��pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
��1��������1������S��__________________________��д�����ܽ����ж������������̷�Ӧ�Ļ�ѧ����ʽ____________________________________________________��
��2����������������������MnO2�������ǽ�________________________��
��3������pH��������������Һ��pH��ΧӦ����Ϊ_______~6֮�䡣
��4��������1����Ŀ���dz�ȥZn2+��Ni2+��������3������Ҫ�ɷ���______________��
��5��������2����Ŀ��������MgF2������ȥMg2+������Һ��ȹ��ߣ�Mg2+��������ȫ��ԭ����_____________________________________________________________________��
��6��д���������������ӷ���ʽ___________________________________________________��
��7����״��������Ԫ���Ͽ���Ϊ����ӵ���������ϣ��仯ѧʽΪLiNixCoyMnz2������Ni��Co��Mn�Ļ��ϼ۷ֱ�Ϊ+2��+3��+4����x=y=![]() ʱ��z=___________��
ʱ��z=___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ��ش��������⣺
��1�������£�����Ũ�ȵ�Na2S2O3��Һ��������Һ��ϣ�2 min����Һ�����Գ��ֻ��ǣ���д����ط�Ӧ�����ӷ���ʽ��__________________________________________�������˻����Һ����50���ˮԡ�У�����ֻ��ǵ�ʱ�佫__________ (������������������������������)��
��2����֪![]() �ĵ���ƽ�ⳣ��
�ĵ���ƽ�ⳣ��![]() ����0.1mol/L
����0.1mol/L![]() ��Һ�еμ�NaOH��Һ��
��Һ�еμ�NaOH��Һ��![]() 1:18����ʱ��ҺPH=________��
1:18����ʱ��ҺPH=________��
��3��CO2��CH4�����������Ƶúϳ���CO��H2��
����֪������Ӧ����صĻ�ѧ�������������£�
��ѧ�� | C��H | C=O | H��H | C |
����/kJ��mol1 | 413 | 745 | 436 | 1075 |
��÷�Ӧ���Ȼ�ѧ��Ӧ����ʽΪ��___________________________���ֱ���v L�����ܱ�����A�����ݣ���B����ѹ���ݻ��ɱ䣩�У�����CH4��CO2��1 mol�Ļ�����塣�������з�Ӧ��ƽ���ų������յ������϶����_______������A�� ����B ������
�ڰ�һ������ȼ���CH4��CO2���ں�ѹ�·�����Ӧ���¶ȶ�CO��H2���ʵ�Ӱ������ͼ��ʾ���˷�Ӧ��ѡ�¶�Ϊ900���ԭ����_________________________________��
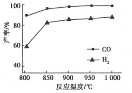
��4����֪2CH3OH(g) ![]() CH3OCH3(g)��H2O(g)��ij�¶��µ�ƽ�ⳣ��K = 4�����¶��£����ܱ������м���CH3OH����Ӧ��20minʱ��ø���ֵ�Ũ�����£�
CH3OCH3(g)��H2O(g)��ij�¶��µ�ƽ�ⳣ��K = 4�����¶��£����ܱ������м���CH3OH����Ӧ��20minʱ��ø���ֵ�Ũ�����£�
���� | CH3OH | CH3OCH3 | H2O |
c / mol��L-1 | 0��4 | 0��1 | 0��1 |
�ٴ�ʱ����Ӧ��___________ (����������������)�ƶ������ܴﵽƽ�⡣
�ڴӼ���CH3OH��ʼ��Ӧ��20minʱ��CH3OCH3����������Ϊ_____________��
�۴ﵽƽ���CH3OH��Ũ��Ϊ_____________��
��5����ȡ���Ҷ����Ҷ����ķ�Ӧ����ʽ_______________________________
��6����һ����������֬����![]() �ṹ��ʽΪ
�ṹ��ʽΪ![]() ,д����ϳɵ������ϩ�裨CH2=CHCN��,2-������ϩ�⣬����Ҫ�ĵ��������ǣ�__________��
,д����ϳɵ������ϩ�裨CH2=CHCN��,2-������ϩ�⣬����Ҫ�ĵ��������ǣ�__________��
��7���л���R��C6H12O2����ϡ���Ṳ������A��B��A�ܹ�����������Ӧ��B���ܷ�����������Ӧ����ôR�Ľṹ��ʽΪ_________��
��8���ҹ�ѧ�߽��ʵ��������ģ�������о����ڽ����������ˮú���任[CO(g)+H2O(g)=CO2(g)+H2(g)]�ķ�Ӧ���̣���ͼ��ʾ�����������ڽ���������ϵ���������ע��
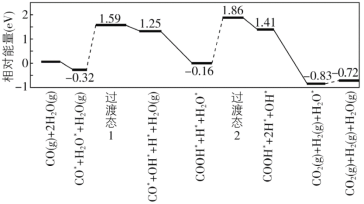
��֪ˮú���任����H________0������������������������С����������������������ݣ���ܣ�E��=_________eV��д���ò���Ļ�ѧ����ʽ_______________________��
��9��ij�л���A��C��H��O����Ԫ�����,��Է�������Ϊ90 .��9.0gA��ȫȼ�յIJ�������ͨ��������Ũ����ͼ�ʯ��,�ֱ�����5.4g��13.2g��A����NaHCO3��Һ��Ӧ,��2����A֮����ˮ�����ɰ�Ԫ��������.��A��һ�������·������۷�Ӧ�IJ���Ľṹ��ʽ��:_________________________
��10����֪��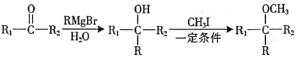 (R��ʾ������R1��R2��ʾ��������ԭ��)�������
(R��ʾ������R1��R2��ʾ��������ԭ��)�������![]() Ϊԭ���Ʊ�
Ϊԭ���Ʊ�![]() �ĺϳ�·��(�ṩCH3MgBr����Ҫ�����Լ�)_______________________________________________________________��
�ĺϳ�·��(�ṩCH3MgBr����Ҫ�����Լ�)_______________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���õ�ⷨ�����������Է�ˮ���õ�����![]() ��ԭ����ͼ��ʾ������˵������ȷ���ǣ� ��
��ԭ����ͼ��ʾ������˵������ȷ���ǣ� ��
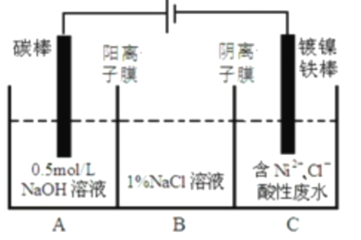
��֪����![]() ����������Һ�з���ˮ�⣻�������ԣ�
����������Һ�з���ˮ�⣻�������ԣ�![]() ����Ũ�ȣ�
����Ũ�ȣ�![]() ����Ũ�ȣ���
����Ũ�ȣ���
A.�������У�B��![]() ��Һ�����ʵ���Ũ�Ƚ���������
��Һ�����ʵ���Ũ�Ƚ���������
B.̼���Ϸ����ĵ缫��Ӧ��![]()
C.Ϊ�����![]() �IJ��ʣ�����������Ҫ���Ʒ�ˮ��
�IJ��ʣ�����������Ҫ���Ʒ�ˮ��![]()
D.��װ���е��ӵ�����Դ��������������������Դ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��T��һ���л�ҩ���ϳ�·����ͼ��

��֪���� ��
��
��
��1��Z�к��������ŵ�����Ϊ_______________��
��2��R�ķ���ʽΪ_________��R������Ӧ������S��д��S�Ľṹ��ʽ��__________________��
��3��![]() �ķ�Ӧ����ʽΪ________________��
�ķ�Ӧ����ʽΪ________________��![]() �ķ�Ӧ����Ϊ________________��
�ķ�Ӧ����Ϊ________________��
��4��W��T��һ��ͬ���칹�壬��������������W�Ľṹ��______________�֣�д������һ�ֵĽṹ��ʽ��___________________________��
���ܷ���������Ӧ��
���ܷ���ˮ�ⷴӦ����ˮ�����֮һ����![]() ��Һ������ɫ��Ӧ��
��Һ������ɫ��Ӧ��
�۷�����ֻ��4�ֲ�ͬ��ѧ�������⡣
��5����ϱ�����Ϣ������2-��-1-������ ������Ϊԭ�����ϳ�X��д���йصĺϳ�·������ͼ�����Լ���ѡ��____________���ϳ�·������ͼʾ�����£�
������Ϊԭ�����ϳ�X��д���йصĺϳ�·������ͼ�����Լ���ѡ��____________���ϳ�·������ͼʾ�����£�![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(H3BO3)Ϊ���ᣬ��֪H3BO3������NaOH��Һ��Ӧ�����ӷ���ʽΪH3BO3+OH-=B(OH)4-��H3BO3����ͨ�����ķ����Ʊ����乤��ԭ����ͼ��ʾ(��Ĥ����Ĥ�ֱ�ֻ���������ӡ�������ͨ��)������˵��������ǣ� ��
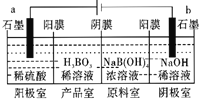
A.�����ĵ缫��ӦʽΪ��2H2O-4e-=O2��+4H+
B.��Ӧһ��ʱ���Ժ�������NaOH��ҺŨ������������H2SO4Ũ������
C.����·��ͨ��3mol����ʱ���ɵõ�1molH3BO3
D.�������У�B(OH)4-������Ĥ�����Ʒ�ϣ�Na+������Ĥ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������NO2��SO2��CO���к�����Դ���������Σ����������Ĺ�ͬ��
��1����ԭ�Ӿ���ѧԭ�������£���ѧ����CO��H2�ڼ��ȼ�ѹ�����ϳ���Һ��ȼ�ϼ״����仯ѧ��Ӧ����ʽΪ__��
��2���Լ״���ȼ�ϵĵ�أ���ͼ��ʾ���为����__����a��b���������ķ�ӦʽΪ___�������ķ�ӦʽΪ___����ȼ�ϵ��������״̬�£�����96.5%�Ļ�ѧ��ת���ɵ��ܣ�������1molҺ��״����ܲ����������ܴ�702.1kJ����ͨ���״�ȼ�յ��Ȼ�ѧ��Ӧ����ʽΪ__��
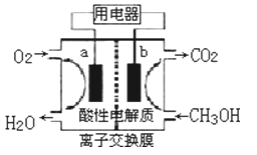
��3����֪��NO2��g��+SO2��g��SO3��g��+NO��g�� ��H=+41.8kJmol��1��һ�������£���NO2��SO2�������1��2�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬����___��
a����ϵѹǿ���ֲ���
b�����������ɫ���ֲ���
c��SO3��NO������ȱ��ֲ���
d��ÿ����1molSO3��ͬʱ����1molNO2
��������Ӧƽ��ʱ�����NO2��SO2�����Ϊ1��6����ƽ�ⳣ��K=__�������Ѵ�ƽ��״̬��������Ӧ����ʱ��ƽ�ⳣ��K��__�������С�䣩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������5���л������Ȳ ��![]() ��
��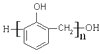 ����֬ �������ǣ��뽫��Ӧ���������ո��ڡ�
����֬ �������ǣ��뽫��Ӧ���������ո��ڡ�
��1�����������������__��
��2�����ڹ�ҵ�ƾ�����__��
��3���������ӻ��и��������__��
��4���ڵĵ�����__����ṹ��ʽ����
��5���۵ĵ�����__����ṹ��ʽ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com