
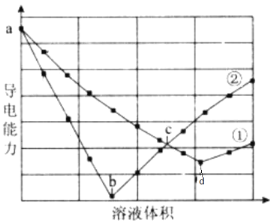
【题目】在两份相同的H2SO4溶液中,分别滴人物质的量浓度相等的Ba(OH)2、NaOH溶液,其导电能力随滴入溶液体积变化的曲线如下图所示。下列分析正确的是( )
A.①代表滴加Ba(OH)2溶液的变化曲线B.ab段发生反应的离子方程式为:OH-+H+=H2O
C.b、d两点对应的溶液均显中性D.c点对应的两溶液中含有相等量的OH-
【答案】C
【解析】
向H2SO4溶液中滴入Ba(OH)2溶液时,发生反应H2SO4+Ba(OH)2=BaSO4↓+2H2O,随着Ba(OH)2溶液的滴入,溶液中H+、SO42-浓度减小,导电能力逐渐减弱,b点恰好反应时几乎不导电,之后过量的Ba(OH)2使溶液中Ba2+、OH-浓度增大,导电能力增强,故图中曲线②表示向H2SO4溶液中滴入Ba(OH)2溶液;向H2SO4溶液中滴入NaOH溶液时,发生反应H2SO4+2NaOH=Na2SO4+2H2O,随着NaOH溶液的滴入,溶液总体积变大,溶液中离子浓度减小,导电能力逐渐减弱,d点恰好反应时导电能力最弱,之后过量的NaOH使溶液导电能力增强,曲线①表示向H2SO4溶液中滴入NaOH溶液。
A. 根据分析,曲线②在b点溶液导电能力接近0,说明该点溶液离子浓度最小,曲线②表示向H2SO4溶液中滴入Ba(OH)2溶液,A错误;
B. ab 段发生反应的离子方程式为:Ba2++SO42-+2OH-+2H+=2H2O+BaSO4↓,B错误;
C. b、d两点,酸碱恰好中和,对应的溶液均显中性,C正确;
D. 曲线②上的c点,Ba(OH)2溶液已经过量,溶液中有OH-,曲线①上的c点,NaOH溶液不足,剩余H2SO4,溶液呈酸性,D错误;
故答案为:C。


科目:高中化学 来源: 题型:
【题目】室温下向10mLpH=3的醋酸溶液中加入水稀释后,下列说法正确的是
A.溶液中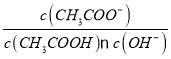 不变
不变
B.溶液中导电粒子的数目减少
C.醋酸的电离程度增大,c(H+)亦增大
D.完全致中和醋酸需加入10mLpH=11的NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 乙酸与碳酸钠溶液反应:2H++CO32—== CO2↑+H2O
B. 醋酸溶液与新制氢氧化铜反应:CH3COOH+OH-→CH3COO-+H2O
C. 苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O →2C6H5OH+CO32—
D. 甲醛溶液与足量的银氨溶液共热:HCHO+4[Ag(NH3)2]++4OH-![]() CO32—+2NH4++4Ag↓+6NH3+2H2O
CO32—+2NH4++4Ag↓+6NH3+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X的基态原子中的电子共有7个能级,且最外层电子数为1,X原子的内层轨道全部排满电子.在气体分析中,常用XCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:2XCl+2CO+2H2O═X2Cl2·2CO·2H2O
(1)X基态原子的电子排布式为__________________.
(2)C、H、O三种原子的电负性由大到小的顺序为__________.
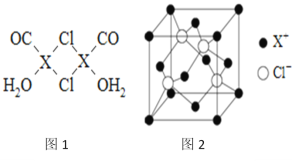
(3)X2Cl2·2CO·2H2O是一种配合物,其结构如图1所示:
①与CO为互为等电子体的分子是_________.
②该配合物中氯原子的杂化方式为__________.
③在X2Cl22CO2H2O中,每个X原子能与其他原子形成3个配位键,在图中用“→”标出相应的配位键_____________.
(4)阿伏加德罗常数的测定有多种方法,X射线衍射法就是其中的一种。通过对XCl晶体的X射线衍射图象的分析,可以得出XCl的晶胞如图2所示,则距离每个X+最近的Cl﹣的个数为____________,若X原子的半径为a pm,晶体的密度为ρg/cm3,试通过计算阿伏加德罗常数NA=___________________(列计算式表达)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在恒容容器中投入一定量纯净的氨基甲酸铵,发生下列反应NH2COONH4(s) ![]() 2NH3(g)+CO2(g)。能判断该分解反应已经达到化学平衡的是
2NH3(g)+CO2(g)。能判断该分解反应已经达到化学平衡的是
A.2v(NH3)=v(CO2)
B.密闭容器中混合气体的密度不变
C.密闭容器中混合气体的平均摩尔质量不变
D.密闭容器中氨气的体积分数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组进行Cu和Fe2(SO4)3溶液的实验。实验探究过程如下:
实验装置:
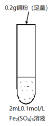
实验操作与现象: ⅰ.加入Cu粉后充分振荡,静置,溶液变成浅蓝绿色;
ⅱ.取少量ⅰ中清液于试管中,滴加3滴0.1mol/L KSCN溶液,立即出现白色沉淀,溶液局部变为红色,振荡后红色迅速褪去。
查阅资料:
Ⅰ.Cu2+可与SCN-反应生成CuSCN(白色沉淀)和(SCN)2: (SCN)2的性质与Cl2相似。
Ⅱ.CuSCN能与稀硝酸反应:CuSCN+HNO3→CuSO4+N2↑+CO2+H2O(未配平)。
回答下列问题:
(1)Cu和Fe2(SO4)3溶液反应的离子方程式为________。
(2)根据表中实验现象推断白色沉淀为___________。为验证该白色沉淀,取少量白色沉淀于试管中,加入___,若____即可证明(补充所加试剂及实验现象)。
(3)试解释ⅱ中溶液局部变为红色的原因是______。
(4)根据ⅱ中实验现象可推知SCN-更易与_______结合(填“Fe3+”或“Cu+”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,固定容积的密闭容器中发生下列反应:![]() 反应过程中,各物质浓度与时间的关系如图:
反应过程中,各物质浓度与时间的关系如图:
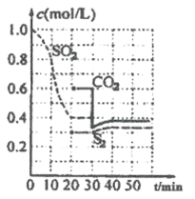
(1)该反应平衡常数表达式为![]() ____________。
____________。
(2)![]() 化学反应速率表示
化学反应速率表示![]() ______;建立平衡过程中,混合气体的密度______(选填“增大”、“减小”或“不变”)。
______;建立平衡过程中,混合气体的密度______(选填“增大”、“减小”或“不变”)。
(3)![]() 时改变外界条件,使
时改变外界条件,使![]() ______
______![]() (选填“大于”、“小于”或“等于”)。
(选填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一个容积为2L的密闭容器中充入2mol NH3和3 mol O2,在恒温和催化剂作用下发生反应:4NH3(g)+5O2(g)4NO(g) + 6H2O(l) ,经过5min后达到平衡状态。此时,c(NH3):c(O2)=4:7。则:
(1)反应开始至平衡时,以NO的浓度变化表示该反应的平均速率v(NO)=__________。
(2)起始状态与平衡状态容器内的压强之比为______。
(3)该条件下反应一段时间,下列能说明反应达到平衡状态的是___________ 。
A.c(H2O)保持不变的状态 B.气体的压强保持不变的状态
C.4v正(NH3)=5v逆(O2) D.NH3与O2浓度之比保持不变的状态
(4)为了研究硫酸铜的量对氢气生成速率的影响,某同学设计了如下一系列的实验:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积的气体所需时间。
A | B | C | D | E | F | |
4mol/L H2SO4(mL) | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液(mL) | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O(mL) | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1 = _________ ,V6 = _________ 。
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因______________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的Mg和Al混合物投入到200mL稀硫酸中,固体全部溶解后,向所得溶液中滴加NaOH溶液至过量,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法不正确的是( )
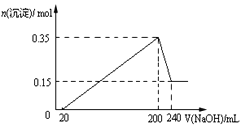
A. 生成的氢气在标准状况下的体积为11.2L
B. 最初20mLNaOH溶液用于中和过量的稀硫酸
C. NaOH溶液物质的量浓度为5mol·L-1
D. Mg和Al的总质量为9g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com