
【题目】有A、B、C、D、E五种元素,它们原子的核电荷数依次递增且均小于18;A原子核内仅有1个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等;D原子有两个电子层,最外层电子数是次外层电子数的3倍;E元素的最外层电子数是其电子层数的三分之一。
(1)试推断它们各是什么元素,写出它们的元素符号:
A______、B______、C.______、D______、E______。
(2)写出A分别与B、C、D所形成化合物的化学式:_________、_________、_________。
(3)A、C、D形成的化合物与A、D、E形成的化合物各属于那类物质?__________写出它们相互反应的化学方程式。___________
【答案】H C N O Na CH4(其它合理答案也可) NH3(其它合理答案也可) H2O(其它合理答案也可) 酸或盐、碱 HNO3+NaOH=NaNO3+H2O(或NH4NO3+NaOH![]() NaNO3+NH3↑+H2O)
NaNO3+NH3↑+H2O)
【解析】
A原子核内仅有1个质子,则A为H;D原子有两个电子层,最外层电子数是次外层电子数的3倍,最外层电子数为6,则D为O;B原子的电子总数与D原子的最外层电子数相等,B有6个电子,则B为C;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等,则C为N;E元素序数小于18,其最外层电子数是其电子层数的三分之一,则电子层数为3,最外层为1,E为Na。
(1)根据分析可知,A为H;B为C;C为N;D为O;E为Na;
(2)H与C、N、O形成的简单化合物的化学式分别为CH4、NH3、H2O;
(3)A、C、D形成的化合物为HNO3或NH4NO3,属于酸或盐;A、D、E形成的化合物为NaOH,属于碱;硝酸(或NH4NO3)与NaOH反应的化学方程式为HNO3+NaOH=NaNO3+H2O(或NH4NO3+NaOH![]() NaNO3+NH3↑+H2O)。
NaNO3+NH3↑+H2O)。


科目:高中化学 来源: 题型:
【题目】将二氧化锰和生物质置于一个由滤纸制成的折纸通道内形成电池(如图所示),该电池可将可乐(pH=2.5)中的葡萄糖转化成葡萄糖内酯并获得能量。下列说法正确的是
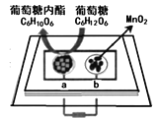
A.a极为正极
B.外电路电子移动方向为b到a
C.b极的电极反应式为:MnO2+2H2O+2e-=Mn2++4OH-
D.当消耗0.01mol葡萄糖时,电路中转移0.02mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的组成、结构或性质的叙述中,正确的是
①HF的稳定性很强,是因为其分子间能形成氢键
②基态原子价电子排布式为(n-1)d6~8ns2的元素属于第ⅧB族
③能层为1时,有自旋方向相反的两个轨道
④“量子化”就是连续的意思,微观粒子运动均有此特点
⑤前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有5种
⑥次氯酸分子的电子式:![]()
⑦氯离子与硫离子的核外电子排布相同,都是1s22s22p63s23p6,两粒子的3p能级上的电子离核的距离相同
⑧S2-、Cl-、K+、Na+半径逐渐减小
⑨最外层有3个未成对电子的原子一定属于主族元素
A.①③④⑦⑧B.⑤⑧⑨C.②③⑤⑥⑦⑨D.②⑦⑧⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有1个未成对电子,次外层有2个电子,其元素符号为____。
(2)B元素是前四周期基态原子中的未成对电子数最多的,其基态原子的价电子排布图为_____。
(3)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,该电子的轨道形状为_____,C的基态原子核外电子占用了_____个原子轨道,被其占用的最外电子层本身有_____个能级。
(4)D元素是自然界中含量居第二位的金属元素,其+3价离子简化的核外电子排布式为______,该离子比同元素的其它离子更稳定的原因是_____。
(5)E元素原子最外层电子数是电子层数的3倍,其核外共有_____种能量不同的电子,写出E的具有18个电子的氢化物的电子式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己二酸是合成尼龙-66的主要原料之一。实验室合成己二酸的原理、有关数据如下:
3![]() +8HNO3→3
+8HNO3→3![]() +8NO↑+7H2O
+8NO↑+7H2O
物质 | 相对分子质量 | 密度(20℃) | 熔点 | 沸点 | 溶解性 |
环己醇 | 100 | 0.962 g/cm3 | 25.9℃ | 160.8℃ | 20℃时,在水中溶解度为3.6g,可混溶于乙醇、苯 |
己二酸 | 146 | 1.360 g/cm3 | 152℃ | 337.5℃ | 在水中的溶解度:15℃时1.44g,25℃时2.3g。易溶于乙醇,不溶于苯 |
步骤Ⅰ:在如图装置的三颈烧瓶中加入16 mL 50%的硝酸(过量,密度为1.310 g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4 mL环己醇。

步骤Ⅱ:水浴加热三颈烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间。
步骤Ⅲ:当环己醇全部加入后,将混合物用80℃~90℃水浴加热约10 min(注意控制温度),直至无红棕色气体生成为止。
步骤Ⅳ:趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后抽滤、洗涤、干燥、称重。请回答下列问题:
(1)装置b的名称为__________,使用时要从_________(填“上口”或“下口”)通入冷水;滴液漏斗的细支管a的作用是________________。
(2)实验中,先将温度由室温升至50℃左右,再慢慢控制在60℃~65℃之间,最后控制在80℃~90℃,目的是____________________。
(3)本实验所用的50%的硝酸物质的量浓度为____________;实验中,氮氧化物废气(主要成分为NO和NO2)可以用NaOH溶液来吸收,其主要反应为NO+NO2+2NaOH == 2NaNO2+H2O。其中NaOH溶液可以用Na2CO3溶液来替代,请模仿上述反应,写出Na2CO3溶液吸收的方程式:______________________________________。
(4)为了除去可能的杂质和减少产品损失,可分别用冰水或______洗涤晶体。
(5)通过称量得到产物7.00 g,则本实验产率为__________(精确到0.1%)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将过量的二氧化碳分别通入:①氯化钙溶液 ②硅酸钠溶液 ③氢氧化钙溶液 ④饱和碳酸钠溶液。最终溶液中有白色沉淀析出的是( )
A.①②③④
B.②④
C.①②③
D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T ℃时在2 L的密闭容器中X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图甲所示;若保持其他条件不变,反应温度分别为T1和T2时,Y的体积分数与时间的关系如图乙所示。

则下列结论正确的是(双选) ( )。
A.该反应可表示为3X(g)+Y(g)![]() 2Z(g)
2Z(g)
B.若其他条件不变,升高温度,平衡将向逆反应方向移动
C.若其他条件不变,开始时将该容器压缩为1 L,则反应将按图丙进行
D.若其他条件不变,使用适当的催化剂,则反应可以按图丙进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯雌酚是人工合成的激素药物,能改善体内激素的平衡状态,其结构如图。下列有关叙述错误的是( )
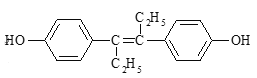
A.乙烯雌酚能发生取代、加成、氧化反应
B.乙烯雌酚可分别与NaOH、NaHCO3溶液反应
C.每1mol该有机物最多可以与含5molBr2的溴水反应
D.该有机物分子中最多有18个碳原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用。
(1)基态Fe2+的电子排布式为______。
(2)FeSO4常作净水剂和补铁剂,SO42-的立体构型是______。
(3)羰基铁[Fe(CO)5]可作催化剂、汽油抗爆剂等。1molFe(CO)5分子中含______molσ键。
(4)氮化铁晶体的晶胞结构如图1所示(Fe3+离子为六方最密堆积)。该晶体中铁、氮的微粒个数之比为______。在该晶胞中,与Fe3+紧邻且等距离的Fe3+数目为______。
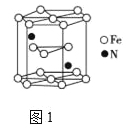
(5)某铁氮化合物(FexNy)的晶胞如图2所示,N原子位于b位置Fe形成的空隙,Cu可以完全替代该晶体中a位置Fe或b位置Fe,形成Cu替代型产物Fe(x-n)CunNy。FexNy转化为两种Cu替代型产物的能量变化如图3所示,其中更稳定的Cu替代型产物的化学式为______。
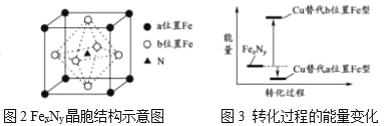
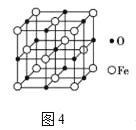
(6)氧化亚铁晶体的晶胞如图4所示。已知:氧化亚铁晶体的密度为ρg/cm3,NA代表阿伏伽德罗常数的值,Fe2+与O2-最短核间距为______pm。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com