
【题目】将 8gSO3 加入 Xg 水中,所形成的溶液里,SO42-和水分子个数之比为 1∶5,则 X 等于( )
A. 9 B. 10.8 C. 12.4 D. 15.6
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】室温下,0.1mol/L氨水10mL,加蒸馏水稀释到1L后,下列变化中正确的是 ①电离度增大 ②C(OH﹣)增大 ③C(H+]增大 ④KW 增大⑤导电性增强 ⑥ ![]() 增大( )
增大( )
A.①②③
B.①③⑤
C.①③⑥
D.②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知298K,1.01×105Pa条件下:2H2(g)+O2(g)═2H2O(g)△H=﹣483.6kJmol﹣1;CO(g)+ ![]() O2(g)═CO2(g)△H=﹣282.9kJmol﹣1则该条件下CO(g)+H2O(g)═H2(g)+CO2(g)的反应热是( )
O2(g)═CO2(g)△H=﹣282.9kJmol﹣1则该条件下CO(g)+H2O(g)═H2(g)+CO2(g)的反应热是( )
A.﹣41.1 kJmol﹣1
B.+200.7 kJmol﹣1
C.﹣766.5 kJmol﹣1
D.+41.1 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上为了处理含有Cr2O ![]() 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量已低于排放标准.关于上述方法,下列说法错误的是( )
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量已低于排放标准.关于上述方法,下列说法错误的是( )
A.阳极反应:Fe﹣2e﹣═Fe2+
B.阴极反应:2H++2e﹣═H2↑
C.在电解过程中工业废水由酸性变为碱性
D.可以将铁电极改为石墨电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用某浓度NaOH溶液滴定一元酸HA的滴定曲线如图所示(横坐标为滴入NaOH的体积,纵坐标为所得混合液的pH).下列判断正确的是( ) 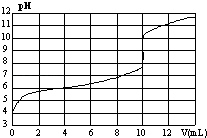
A.HA的浓度为1×10﹣4molL﹣1
B.实验时可选甲基橙作指示剂
C.pH=7时,溶液中c(Na+)>c(A﹣)
D.V=10mL,酸碱恰好中和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1 mol MgCl2中含有 ( )
A. 3.01×1023个Mg2+B. 6.02×1023个Cl-
C. 1 mol Mg2+D. 1 mol Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2SO4溶液和KOH溶液反应时有热量放出,已知反应物的总能量为E1,生成物的总能量为E2。试回答下列问题:
(1)用离子方程式表示中和反应的实质 。
(2)判断E1和E2的大小关系:E1 E2。
(3)已知H+(aq)+OH(aq)![]() H2O(l) ΔH=57.3 kJ/mol,计算下列中和反应中放出的热量。
H2O(l) ΔH=57.3 kJ/mol,计算下列中和反应中放出的热量。
①用20 g NaOH配成稀溶液与足量稀盐酸反应,能放出 kJ的热量。
②用0.1 mol Ba(OH)2配成稀溶液跟足量稀硝酸反应,能放出 kJ的热量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com