
【题目】I.实验室配制90mL 1 mol·L-1的NaOH溶液:
(1)用托盘天平称量NaOH的质量为________g。
(2)配制该溶液时需用的主要仪器有烧杯、玻璃棒、胶头滴管、_______________等。
(3)误差下列情况使配制结果偏大的是________。
A.溶解后未冷却即转移、定容
B.定容时仰视容量瓶刻度线
C.用胶头滴管向容量瓶中加水时溶液凹面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切
D.托盘天平砝码生锈
E.容量瓶内残有少量蒸馏水
Ⅱ. 某同学学习了铁及其化合物的性质,欲设计实验研究铁及其化合物的部分性质。
(1)该同学根据下图装置做相关实验,请回答下列问题:
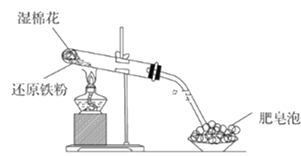
①硬质试管中发生反应的化学方程式为_______________。
②该同学将硬质试管冷却后的少量固体物质溶于稀盐酸得溶液A,向溶液A中滴加KSCN溶液,若溶液未变红色,原因是:________________(用离子方程式表示)。
③该同学向溶液A中滴入一定量的氯水,用该所得溶液腐蚀刻铜板制电路板的主要反应离子方程式___________。
(2)该同学用如下图所示装置制取Fe(OH)2,实验时使用铁屑、6 mol/L硫酸,其他试剂任选。回答下列问题:
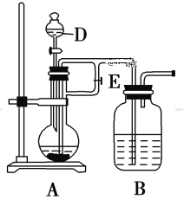
向仪器D中需要放入硫酸,装置B中盛有一定量的NaOH溶液,A中盛有铁屑,实验开始时应先将活塞E打开,待装置中空气排尽后,将活塞E关闭,一段时间后能够长时间观察到装置B中的白色沉淀原因是_____;待A中停止反应后,观察到装置B的白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,写出B中出现该现象的反应方程式______。
【答案】4.0 100mL容量瓶 AD 3Fe+4H2O(g)![]() Fe3O4+4H2 Fe+2Fe3+= 3Fe2+ Cu+2Fe3+=Cu2++2Fe2+ Fe与盐酸反应生成了氢气,隔绝了空气 4Fe(OH)2+O2+2H2O = 4Fe(OH)3
Fe3O4+4H2 Fe+2Fe3+= 3Fe2+ Cu+2Fe3+=Cu2++2Fe2+ Fe与盐酸反应生成了氢气,隔绝了空气 4Fe(OH)2+O2+2H2O = 4Fe(OH)3
【解析】
I.(1)实验室没有90 mL的容量瓶,配制90mL 1 mol·L-1的NaOH溶液应选用100mL容量瓶;
(2)用托盘天平称量4.0g NaOH后,配制该溶液的实验步骤为溶解、转移、洗涤、定容、振荡、装瓶,需用的主要仪器有烧杯、玻璃棒、胶头滴管、100mL容量瓶;
(3)依据溶质的物质的量和溶液的体积是否变化分析判断;
Ⅱ.(1)①硬质试管中还原铁粉高温下与水蒸气反应生成四氧化三铁和氢气;
②若还原铁粉过量,将硬质试管冷却后的少量固体物质溶于稀盐酸后,四氧化三铁溶于盐酸生成氯化铁和氯化亚铁,还原铁粉与反应生成的氯化铁恰好反应生成氯化亚铁,向溶液中滴加KSCN溶液,溶液不会变红色;
③向氯化亚铁溶液中滴入一定量的氯水,氯气将氯化亚铁氧化为氯化铁,氯化铁溶液与铜反应生成氯化亚铁和氯化铜;
(3)实验开始时应先将活塞E打开,铁和稀硫酸反应生成硫酸亚铁和氢气,生成的氢气进入整套实验装置中而排出空气,防止氢氧化亚铁被氧化;关闭活塞E,在气体压强的作用下,A中含有硫酸亚铁溶液被压人B中,硫酸亚铁和氢氧化钠溶液反应,生成Fe(OH)2白色沉淀;氢氧化亚铁不稳定,易被氧气氧化生成红褐色氢氧化铁沉淀,所以待A中停止反应后,空气中氧气将Fe(OH)2氧化,观察到白色沉淀先转化为灰绿色最后转化为红褐色。
I.(1)实验室没有90 mL的容量瓶,配制90mL 1 mol·L-1的NaOH溶液应选用100mL容量瓶,氢氧化钠的物质的量为1 molL-1×0.1L=0.1mol,NaOH的质量为0.1mol×40g/mol=4.0g,则用托盘天平称量NaOH的质量为4.0g,故答案为:4.0;
(2) 用托盘天平称量4.0g NaOH后,配制该溶液的实验步骤为溶解、转移、洗涤、定容、振荡、装瓶,需用的主要仪器有烧杯、玻璃棒、胶头滴管、100mL容量瓶,故答案为:100mL容量瓶;
(3)A、溶解后未冷却即转移、定容,溶液体积会偏小,导致所配溶液浓度偏大,故正确;
B、定容时仰视容量瓶刻度线,导致溶液体积偏大,所配溶液浓度偏小,故错误;
C、用胶头滴管向容量瓶中加水时溶液凹面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切,会导致溶质的物质的量偏小,所配溶液浓度偏小,故错误;
D、托盘天平砝码生锈,会导致所测氢氧化钠的质量偏大,所配溶液浓度偏大,故正确;
E、由稀释定律可知,容量瓶内残有少量蒸馏水,对氢氧化钠的物质的量没有影响,对所配溶液浓度无影响,故错误;
AD正确,故答案为:AD;
Ⅱ.(1)①硬质试管中还原铁粉高温下与水蒸气反应生成四氧化三铁和氢气,反应的化学方程式为3Fe+4H2O(g)![]() Fe3O4+4H2,故答案为:3Fe+4H2O(g)
Fe3O4+4H2,故答案为:3Fe+4H2O(g)![]() Fe3O4+4H2;
Fe3O4+4H2;
②若还原铁粉过量,将硬质试管冷却后的少量固体物质溶于稀盐酸后,四氧化三铁溶于盐酸生成氯化铁和氯化亚铁,还原铁粉与反应生成的氯化铁恰好反应生成氯化亚铁,向溶液中滴加KSCN溶液,溶液不会变红色,还原铁粉与反应生成的氯化铁恰好反应生成氯化亚铁的离子方程式为Fe+2Fe3+= 3Fe2+,故答案为:Fe+2Fe3+= 3Fe2+;
③向氯化亚铁溶液中滴入一定量的氯水,氯气将氯化亚铁氧化为氯化铁,氯化铁溶液与铜反应生成氯化亚铁和氯化铜,则氯化铁溶液腐蚀刻铜板制电路板的主要反应离子方程式为Cu+2Fe3+=Cu2++2Fe2+,故答案为:Cu+2Fe3+=Cu2++2Fe2+;
(3)实验开始时应先将活塞E打开,铁和稀硫酸反应生成硫酸亚铁和氢气,生成的氢气进入整套实验装置中而排出空气,防止氢氧化亚铁被氧化;关闭活塞E,在气体压强的作用下,A中含有硫酸亚铁溶液被压人B中,硫酸亚铁和氢氧化钠溶液反应,生成Fe(OH)2白色沉淀;氢氧化亚铁不稳定,易被氧气氧化生成红褐色氢氧化铁沉淀,所以待A中停止反应后,空气中氧气将Fe(OH)2氧化,观察到白色沉淀先转化为灰绿色最后转化为红褐色,反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为:Fe与盐酸反应生成了氢气,隔绝了空气;4Fe(OH)2+O2+2H2O=4Fe(OH)3。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是( )
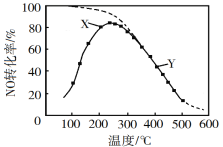
A.反应2NO(g)+O2(g)![]() 2NO2(g)的ΔH>0
2NO2(g)的ΔH>0
B.图中X点所示条件下,延长反应时间不能提高NO转化率
C.图中Y点所示条件下,增加O2的浓度不能提高NO转化率
D.380℃下,c起始(O2)=5.0×104 mol·L1,NO平衡转化率为50%,则平衡常数K>2000
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:
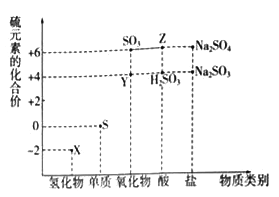
(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有_______(填化学式)。
(2)将X与Y混合,可生成淡黄色固体,该反应中氧化剂与还原剂的物质的量之比为_______。
(3)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为_______。
(4)Na2S2O3是重要的化工原料.从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是______(填代号)。
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(5)已知Na2SO3能被K2Cr2O7氧化为Na2SO4则24mL 0.05molL﹣1的Na2SO3溶液与 20mL 0.02molL﹣1的K2Cr2O7溶液恰好反应时,Cr元素在还原产物中的化合价为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是某同学探究Na2SO3溶液和铬(VI)盐溶液反应规律的实验记录,已知:Cr2O72-(橙色)+ H2O![]() 2CrO42-(黄色)+ 2H+
2CrO42-(黄色)+ 2H+
序号 | a | b | 现象 | |
| 1 | 2 mL 0.05 mol·L1 K2Cr2O7溶液(pH = 2) | 3滴饱和Na2SO3溶液(pH = 9) | 溶液变绿色(含Cr3+) |
2 | 2 mL 0.1 mol·L1 K2CrO4溶液(pH = 8) | 3滴饱和Na2SO3溶液 | 溶液没有明显变化 | |
3 | 2 mL饱和Na2SO3溶液 | 3滴0.05 mol·L1 K2Cr2O7溶液 | 溶液变黄色 | |
4 | 2 mL蒸馏水 | 3滴0.05 mol·L1 K2Cr2O7溶液 | 溶液变成浅橙色 |
下列说法不正确的是
A. 实验1中的绿色溶液中含有SO42-
B. 实验1、2的a溶液中所含的离子种类相同
C. 向实验3溶液中继续滴加过量硫酸可使溶液变为浅橙色
D. 实验4的目的是排除稀释对溶液颜色变化造成的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是
A. ![]() 的溶液中:K+、Na+、CO32-、NO3-
的溶液中:K+、Na+、CO32-、NO3-
B.澄清透明的溶液中:Fe3+、Mg2+、SCN-、Cl-
C.c(Fe2+)=1 mol/L的溶液中: Na+、NH4+、AlO2-、SO42-
D.能使甲基橙变红的溶液中: K+、NH4+、SO42-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色透明酸性溶液中可能含有K+、Fe2+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、SO42-、NO3-中的若干种离子。某同学取50 mL的溶液进行如下实验:
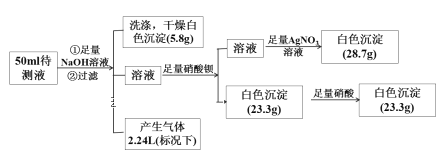
回答下列问题:
(1)原溶液中肯定存在的离子是____________ ,肯定不存在的离子是______________ 。
(2)原溶液中可能存在的离子是______________ 。
(3)原溶液中Cl-的浓度为______________ 。
(4)原溶液中c(K+)范围:_______________ (若不存在,说明理由)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
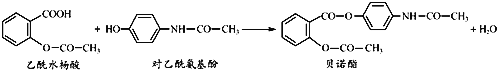
下列有关叙述正确的是
A.贝诺酯分子中有三种含氧官能团
B.贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
C.乙酰水杨酸和对乙酰氨基酚均能与Na2CO3溶液反应放出CO2气体
D.可用FeCl3 溶液区别乙酰水杨酸和对乙酰氨基酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的方程式正确的是
A.电解氯化镁溶液:2Cl–+2H2O![]() H2↑+Cl2↑+2OH–
H2↑+Cl2↑+2OH–
B.碳酸氢铵溶液中加入足量石灰水:Ca2++![]() +OH–=CaCO3↓+H2O
+OH–=CaCO3↓+H2O
C.Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
D.氢氧化钡溶液中加入稀硫酸:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】选用如图所示仪器中的两个或几个(内含物质)组装成实验装置,以验证木炭可被浓硫酸氧化成CO2,下列说法正确的是( )
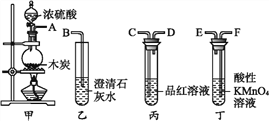
A.按气流从左向右流动,连接装置的正确顺序是A→F→E→C→D→B
B.丁中溶液褪色,乙中溶液变浑浊,说明甲中生成CO2
C.丙中品红溶液褪色,乙中溶液变浑浊,说明甲中生成CO2
D.丁和丙中溶液都褪色,乙中溶液变浑浊,说明甲中有CO2生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com