
【题目】常温下,下列各组离子在指定溶液中能大量共存的是
A. ![]() 的溶液中:K+、Na+、CO32-、NO3-
的溶液中:K+、Na+、CO32-、NO3-
B.澄清透明的溶液中:Fe3+、Mg2+、SCN-、Cl-
C.c(Fe2+)=1 mol/L的溶液中: Na+、NH4+、AlO2-、SO42-
D.能使甲基橙变红的溶液中: K+、NH4+、SO42-、HCO3-
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】向体积均为2 L的两个恒容密闭容器中分别充入1mol SiHCl3,维持容器的温度分别为T1℃和T2℃不变,发生反应:2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g) ΔH1=a kJ·mol1。反应过程中SiHCl3的转化率随时间的变化如图所示。下列说法正确的是( )
SiH2Cl2(g)+SiCl4(g) ΔH1=a kJ·mol1。反应过程中SiHCl3的转化率随时间的变化如图所示。下列说法正确的是( )

A.T1<T2
B.T1℃时,0~100min反应的平均速率υ(SiHCl3)=0.001mol·(L·min)-1
C.T2℃时,反应的平衡常数:K=1/64
D.T2℃时,使用合适的催化剂,可使SiHCl3的平衡转化率与T1℃时相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应路线及所给信息填空。
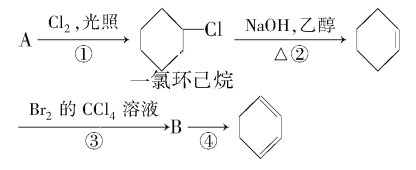
(1)A的结构简式是________。
(2)①②的反应类型分别是_______,②的反应方程式是_________。
(3)反应③的化学方程式是________。
(4)反应④的化学方程式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表前三周期的一部分:
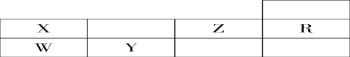
(1)判断X __________ Y __________ Z __________W__________R ________(写元素符号)。
(2)写出X的氢化物的化学式;__________,W的氢化物的化学式__________,其沸点比较:__________>________(填化学式)
(3)下图是X的基态原子的电子排布图,其中有一个是错误的,它不能作为基态原子的电子排布图是因为它不符合________。
①![]()
②![]()
(4)以上五种元素中,________(填元素符号)元素第一电离能最大。__________元素电负性最大,Y的基态原子的电子排布式为__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是周期表的一部分,其中的编号代表对应的元素。
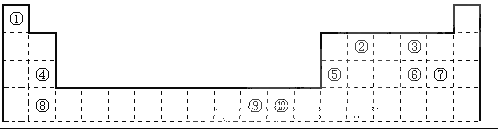
请回答下列问题:
(1)表中属于d区的元素是_______(填编号)。
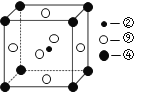
(2)科学发现,②、④、⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如图(图中②、④、⑨分别位于晶胞的体心、顶点、面心),则该化合物的化学式为 _______(用对应的元素符号表示)。
(3)元素②的一种氢化物是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是 _______。
a 分子中含有氢键 b 属于非极性分子
c 含有4个σ键和1个π键 d 该氢化物分子中,②原子采用sp2杂化
(4)某元素的外围电子排布式为nsnnpn+1,该元素可与①形成三角锥形的分子X, X在①与③形成的分子Y中的溶解度很大,其主要原因是________。
(5)将过量的X通入含有元素⑩的硫酸盐溶液中,现象是________,反应的离子方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.实验室配制90mL 1 mol·L-1的NaOH溶液:
(1)用托盘天平称量NaOH的质量为________g。
(2)配制该溶液时需用的主要仪器有烧杯、玻璃棒、胶头滴管、_______________等。
(3)误差下列情况使配制结果偏大的是________。
A.溶解后未冷却即转移、定容
B.定容时仰视容量瓶刻度线
C.用胶头滴管向容量瓶中加水时溶液凹面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切
D.托盘天平砝码生锈
E.容量瓶内残有少量蒸馏水
Ⅱ. 某同学学习了铁及其化合物的性质,欲设计实验研究铁及其化合物的部分性质。
(1)该同学根据下图装置做相关实验,请回答下列问题:
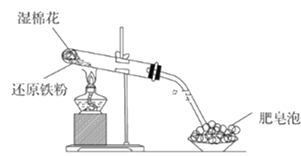
①硬质试管中发生反应的化学方程式为_______________。
②该同学将硬质试管冷却后的少量固体物质溶于稀盐酸得溶液A,向溶液A中滴加KSCN溶液,若溶液未变红色,原因是:________________(用离子方程式表示)。
③该同学向溶液A中滴入一定量的氯水,用该所得溶液腐蚀刻铜板制电路板的主要反应离子方程式___________。
(2)该同学用如下图所示装置制取Fe(OH)2,实验时使用铁屑、6 mol/L硫酸,其他试剂任选。回答下列问题:
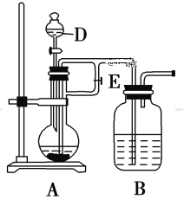
向仪器D中需要放入硫酸,装置B中盛有一定量的NaOH溶液,A中盛有铁屑,实验开始时应先将活塞E打开,待装置中空气排尽后,将活塞E关闭,一段时间后能够长时间观察到装置B中的白色沉淀原因是_____;待A中停止反应后,观察到装置B的白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,写出B中出现该现象的反应方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )

下列图示与对应的叙述符合的是( )
A.图甲实线、虚线分别表示某可逆反应未使用催化剂和使用催化剂的正、逆反应速率随时间的变化
B.图乙表示反应2SO2(g)+O2(g) ![]() 2SO3(g)△H<0的平衡常数K与温度和压强的关系
2SO3(g)△H<0的平衡常数K与温度和压强的关系
C.图丙表示向0.1mol/L的NH4Cl溶液中滴加0.1mol/L的HCl溶液时,溶液中 随HCl溶液体积变化关系
随HCl溶液体积变化关系
D.图丁表示常温下向20mL pH=3的醋酸中滴加pH=11的NaOH溶液,溶液的pH随NaOH溶液体积的变化关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如何降低大气中CO2的含量及有效地开发利用碳资源的研究越来越紧迫。请运用化学反应原理的相关知识研究碳及其化合物的性质.
(1)工业上在恒容密闭容器中用下列反应合成甲醇:CO(g)+2H2(g)![]() CH3OH(g) △H
CH3OH(g) △H
如表所列数据是反应在不同温度下的化学平衡常数(K)。
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
①由表中数据判断△H ________0 ( 填“>”、 “ < “ 或 “ = ”) ;
②判断反应达到平衡状态的依据是________.
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的平均相对分子质量不变
C.混合气体的密度不变
D.CH3OH、CO、H2的浓度都不再发生变化
③借助上表数据判断,要提高CO的转化率,可采取的措施是________.
A.升温 B.充入更多H2 C.分离出甲醇 D.加入催化剂
(2)CH3OH可以用做燃料电池的燃料,以甲醇与氧气的反应为原理设计,现有电解质溶液是KOH溶液的燃料电池。请写出该电池负极的电极反应式:____________________.
(3)向BaSO4沉淀中加入饱和碳酸钠溶液,充分搅拌,弃去上层清液,如此处理多次,可使BaSO4全部转化为BaCO3,发生反应:BaSO4(s)+CO32-(aq)BaCO3(s)+SO42-(aq)。已知某温度下该反应的平衡常数K=4.0×10-2,BaSO4的Ksp=1.0×10-10,则 BaCO3的溶度积Ksp=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正硼酸(H3BO3)是一种片层状结构白色晶体,有与石墨相似的层状结构。层内的 H3BO3 分子通过氢键相连(如下图)。下列有关说法正确的是( )
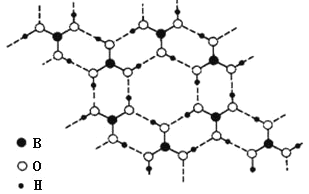
A.正硼酸晶体属于原子晶体
B.正硼酸晶体层与层之间的作用力是范德华力
C.含 1molH3BO3 的晶体中有 2mol 氢键
D.分子中 B 原子杂化轨道的类型为 sp3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com