
【题目】25℃时,Ag2CrO4在不同浓度CrO42-溶液中的溶解度如图所示,下列说法正确的是![]()
![]()
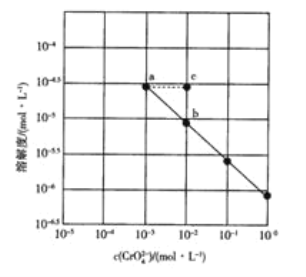
A.图中a、b两点c(Ag+)相同
B.图中a点Ag2CrO4的溶度积比b点的大
C.在a点向溶液中加如入少量AgNO3,溶解度可变为c点
D.该温度下,Ag2CrO4溶度积的数量级为10-12
【答案】D
【解析】
A. 曲线为达到沉淀溶解平衡时的曲线,a点和b点c(CrO42-)不同;
B. 溶度积只与温度有关;
C. a点达到溶解平衡,在a点时向溶液中加入少量的AgNO3,可析出Ag2CrO4,但仍为沉淀的溶解平衡;
D. 根据数据计算Ksp(Ag2CrO4)。
A. 曲线为达到沉淀溶解平衡时的曲线,a点和b点c(CrO42-)不同,那么c(Ag+)=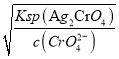 不同,A项错误;
不同,A项错误;
B. 溶度积只与温度有关,温度不变Ksp不变,B项错误;
C. a点达到溶解平衡,在a点时向溶液中加入少量的AgNO3,可析出Ag2CrO4,但仍为沉淀的溶解平衡,C项错误;
D. 利用b点数据进行计算,b点c(CrO42-)=10-2mol/L,溶解度为10-5mol/L,那么Ksp(Ag2CrO4)=c2(Ag+)c(CrO42-)=(2×10-5)2×10-2=4×10-12,数量级为10-12,D项正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】一定温度压强下,在容积可变的密闭容器中发生反应CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0,则下列说法不正确的是
CO2(g)+H2(g) ΔH<0,则下列说法不正确的是
A.其他条件不变,加催化剂与不加催化剂其ΔH 相同
B.当达到平衡,向体系中充入CO2其平衡向左移动
C.理论上该反应可设计成燃料电池,H2O(g)在正极上发生还原反应
D.平衡混合气体通入NaOH溶液恰好反应,升高温度溶液碱性增强,其pH一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某1L待测溶液中除含有0.2mol/L的Na+外,还可能含有下列离子中的一种或多种:K+、NH4+、Fe3+、Ba2+、Cl-、Br-、CO32-、HCO3-、SO32-、SO42-。现进行如下实验操作(每次实验所加试剂均过量):
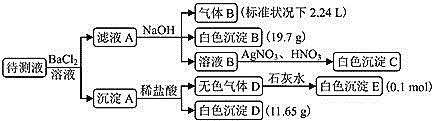
下列说法正确的是
A.待测液中一定含有NH4+、HCO3-和Cl-
B.待测液中一定没有Fe3+和Ba2+,可能含有Br-
C.生成白色沉淀B的离子方程式为:![]()
D.待测液中一定含有K+,且c(K+)=0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是:
A. 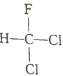 和
和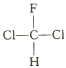 互为同分异构体
互为同分异构体
B. 15g甲基(﹣CH3)含有的电子数是9NA
C. 7.8g苯中含有的碳碳双键数为0.3NA
D. 标准状况下,2.24 L CCl4中的原子总数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:
![]() +H2O
+H2O
![]()
项目 | 相对分子质量 | 密度/(gcm3) | 沸点/℃ | 水中溶解性 |
异戊醇 | 88 | 0.8123 | 131 | 微溶 |
乙酸 | 60 | 1.0492 | 118 | 溶 |
乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
实验步骤:
在A中加入4.4 g异戊醇、6.0 g乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A50 min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9 g。
回答下列问题:
(1)仪器B的作用是_______。
(2)在洗涤操作中,第一次水洗的主要目的是___,第二次水洗的主要目的是___。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后______(填标号)。
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)本实验中加入过量乙酸的目的是______;加入少量无水MgSO4的目的是______。
(5)在蒸馏操作中,仪器选择及安装都正确的是_______(填标号)。
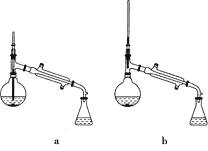
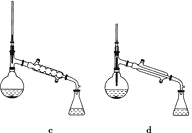
(6)本实验的产率是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油是一种重要的资源。A~F是常见有机物,它们之间的转化关系如图1所示(部分产物和反应条件已略去),其中A的产量可以用来衡量一个国家的石油化工发展水平,E是最简单的芳香烃。回答下列问题:

(1)步骤②所用试剂X为___________(写化学式),D的官能团名称是_______;
(2)F的结构简式为________________,步骤①的反应类型:___________;
(3)写出下列步骤中的化学方程式(注明反应条件):
步骤③_____________________________________;
步骤④_______________________________________;
(4)用图2所示实验装置制取乙酸乙酯。请回答:试管b中所装溶液应为_____,乙酸乙酯生成后,分离出产品时的操作方法是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了研究Mg(OH)2溶于铵盐溶液的原因,进行如下实验:
①向2mL 0.2mol/LMgCl2溶液中滴加1mol/LNaOH溶液至不再产生沉淀,将浊液分为2等份。
②向一份中逐滴加入4mol/L NH4Cl溶液,另一份中逐滴加入4mol/L CH3COONH4溶液(pH≈7),边滴加边测定其中沉淀的量,沉淀的量与铵盐溶液的体积的关系如图。
③将①中的NaOH溶液用氨水替换,重复上述实验。
下列说法不正确的是
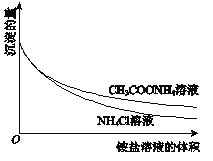
A. Mg(OH)2浊液中存在:Mg(OH)2(s)![]() Mg2+(aq)+2OH﹣(aq)
Mg2+(aq)+2OH﹣(aq)
B. ②中两组实验中均存在反应:Mg(OH)2+2NH4+=Mg2++2NH3H2O
C. H+可能参与了NH4Cl溶液溶解Mg(OH)2的过程
D. ③中获得的图象与②相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池是目前电池研究的热点之一。某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极下列叙述不正确的是( )

A.a极是负极,该电极上发生氧化反应
B.b极发生的电极反应是O2+4OH--4e-=2H2O
C.电池总反应方程式为2H2+O2=2H2O
D.氢氧燃料电池是一种具有应用前景的绿色电源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辉钼精矿主要成分是二氧化钼(MoS2),还含有石灰石、石英、黄铜矿(CuFeS2)等杂质。某学习小组设计提取MoS2的过程如下:下列说法错误的是
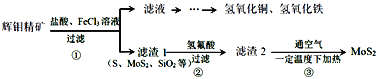
A.为加快辉钼精矿溶解,可将矿石粉粹并适当加热
B.加滤液中含Ca2+、Fe2+、Fe3+、Cu2+、H+等离子
C.以上①②③过程均涉及氧化还原反应
D.步骤③温度不宜过高,以免MoS2被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com