
【题目】室温下,甘氨酸在水溶液中主要以 、
、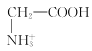 和
和![]() 三种微粒形式存在,实验测得不同pH甘氨酸溶液中各成分分布分数δ与pH关系如图所示。下列说法正确的是( )
三种微粒形式存在,实验测得不同pH甘氨酸溶液中各成分分布分数δ与pH关系如图所示。下列说法正确的是( )
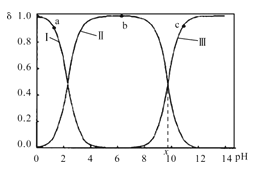
A.a点溶液中,水的电离程度大于b点
B.c点溶液中,c(![]() )>c(
)>c( )
)
C.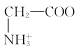 +H2O
+H2O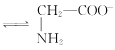 +H3O+的平衡常数为x
+H3O+的平衡常数为x
D.a点溶液中,存在关系式:c(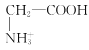 )+c(H+)=c(
)+c(H+)=c(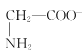 )+c(OH-)
)+c(OH-)
科目:高中化学 来源: 题型:
【题目】下列有关化学平衡常数的描述中正确的是( )
A. 化学平衡常数的大小取决于化学反应本身,与其他外界条件无关
B. 相同温度下,反应A+BC与反应CA+B的化学平衡常数相同
C. 反应2SO2(g)+O2(g)2SO3(g) ΔH<0的化学平衡常数随温度升高而增大
D. 反应A(g)+B(g)2C(g)的平衡常数表达式为K=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在工业废气和汽车尾气中含有多种氮氧化物,氮氧化物能破坏臭氧层,产生光化学烟雾,是造成大气污染的来源之一。
(1)处理 NO 尾气通常是将 NO 与 O2 混合通入碱液中吸收。已知一定条件下有下列反应:
Ⅰ:2N2O5(g) ![]() 4NO2(g)+O2(g) △H1
4NO2(g)+O2(g) △H1
Ⅱ:2NO2(g)![]() 2NO(g)+O2(g) △H2
2NO(g)+O2(g) △H2
Ⅲ:2NaOH(aq)+N2O5(g)=2NaNO3(aq)+H2O(1) △H3
写出 NO 和O2 的混合物溶于NaOH 溶液生成硝酸盐的热化学方程式______。
(2)常温下,NO 极易被 O2 氧化为 NO2,温度高于 423K 时,NO2 发生分解:2NO2(g) ![]() 2NO(g)+O2(g)△H=114kJ·mol -1,实验测得:
2NO(g)+O2(g)△H=114kJ·mol -1,实验测得:
υ正=υ(NO2)消耗=k 正C2(NO2), υ逆=υ(NO)消耗=2υ(O2) 消耗=k 逆c2(NO)·c( O2),k 正、k 逆 为速率常数,受温度影响。不同温度下,将 NO2 置于体积为 VL 的密闭容器中,NO2 的物质的量的浓度与反应时间的关系如图所示:
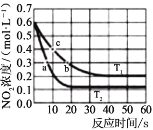
①T1 温度下 0-10s 内,O2 的反应速率υ(O2)=______、平衡常数 KT1=___________。
②T1 温度下,要减少 NO2 的分解率,并缩短达到平衡的时间,可采取的单一措施有______
③平衡常数KT1 ______ KT2 填“大于”“小于”或“等于”,下同);反应速率υa_______υb。
④计算 c 处υ正/υ逆=______。
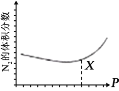
(3)NO 也 可 通 过 如 下 反 应 处 理 :6NO(g)+4NH3(g) =5N2(g) +6H2O(g);一定条件下,平衡时 N2 的体积分数与压强的关系如图所示。N2 的体积分数先减小后增大的原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,原子最外层电子数之和为17。其中W、X、Y三种元素的简单离子的核外电子排布相同,且可形成结构如图所示的化合物。下列说法正确的是( )
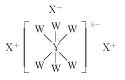
A.原子半径:Z>Y>X>W
B.X与Z形成的化合物会抑制水的电离
C.X、Z均能形成两种常见氧化物
D.W的最高价氧化物对应水化物的酸性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列电化学习题:
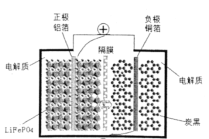
(1)某电池工作时的总反应可简化为:![]() ,电池中的固体电解质可传导Li+,则放电时,正极的电极反应式为________。充电时,Li+迁移方向为____(填“由左向右”或“由右向左”),图中聚合物隔膜应为____(填“阳”或“阴”)离子交换膜。
,电池中的固体电解质可传导Li+,则放电时,正极的电极反应式为________。充电时,Li+迁移方向为____(填“由左向右”或“由右向左”),图中聚合物隔膜应为____(填“阳”或“阴”)离子交换膜。
(2)使用间接电解法可处理燃煤烟气中的NO,装置如下图左。已知电解池的阴极室中溶液在pH在4~7(酸性)之间,试写出阴极的电极反应式______;用离子方程式表示吸收塔中除去NO的原理________。

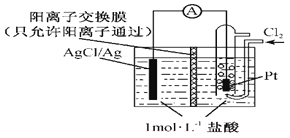
(3)某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。则负极反应为_______,放电时交换膜右侧溶液中酸性____(填“增强”、“减弱”或“不变”),若用KCl溶液代替盐酸,则电池总反应______(填“改变”或“不变”)。
(4)在生产和生活中采取了多种防止金属腐蚀的措施,利用原电池原理保护金属的方法是_______。
(5)纯锌与酸反应,为什么加入少许硫酸铜后会加速反应_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程表达式中,属于电离方程式的是( )
A. HSO3-+H3O+![]() H2SO3+H2OB. NH3·H2O
H2SO3+H2OB. NH3·H2O![]() NH4++OH-
NH4++OH-
C. CH3COO-+H2O![]() CH3COOH+OH-D. HCO3-+OH-=H2O+CO32-
CH3COOH+OH-D. HCO3-+OH-=H2O+CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用元素的化合价推测物质的性质是化学研究的重要手段。图是硫元素的常见化合价与部分物质类别的对应关系。
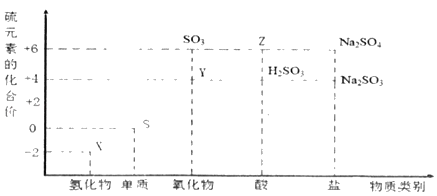
(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的氧化物为_____(填化学式)。
(2)将X与Y混合可生成淡黄色固体,该反应的化学方程式为_____。
(3)Z的浓溶液与碳在一定条件下可以发生反应,体现了Z的_____性。
(4)写出硫与浓硫酸在加热条件下反应的化学方程式_____。
(5)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方法理论上可行的是_____(填字母)。
a.Na2SO3+S b.Na2S+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]()
![]() 根据以上热化学方程式,下列判断 不 正 确的是
根据以上热化学方程式,下列判断 不 正 确的是
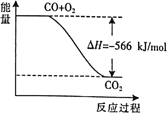
A.上图可表示由CO生成![]() 的反应过程和能量关系
的反应过程和能量关系
B.CO的燃烧热![]()
C.![]()
D.![]() 与
与![]() 反应放出
反应放出![]() 热量时,电子转移数为
热量时,电子转移数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见如图,电池总反应可表示为2H2+O2═2H2O,下列有关说法正确的是( )
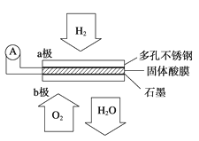
A. 电流通过外电路从a极流向b极
B. b极上的电极反应式为O2+2H2O+4e-═4OH-
C. 每转移0.2 mol电子,在负极上消耗标况下1.12 L的O2
D. H+由a极通过固体酸电解质传递到b极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com