
【题目】下列叙述中,正确的是( )
A.共价化合物中可能含离子键
B.离子化合物中可能含共价键
C.非金属原子间不可能形成离子键
D.非极性键只存在于双原子单质分子里
 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
【题目】可逆反应aA(s)+bB(g) ![]() cC(g)+dD(g);△H=QkJ/mol,在反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如下图所示:则以下正确的是
cC(g)+dD(g);△H=QkJ/mol,在反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如下图所示:则以下正确的是

A. T1>T2,Q>0
B. T2>T1,Q>0
C. P1<P2,a+b=c+d
D. P1<P2,b=c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Ka(HCOOH)=1.77×104,Ka(CH3COOH)=1.75×105,Kb(NH3·H2O) =1.75×105,下列说法正确的是
A. 相同体积 pH 均为 3 的 HCOOH 和 CH3COOH 溶液,中和 NaOH 的能力相同
B. 0.2 mol·L-1 HCOOH 与 0.1 mol·L-1 NaOH 等体积混合后:c(HCOO-)+c(OH-)>c(Na+)+c(H+)
C. 均为 0.1 mol·L-1 的 HCOOH 和 NH3·H2O 溶液中水的电离程度相同
D. 0.1 mol·L-1 CH3COOH 溶液中逐滴加入 0.1 mol·L-1 HCl溶液中 不变。
不变。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭烧瓶中注入NO2,在25℃时建立下列平衡:2NO2![]() N2O4(正反应为放热反应),若把烧瓶置于100℃的沸水中,下列情况:①颜色,②平均相对分子质量,③质量,④压强,⑤密度。其中不变的是
N2O4(正反应为放热反应),若把烧瓶置于100℃的沸水中,下列情况:①颜色,②平均相对分子质量,③质量,④压强,⑤密度。其中不变的是
A. ②④ B. ③④ C. ③⑤ D. ①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知苯乙烯的结构为![]() 。有关该物质的下列说法正确的是( )
。有关该物质的下列说法正确的是( )
A. 该物质在一定条件下和氢气完全加成,加成产物的一溴取代物 6 种
B. 该物质能使溴水和酸性高锰酸钾溶液褪色,褪色原理完全相同
C. 苯乙烯分子的所有原子不可能在同一平面上
D. 除去乙苯中混有的苯乙烯可以通入等量氢气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去粗盐中含有的可溶性杂质CaCl2、MgCl2和Na2SO4,需进行下列实验操作,请在( )中填写所使用和除杂试剂的化学式,在![]() 中填写实验操作名称。写出符合下列条件的离子方程式
中填写实验操作名称。写出符合下列条件的离子方程式

(1)①___________ 、 ____________;②_______________________;③____________;④____________;⑤____________;⑥____________;⑦____________。
(2)除去Mg2+的离子方程式_______________________________________________
(3)除去SO42-的离子方程式______________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合图回答问题:
(1)学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容如图Ⅰ,现欲用此硫酸配制配制成浓度为0.50molL﹣1的稀硫酸100mL.①所需玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外还需________。
②所取浓硫酸的体积为________ mL。
(2)写出上述装置中仪器的名称:②________;③________。
(3)若利用装置Ⅱ分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物,还缺少的仪器有________,将仪器补充完整后进行的实验操作的名称为________。
(4)实验室常用装置Ⅲ分离碘水中的碘, 进行该操作时,需在碘水中加一试剂,在选择试剂时,下列性质你认为哪些性质是必需的:________(填序号)。①常温下为液态 ②I2在其中溶解程度大 ③与水互不相容 ④密度要比水大。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向盛有乙醇的烧杯中投入一小块金属钠,可以观察到的现象是( )
A.钠块沉在乙醇液面下面B.钠块熔成小球
C.钠块在乙醇液面上游动D.钠块表面无气泡产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼(Mo)是一种难熔稀有金属,我国的钼储量居世界前列,钼及其合金在冶金、环保和航天等方面有着广泛的应用。
(1)Mo可被发烟硝酸及氢氟酸氧化生成X和Y(少量),X和Y中Mo价态相同,硝酸本身被还原为NO2,该反应中氧化剂与还原剂的物质的量之比为6:1,则Mo在氧化产物中的化合价为___________;
(2)已知:2Mo(s)+3O2(g)===2MoO3(s) △H1;
MoS2(s)+2O2(g)===Mo(s)+2SO2(g) △H2。
写出MoS2(s)与氧气反应生成MoO3(s)的热化学方程式_____________________________;
(3)碳酸钠作固硫剂并用氢还原辉钼矿的原理为
MoS2(s)+4H2(g)+2Na2CO3(s)![]() Mo(s)+2CO (g)+4H2O(g)+2Na2S(s) △H,实验测得平衡时的有关变化曲线如图所示。
Mo(s)+2CO (g)+4H2O(g)+2Na2S(s) △H,实验测得平衡时的有关变化曲线如图所示。
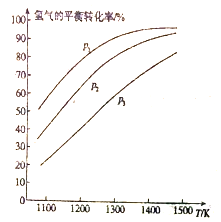
(a)不同压强下温度与H2平衡转化率的关系

(b)0.1MPa下温度与平衡时气体成分的关系
①由图(a)可知,该反应△H___________0(填“>”或“<”),p1、p2、p3由大到小的顺序为___________;
②由图(b)可知,B点时H2的平衡转化率为___________;
③A点对应的平衡常数K=___________(MPa)2。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(4)电氧化法提纯钼的原理:将辉钼矿(MoS2)放入装有食盐水的电解槽中,用惰性电极电解,MoS2被氧化为MoO42-和SO42-。
①辉钼矿应放入电解槽的___________(填“阴极区”或“阳极区”);
②阴极的电极反应式为_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com