
【题目】将含有C、H、O的某有机物3.24 g装入元素分析装置,通入足量的O2使它完全燃烧,将生成的气体依次通过氯化钙干燥管(A)和碱石灰干燥管(B)。测得A管增重2.16 g,B管增重9.24 g。已知有机物的相对分子质量为108。
(1)燃烧此化合物3.24 g,须消耗的氧气的质量是多少?__________
(2)求此化合物的分子式。__________
(3)该化合物1分子中存在1个苯环和1个羟基,试写出其同分异构体的结构简式和名称。_________
【答案】8.16g C7H8O 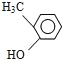 (邻甲基苯酚)、
(邻甲基苯酚)、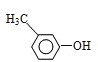 (间甲基苯酚)、
(间甲基苯酚)、![]() (对甲基苯酚)、
(对甲基苯酚)、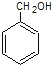 (苯甲醇)
(苯甲醇)
【解析】
(1)A管质量增加了2.16g为生成水的质量,B管增加了9.24g为生成二氧化碳的质量,根据质量守恒计算消耗氧气的质量;
(2)根据n=![]() 计算二氧化碳、水、氧气的物质的量,根据原子守恒计算3.24g有机物中C、H、O原子物质的量,进而确定最简式,结合有机物的相对分子质量为108,进而确定分子式;
计算二氧化碳、水、氧气的物质的量,根据原子守恒计算3.24g有机物中C、H、O原子物质的量,进而确定最简式,结合有机物的相对分子质量为108,进而确定分子式;
(3)该化合物的分子中有1个苯环和1个羟基,且只有一个侧链,则侧链为-CH2OH,据此写出满足条件的有机物的结构简式。
(1)A管质量增加了2.16g为生成水的质量,B管增加了9.24g为生成二氧化碳的质量,根据质量守恒可知,消耗氧气的质量=2.16g+9.24g3.24g=8.16g,
故答案为:8.16g;
(2)2.16g水的物质的量=![]() =0.12mol,n(H)=0.24mol,
=0.12mol,n(H)=0.24mol,
9.24g二氧化碳的物质的量=![]() =0.21mol,n(C)=0.21mol,
=0.21mol,n(C)=0.21mol,
8.16g氧气的物质的量=![]() =0.255mol,
=0.255mol,
3.24g有机物中n(O)=0.21mol×2+0.12mol0.255mol×2=0.03mol,
3.24g有机物中C、H、O原子物质的量之比为:0.21mol:0.24mol:0.03mol=7:8:1,
故该有机物最简式为C7H8O,
有机物的相对分子质量为108,而最简式C7H8O的式量=12×7+8+16=108,故其最简式即为分子式,即有机物分子式为:C7H8O,
故答案为:C7H8O;
(3)若该有机物含有1个苯环和羟基,C7H8O的不饱和度=![]() =4,侧链不含不饱和键,若只有1个侧链,则为CH2OH,若侧链有2个,为OH、CH3,有邻、间、对三种位置关系,故符合条件的有机物的结构简式为:
=4,侧链不含不饱和键,若只有1个侧链,则为CH2OH,若侧链有2个,为OH、CH3,有邻、间、对三种位置关系,故符合条件的有机物的结构简式为: (邻甲基苯酚)、
(邻甲基苯酚)、 (间甲基苯酚)、
(间甲基苯酚)、![]() (对甲基苯酚)、
(对甲基苯酚)、 (苯甲醇),
(苯甲醇),
故答案为: (邻甲基苯酚)、
(邻甲基苯酚)、 (间甲基苯酚)、
(间甲基苯酚)、![]() (对甲基苯酚)、
(对甲基苯酚)、 (苯甲醇)。
(苯甲醇)。


 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:
【题目】茉莉酸甲酯具有强烈而持久的茉莉花香,广泛用于人工配制的茉莉精油中,其结构简式如图所示。下列关于茉莉酸甲酯的说法中不正确的是( )
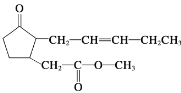
A.分子式为C13H20O3
B.茉莉酸甲酯易溶于水
C.能发生氧化、水解和加聚反应
D.分子中含2个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)(填序号)下列实验操作或对实验事实的叙述正确的是______。
①用稀HNO3清洗做过银镜反应实验的试管
②配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌
③用碱式滴定管量取20.00 mL 0.1000 mol·L-1KMnO4溶液
④用托盘天平称取10.50 g干燥的NaCl固体
⑤不慎将苯酚溶液沾到皮肤上,立即用酒精清洗
⑥用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物
⑦向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体
⑧配制Al2(SO4)3溶液时,加入少量的稀硫酸
(2)为了确定乙醇分子的结构简式是CH3—O—CH3还是CH3CH2OH,实验室利用如图所示的实验装置,测定乙醇与钠反应(ΔH<0)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子的数目。试完成下列问题:
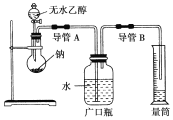
指出实验装置中的错误________。
②若实验中用含有少量水的乙醇代替相同质量的无水乙醇,相同条件下,测得的氢气体积将______(填“偏大”、“偏小”或“不变”)。
③请指出能使该实验安全、顺利进行的关键实验步骤________________(至少指出两个关键步骤)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用系统命名法命名烃A:_______________________________;
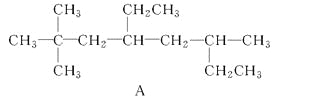
烃A的一氯代物具有不同沸点的产物有________种。
(2)有机物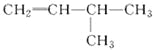 的系统名称是______________,将其在催化剂存在下完全氢化,所得烷烃的系统名称是__________________。
的系统名称是______________,将其在催化剂存在下完全氢化,所得烷烃的系统名称是__________________。
(3)有机物![]() 的系统名称是______________,将其在催化剂存在下完全氢化,所得烷烃的系统名称是__________________。
的系统名称是______________,将其在催化剂存在下完全氢化,所得烷烃的系统名称是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯酚![]() 在一定条件下能与H2加成得到环己醇
在一定条件下能与H2加成得到环己醇![]() 。下面关于这两种物质的叙述中,错误的是
。下面关于这两种物质的叙述中,错误的是
A. 常温时在水中的溶解性都比乙醇差
B. 都能与金属Na、K等金属反应放出氢气
C. 都显弱酸性,且酸性都弱于碳酸
D. 苯酚与FeCl3溶液作用显紫色,环己醇加入FeCl3溶液,液体分层,上层无色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):

H2SO4(浓)+NaBr ![]() NaHSO4+HBr↑
NaHSO4+HBr↑
CH3CH2OH+HBr![]() CH3CH2Br+H2O。有关数据见下表:
CH3CH2Br+H2O。有关数据见下表:
乙醇 | 溴乙烷 | 溴 | |
状态 | 无色液体 | 无色液体 | 深红色液体 |
密度/(g·cm-3) | 0.79 | 1.44 | 3.1 |
沸点/℃ | 78.5 | 38.4 | 59 |
(1)A装置的名称是______________。
(2)实验中用滴液漏斗代替分液漏斗的优点为_______________________。
(3)给A加热温度过高或浓硫酸的浓度过大,均会使C中收集到的粗产品呈橙色,原因是A中发生了副反应,写出此反应的化学方程式________________________。
(4)给A加热的目的是________________________,F接橡皮管导入稀NaOH溶液,其目的主要是___________________。
(5)图中C中的导管E的末端须在水面以下,其目的是______________________。
(6)粗产品洗涤、分液后,再经过蒸馏水洗涤、分液,然后加入少量的无水硫酸镁固体,静置片刻后过滤,再将所得滤液进行蒸馏,收集到的馏分约10.0 g。从乙醇的角度考虑,本实验所得溴乙烷的产率是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
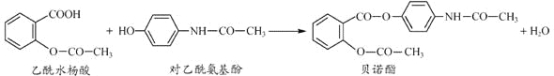
下列有关叙述正确的是( )
A. 贝诺酯分子中有三种含氧官能团
B. 可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚
C. 乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应
D. 贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积可变的密闭容器中存在如下反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H<0
CO2(g)+H2(g) △H<0

下列分析中正确的是
A、图Ⅱ研究的只是t0时使用催化剂对反应速率的影响
B、图Ⅰ研究的是t0时缩小容器体积对反应速率的影响
C、图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高
D、图Ⅲ研究的是催化剂对化学平衡的影响,且甲使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】精炼铜工业中阳极泥的综合利用具有重要意义。一种从铜阳极泥(主要含有铜、银、金、少量的镍)中分离提取多种金属元素的工艺流程如下:

已知:ⅰ分金液中含金离子主要成分为[AuCl4]-;分金渣的主要成分为AgCl;
ⅱ分银液中含银离子主要成分为[Ag(SO3)2]3-,且存在[Ag(SO3)2]3—![]() Ag++2SO
Ag++2SO![]()
ⅲ“分铜”时各元素的浸出率如下表所示。

(1)由表中数据可知,Ni的金属性比Cu______。分铜渣中银元素的存在形式为(用化学用语表示)______。“分铜”时,如果反应温度过高,会有明显的放出气体现象,原因是_______。
(2)“分金”时,单质金发生反应的离子方程式为________。
(3)Na2SO3溶液中含硫微粒物质的量分数与pH的关系如图所示。

“沉银”时,需加入硫酸调节溶液的pH=4,分析能够析出AgCl的原因为_______。调节溶液的pH不能过低,理由为______(用离子方程式表示)。
(4)已知Ksp[Ag2SO4]=1.4×10-5,沉银时为了保证不析出Ag2SO4,应如何控制溶液中SO42—浓度(假定溶液中Ag+浓度为0.1mol/L)。________。
(5)工业上,用镍为阳极,电解0.1 mol/L NiCl2溶液与一定量NH4Cl组成的混合溶液,可得高纯度的球形超细镍粉。当其他条件一定时,NH4Cl的浓度对阴极电流效率及镍的成粉率的影响如图所示:
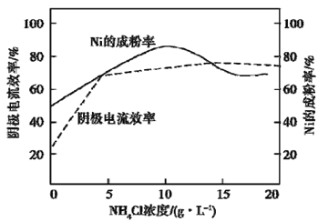
为获得髙纯度的球形超细镍粉,NH4Cl溶液的浓度最好控制为_______g/L,当NH4Cl溶液的浓度大于15g/L时,阴极有无色无味气体生成,导致阴极电流效率降低,该气体为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com