
| A、此时正反应速率一定大于逆反应速率 |
| B、反应一定放出热量 |
| C、平衡时反应物的浓度一定降低 |
| D、平衡时生成物的质量分数一定增加 |


科目:高中化学 来源: 题型:
| A、饱和氯水中 Cl-、NO3-、Na+、SO32- |
| B、强酸性的溶液中 C6H5O-、K+、SO42-、Br- |
| C、Na2S溶液中 SO42-、K+、Cl-、Cu2+ |
| D、强碱性的溶液中 NO3-、I-、Na+、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
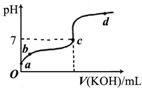 已知某温度下CH3COOH的电离常数K=1.6×10-5.该温度下向20mL0.01mol/LCH3COOH溶液中逐滴加入0.01mol/L KOH溶液,其pH变化曲线如图所示(忽略温度变化).请回答下列有关问题:
已知某温度下CH3COOH的电离常数K=1.6×10-5.该温度下向20mL0.01mol/LCH3COOH溶液中逐滴加入0.01mol/L KOH溶液,其pH变化曲线如图所示(忽略温度变化).请回答下列有关问题:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HI、H2、I2的浓度不再发生变化 |
| B、HI、H2、I2的浓度相等 |
| C、HI、H2、I2在密闭容器中共存 |
| D、反应停止,正、逆反应速率都等于零 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、光导纤维的主要成分是二氧化硅 |
| B、硅酸不溶于水,且硅酸的酸性比碳酸弱 |
| C、不用带玻璃瓶塞的试剂瓶盛放NaOH溶液 |
| D、二氧化硅不溶于水,也不溶于任何酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、饱和氯水中:Cl-、NO3-、Na+、SO32- |
| B、c(H+)=1.0×10-13mol/L溶液中:CH3COO-、K+、SO42-、Br- |
| C、与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- |
| D、pH=12的溶液中:NO3-、I-、Na+、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com