
����Ŀ����������(SO2)��һ���ڿռ������������ѧ�����ʿ�̽�������ܵ��㷺�о���һ�����塣
��.ij�о�С�������һ���Ʊ�������SO2�������ʵ�װ�ã���ͼ��ʾ��
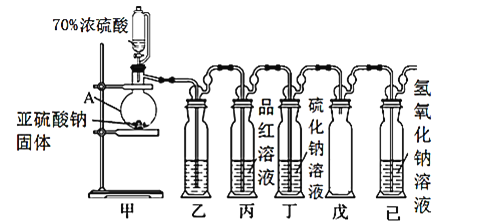
(1)����A������____________��
(2)װ���ҵ�������Ϊ�˹۲�����SO2�����ʣ���װ�����м�����Լ���____________��
(3)��ʵ��ǰ��ͬѧ������ɣ���װ��û���ſ������������е�O2������ǿ��SO2�����װ�ö��м�ʹ�л�������Ҳ����˵����SO2���µġ�����д��O2��Na2S��Һ��Ӧ�Ļ�ѧ��Ӧ����ʽ____________��
��Ϊ��һ������װ�ö��������������ԭ�����µ�ʵ��̽����ʵ����������������
��� | ʵ����� | ʵ������ |
1 | ��10 mL 1 mol/L Na2S��Һ��ͨO2 | 15 min����Һ�ų��ֻ��� |
2 | ��10 mL 1 mol/L Na2S��Һ��ͨSO2 | ��Һ�������ֻ�ɫ���� |
��ʵ�������֪����ʵ��������Na2S��Һ���ֻ���������SO2���µġ�����Ϊ�ϱ�ʵ��1��Ӧ������ԭ�������____________��
��.����ʯ����Ԫ�صIJⶨ����ʹ��ȼ�յ���������ԭ�����Ե���Ϊ���壬��ϡ���ᡢ���ۺ͵⻯�صĻ����ҺΪ����Һ����0.0010 mol��L-1KIO3����Һ���еζ������װ����ͼ��ʾ��
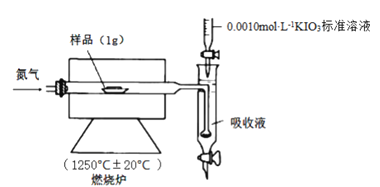
[��������] ��ʵ�����5min��Ʒ�е�SԪ�ض���ת��ΪSO2
��2IO3-+5SO2+4H2O=8H++5SO42-+I2
��I2+SO2+2H2O=2I-+SO42-+4H+
��IO3-+5I-+6H+=3I2+3H2O
(4)��ҵ�趨�ĵζ��յ�������____________��
(5)ʵ��һ��������Ʒ����ʵ�飬5 min�������ı�Һ���ΪV1
ʵ���������1 g��Ʒ�ٽ���ʵ�飬5 min�������ı�Һ���ΪV2
�ٱȽ����ݷ���V1ԶԶС��V2���ɺ��Բ��ơ�������ʵ��һ��Ŀ����___________��
�ڲ��V2����������
��� | 1 | 2 | 3 |
KIO3����Һ���/mL | 10.02 | 9.98 | 10.00 |
�÷�����ʯ��Ʒ����Ԫ�ص������ٷֺ���Ϊ____________��
���𰸡�������ƿ ����������������Һ O2+2H2O+2Na2S=4NaOH+2S�� ������ˮ�е��ܽ�ȱȶ�������С ����Һ�����ȶ�����ɫ �հ�ʵ�� 0.096%
��������
I.��װ��A����ȡSO2���壬ͨ���ҹ۲�SO2������������ʣ���Ʒ����Һ����SO2��Ư���ԣ���װ�ö���SO2��Na2S�ᷢ��������ԭ��Ӧ����S���ʣ�SO2����Ӧ������H2S�����ж����壬��NaOH��Һβ���������ų���
II.����IO3-�ܹ�����SO2ΪSO42-������I-ΪI2��SO2��Ӧ��ȫ���ٵ����IO3-��Һ��I2���ٷ�Ӧ����Һ�е�I2��������Һ��Ϊ��ɫ��Ҫ�ⶨ���ʺ�����Ӧ���ų����ʵĸ��ţ���ƶԱ�ʵ�飬Ϊ����ʵ���żȻ�ԣ�Ҫ���ж��ƽ��ʵ�飬ȡ���ʵ���ƽ��ֵ�����ݷ�Ӧ�����е����غ��������ʯ��Ʒ����Ԫ�ص�����������
(1)����ͼʾ�����ṹ��֪������A������Ϊ������ƿ��
(2)װ���ҵ�������Ϊ�˹۲�����SO2�����ʣ�Ϊ�˼���SO2��������Һ�е��ܽ⣬�ɸ���H2SO3�Ƕ�Ԫ���ᣬ����Һ�д��ڵ���ƽ������ʣ���װ�����м�����Լ�Ϊ����NaHSO3��Һ��
(3)��Na2S���л�ԭ�ԣ�O2���������ԣ�����Һ�лᷢ��������ԭ��Ӧ����S���ʺ�NaOH����Ӧ�Ļ�ѧ����ʽΪO2+2H2O+2Na2S=4NaOH+2S����
�ڸ���O2��SO2����ֱ�ͨ�뵽Na2S��Һ�в���S���ʵ�ʱ���֪�����ʵ������ԣ�SO2>O2����ʵ��������Na2S��Һ���ֻ���������SO2���µġ�����ʵ��1��Ӧ������ԭ�������O2������ˮ����SO2������ˮ������������ˮ�е��ܽ�ȱȶ�������С�����·�Ӧ���ʽ�����
II. (4)���ݷ���ʽ��֪���ʵ������ԣ�IO3->I2>SO2������SO2��KI�͵�����Һ�еμ�KIO3��Һ�����ȷ����ڷ�Ӧ����SO2��Ӧ��ȫ������Ӧ�ܣ���Ӧ������I2������������Һ���Ϊ��ɫ���Ұ��������Һ��ɫ����ȥ����֤���ζ��ﵽ�յ㣻
(5)��ͨ���Ƚ�ʵ��һ��ʵ��������ݣ�����V1ԶԶС��V2���ɺ��Բ���V1������ʵ��һ��Ŀ���ǿհԱ�ʵ�飬�ų��������صĴ��ڣ�
������ʵ������������Ч����ƽ������KIO3����Һ���V(KIO3)=![]() mL=10.00 mL��n(KIO3)=c��V=0.0010 mol/L��0.0100 L=1.0��10-5 mol�����ݵ����غ㼰��Ϣڢ۷���ʽ��֪n(SO2)=3n(KIO3)=3.0��10-5 mol������SԪ���غ��֪���к���SԪ�ص�����Ϊm(S)=n��M=3.0��10-5 mol��32 g/mol=9.6��10-4 g�����Ը÷�����ʯ��Ʒ����Ԫ�ص������ٷֺ���Ϊ
mL=10.00 mL��n(KIO3)=c��V=0.0010 mol/L��0.0100 L=1.0��10-5 mol�����ݵ����غ㼰��Ϣڢ۷���ʽ��֪n(SO2)=3n(KIO3)=3.0��10-5 mol������SԪ���غ��֪���к���SԪ�ص�����Ϊm(S)=n��M=3.0��10-5 mol��32 g/mol=9.6��10-4 g�����Ը÷�����ʯ��Ʒ����Ԫ�ص������ٷֺ���Ϊ![]() ��100%=0.096%��
��100%=0.096%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ����̼�Ͷ�����������;�㷺�Ļ�������ԭ�ϡ�
��1����֪��C��s����O2��g����CO2��g�� ��H1���C 393.5 kJ��mol �C 1
C��s����CO2��g����2CO��g�� ��H2����172.5 kJ��mol �C 1
S��s����O2��g����SO2��g�� ��H3���C 296.0 kJ��mol �C 1
��֪ij��Ӧ��ƽ�ⳣ��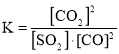 ����������Ϣ����д���÷�Ӧ���Ȼ�ѧ��Ӧ����ʽ��________________��
����������Ϣ����д���÷�Ӧ���Ȼ�ѧ��Ӧ����ʽ��________________��
��2����ҵ����һ����̼��ȡ�����ķ�ӦΪ��CO��g����H2O��g�� ![]() CO2��g����H2��g������֪420��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ9.0�������Ӧ��ʼʱ����2 L���ܱ������г���CO��H2O�����ʵ�������0.60 mol��5 minĩ�ﵽƽ�⣬���ʱCO��ת����Ϊ______��H2�Ļ�ѧ��Ӧ����Ϊ_____��
CO2��g����H2��g������֪420��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ9.0�������Ӧ��ʼʱ����2 L���ܱ������г���CO��H2O�����ʵ�������0.60 mol��5 minĩ�ﵽƽ�⣬���ʱCO��ת����Ϊ______��H2�Ļ�ѧ��Ӧ����Ϊ_____��
��3����ҵ���÷�Ӧ2SO2��g����O2��g�� ![]() 2SO3��g�������ᣬһ�������£���1molSO2��2molO2���ں����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬����______
2SO3��g�������ᣬһ�������£���1molSO2��2molO2���ں����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬����______
a ��ϵѹǿ���ֲ���
b ��������ܶȱ��ֲ���
c SO2��O2�����ʵ������ֲ���
d ÿ����1 mol SO3��ͬʱ������0.5 mol O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������پ��徧���Ľṹģ������ͼ��ʾ��ʵ���ý����ٵ��ܶ�Ϊ19.30![]() ��֪�ٵ����ԭ������Ϊ183.8���ش���������:
��֪�ٵ����ԭ������Ϊ183.8���ش���������:
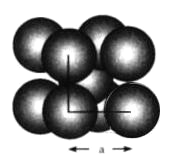
��1�����پ�����ÿ������ռ�е���ԭ����Ϊ__________����
��2���پ��徧���ı߳�Ϊ![]() __________
__________![]() ��
��
��3����ԭ�ӵİ뾶Ϊ__________![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ��X��Y��Z��W��Ϊ������Ԫ�أ���ԭ����������������֪Yԭ������������ռ�������������3/4��W����Z+��X+�����Ӱ뾶��С��������XW������Ϊ���壬Z�DZ������г�ϡ������Ԫ���⣬ԭ�Ӱ뾶����Ԫ�ء��ݴ˻ش��������⣺
��1��W��Ԫ�����ڱ��е�λ��___________________��ʵ������ȡW���ʵ����ӷ���ʽ��____________________________________________________________��
��2��A��B������������Ԫ���е�������ɵ�ǿ����ʣ�A��һ��ǿ�B��ij�ּ�������Һ����Ч�ɷ֣���A��B�Ļ�ѧʽ�ֱ�Ϊ___________��____________��
��3��C����Y��Z����Ԫ����ɵ�һ�ֻ��������Y��Z��ԭ�Ӹ�����Ϊ1��1����C�ĵ���ʽ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ��̼���������������ס���������Ԫ������ͭԪ���ڻ�ѧ���к���Ҫ�ĵ�λ���ش��������⣺
(1)�ڻ�̬14Cԭ����,�������___�������෴�ĵ��ӣ���̬��ԭ�ӵļ۲�����Ų�ͼΪ____��
(2)��F2ͨ��ϡNaOH��Һ�п�����OF2,OF2���ӹ���Ϊ__������ԭ�ӵ��ӻ���ʽΪ_______��
(3)CuSO4��Һ������P4�ж��Ľⶾ��,��Ӧ������P����ۺ������ͭ,�÷�Ӧ�Ļ�ѧ����ʽ��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������![]() ����
���� ����
���� �Ⱦ�Ϊ��Ҫ���л�����ԭ�ϡ�����˵����ȷ����
�Ⱦ�Ϊ��Ҫ���л�����ԭ�ϡ�����˵����ȷ����
A. �����ơ��Ż�Ϊͬϵ��B. �����ơ��ŵ�һ�ȴ���ֱ�Ϊ2��5��3��
C. �����ơ�����ֻ����������ˮD. �����ơ��ŵ�����ԭ�Ӳ����ܴ���ͬһƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���п�Ժ������ѧ�����о�����һ�����³ɹ�ʵ���˼����Ч������ϩ�������ڴ����������⣬�������о����ɻ�ż����Ӧ������ϩ����ͼ��ʾ��

��1���ִ�ʯ�ͻ�������Ag����������ʵ����ϩ�������Ʊ�X������ʽC2H4O������˫�������÷�Ӧ�����������ԭ�Ӿ��ã���Ӧ�Ļ�ѧ����ʽ��___���л�����д�ṹ��ʽ����
��2����֪������ʵ�ȼ�������ϱ���д�������Ʊ���ϩ���Ȼ�ѧ����ʽ___��
��3����400��ʱ�����ʼ���1L�ĺ�ѹ��Ӧ���г���1molCH4������������Ӧ�����ƽ����������C2H4���������Ϊ20.0%����
���ڸ��¶��£���ƽ�ⳣ��K=__��
�����������ͨ�����ˮ���������μӷ�Ӧ������400�棩��C2H4�IJ��ʽ�__��ѡ��������������С��������������ȷ��������������___��
������������̶�����ͬѹǿ�¿ɵñ仯��ͼ����ѹǿ�Ĺ�ϵ��___��

��ʵ���Ʊ�C2H4ʱ��ͨ�����ڸ���Ӧ��2CH4(g)��C2H6(g)��H2(g)����Ӧ����CH4��ʼ�����䣬��ͬ�¶���C2H6��C2H4������������¶ȵĹ�ϵ������ͼ��
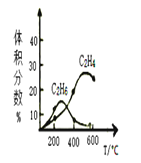
��200��ʱ����������������ϩ�����Ҫԭ�������___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����X��Y��Z���ֶ�����Ԫ�أ���֪Xԭ��L����ӱ�M����Ӷ�2���� Y3+���ӵ��Ӳ�ṹ��Ne��ͬ��Z��X����ͬһ���ڣ�����̬������˫ԭ�ӷ��ӣ���ԭ�ӹ��ã��Ե��ӡ��Իش�
��1��д��Ԫ��X������________ ��
��2��д��YԪ����Ԫ�����ڱ���λ��_______________ ;
��3������Ԫ��Z��ԭ�ӽṹʾ��ͼ��___________________ ��
��4��ZԪ�����������Ԫ���γɵĺ�����������ǿ���ǣ�д��ѧʽ��____________��
��5��X���⻯��ĵ���ʽΪ______________��
��6��д��Y����������������Һ��Ӧ��ѧ����ʽ_________________��
��7����״���£�2.24LZ��������������������ȫ��Ӧʱ������ת������Ϊ_____mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȼ��0.1 molij�л����0.2 mol CO2��0.3 mol H2O���ɴ˵ó��Ľ��۲���ȷ����(����)
A. ���л�����ӵĽṹ��ʽΪCH3��CH3
B. ���л�����̼����Ԫ��ԭ����Ŀ֮��Ϊ1��3
C. ���л�������в����ܺ���![]() ˫��
˫��
D. ���л�������п��ܺ�����ԭ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com