
【题目】以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
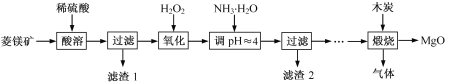
(1)MgCO3与稀硫酸反应的离子方程式为_______。
(2)加入H2O2氧化时,发生反应的化学方程式为_______。
(3)滤渣2 的成分是_______(填化学式)。
【答案】MgCO3+2H+=Mg2++CO2↑+H2O 2FeSO4+H2O2+H2SO4=Fe2(SO4)3+2H2O Fe(OH)3
【解析】
菱镁矿(主要成分为MgCO3,含少量FeCO3)和硫酸反应生成硫酸镁、硫酸亚铁,不溶性杂质过滤掉,再将亚铁离子氧化为铁离子,调节溶液的pH,将铁离子变为氢氧化亚铁,过滤得到硫酸镁,再得到硫酸镁,硫酸镁和木炭反应生成氧化镁。
以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:

⑴MgCO3与稀硫酸反应生成硫酸镁、水和二氧化碳气体,其离子方程式为MgCO3+2H+= Mg2++CO2↑+H2O,
故答案为:MgCO3+2H+ = Mg2++CO2↑+H2O;
⑵加入H2O2氧化时,主要是亚铁离子被双氧水氧化为铁离子,发生反应的化学方程式为2FeSO4+H2O2+H2SO4=Fe2(SO4)3+2H2O,
故答案为:2FeSO4+H2O2+H2SO4=Fe2(SO4)3+2H2O;
⑶滤渣2主要是由于调节pH值将铁离子变为Fe(OH)3,
故答案为:Fe(OH)3。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列关系图中,A 是一种正盐,B 是气态氢化物,C 是单质,F 是强酸。当 X 无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当 X 是强碱时,过量的 B 跟 Cl2 反应除生成 C 外,另一产物是盐酸盐。
下列说法中不正确的是( )
![]()
A.当 X 是强酸时,A、B、C、D、E、F中均含同一种元素,F 可能是 H2SO4
B.当 X 是强碱时,A、B、C、D、E、F中均含同一种元素,F 是 HNO3
C.用 O2 代替 Cl2, 也能与 B 反应生成 C 物质
D.当 X 是强酸时,C 在常温下是一种易溶于酒精的固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、X、Y、Z五种短周期元素,原子序数逐渐增大。它们的性质或原子结构如表:
元素 | 性质或原子结构 |
A | 原子核内只有一个质子 |
B | 单质是空气中含最多的气体 |
X | 原子的最外层电子数是次外层电子数的3倍 |
Y | 短周期元素中原子半径最大的元素(除稀有气体外) |
Z | 最高正化合价与最低负化合物的代数和为6 |
(1)X的元素名称及在元素周期表中的位置:___、___。
(2)B、X、Y的原子半径由大到小的顺序为(用元素符号表示)___。
(3)W元素的核电荷数是B、X的核电荷数的和,则W与Z的氢化物稳定性为___>___(填化学式)。
(4)A、X两元素形成的原子个数比为2:1的化合物属于___晶体,写出该晶体与Z元素形成的单质反应的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水钴矿中除SiO2外,还有9.24%CoO、2.78%Fe2O3、0.96%MgO、0.084%CaO。从中提取钴的主要工艺流程如下:
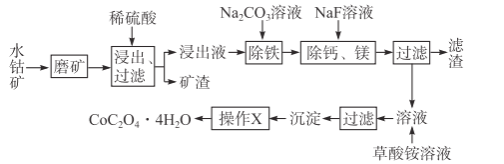
(1)浸出过程中,CoO溶解的离子反应方程式为___,矿渣的主要成分是___、___。
(2)请配平下列除铁的化学方程式:
_Fe2(SO4)3+_H2O+_Na2CO3=_Na2Fe6(SO4)4(OH)12↓+_Na2SO4+_CO2↑
(3)除钙、镁过程中,逐渐加入NaF溶液,当CaF2开始沉淀时,溶液中![]() =___。[已知Ksp(CaF2)=1.0×10-10、Ksp(MgF2)=7.4×10-11]。
=___。[已知Ksp(CaF2)=1.0×10-10、Ksp(MgF2)=7.4×10-11]。
(4)“操作X”是___。进行该操作的主要目的是除去沉淀中的杂质离子,检验杂质中的主要阴离子是否除净的试剂是___。
(5)100t水钴矿最多可获得___tCoC2O44H2O产品。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国制碱工业的先驱——侯德榜先生发明了著名的侯氏制碱法,其核心反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O→NH4Cl+NaHCO3(晶体)。依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和。

(1)A装置中所发生反应的离子方程式为___。C装置中稀硫酸的作用为___。
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
温度 溶解度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
参照表中数据,请分析B装置中使用冰水的目的是___。
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在___装置与___装置之间(填写字母)连接一个盛有___的洗气装置,其作用是___。
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解质溶液在电解质溶液在电解质储罐和电池间不断循环.下列说法不正确的是
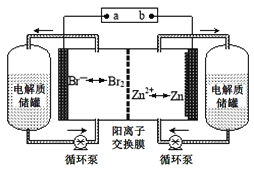
A.阳离子交换膜可阻止Br2与Zn直接发生反应
B.放电时正极的电极反应式为Br2+2e-=2Br-
C.充电时电极b连接电源的正极
D.放电时左侧电解质储罐中的离子总浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是25 ℃时某些盐的溶度积常数和弱酸的电离平衡常数,下列说法正确的是
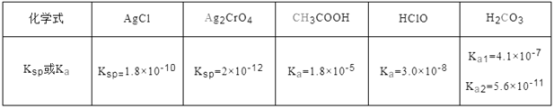
A. 相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
B. 碳酸钠溶液中滴加少量氯水的离子方程式H2O+2CO32-+Cl2===2HCO3-+Cl-+ClO-
C. 向0.1 mol·L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=9:5,此时溶液pH=5
D. 向浓度均为1×10-3mol·L-1的KCl和K2CrO4混合液中滴加1×10-3mol· L-1的AgNO3溶液,CrO42-先形成沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲苯(![]() )是一种重要的化工原料,能用于生产苯甲醛(
)是一种重要的化工原料,能用于生产苯甲醛(![]() )、苯甲酸(
)、苯甲酸(![]() )等产品。下表列出了有关物质的部分物理性质,请回答:
)等产品。下表列出了有关物质的部分物理性质,请回答:
名称 | 性状 | 熔点(℃) | 沸点(℃) | 相对密度(ρ水=1g·cm-3) | 溶解性 | |
水 | 乙醇 | |||||
甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8660 | 不溶 | 互溶 |
苯甲醛 | 无色液体 | -26 | 179 | 1.0440 | 微溶 | 互溶 |
苯甲酸 | 白色片状或针状晶体 | 122.1 | 249 | 1.2659 | 微溶 | 易溶 |
注:甲苯、苯甲醛、苯甲酸三者互溶。
实验室可用如图装置模拟制备苯甲醛。实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入15mL冰醋酸(作为溶剂)和2mL甲苯,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时。

(1)装置a的名称是___。
(2)三颈瓶中发生反应的化学方程式为___。
(3)写出苯甲醛与银氨溶液在一定的条件下发生反应的化学方程式:___。
(4)反应完毕后,反应混合液经过自然冷却至室温时,还应经过___、___(填操作名称)等操作,才能得到苯甲醛粗产品。
(5)实验中加入过量过氧化氢且反应时间较长,会使苯甲醛产品中产生较多的苯甲酸。若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是___(按步骤顺序填字母)。
a.对混合液进行分液
b.过滤、洗涤、干燥
c.水层中加入盐酸调节pH=2
d.加入适量碳酸氢钠溶液混合振荡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com