
【题目】(1)在反应A(g)+3B(g)=2C(g)中,若以物质A表示的该反应的化学反应速率为0.2 mol·L1·min1,则以物质B表示此反应的化学反应速率为________mol·L1·min1。
(2)在2 L的密闭容器中,充入2 mol N2和3 mol H2,在一定条件下发生反应,3 s后测得N2为1.9 mol,则以H2的浓度变化表示的反应速率为____________________________。
(3)将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g) ![]() 2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L1·s1,则在2 s时,容器中有______ mol A,此时C的物质的量浓度为________。
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L1·s1,则在2 s时,容器中有______ mol A,此时C的物质的量浓度为________。
【答案】 0.6 0.05 mol·L1·s1 8.8 0.08 mol·L1
【解析】(1)根据化学方程式中的计量数关系可知![]() =
=![]() ,v(B)=3v(A)=3×0.2 mol·L1·min1=0.6 mol·L1·min1。(2)3 s内消耗的N2的物质的量为2 mol1.9 mol=0.1 mol,根据化学方程式N2+3H2
,v(B)=3v(A)=3×0.2 mol·L1·min1=0.6 mol·L1·min1。(2)3 s内消耗的N2的物质的量为2 mol1.9 mol=0.1 mol,根据化学方程式N2+3H2![]() 2NH3,可以计算出3 s内消耗的H2的物质的量为0.3 mol,根据化学反应速率的计算公式可知v(H2)=
2NH3,可以计算出3 s内消耗的H2的物质的量为0.3 mol,根据化学反应速率的计算公式可知v(H2)= ![]() =0.05 mol·L1·s1。(3)在最初2 s内,消耗A的平均速率为0.06 mol·L1·s1,则消耗A的浓度是0.06 mol·L1·s1×2s=0.12mol/L,根据方程式可知
=0.05 mol·L1·s1。(3)在最初2 s内,消耗A的平均速率为0.06 mol·L1·s1,则消耗A的浓度是0.06 mol·L1·s1×2s=0.12mol/L,根据方程式可知
3A(g)+B(g)![]() 2C(g)
2C(g)
起始浓度(mol/L) 1 0.5 0
转化浓度(mol/L) 0.12 0.04 0.08
2s时浓度(mol/L)0.88 0.46 0.08
则在2 s时,容器中A的物质的量是0.88mol/L×10L=8.8mol,此时C的物质的量浓度为0.08molL。


科目:高中化学 来源: 题型:
【题目】有关图中化合物的说法错误的是( ) 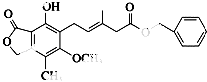
A.该化合物与Br2能发生加成反应和取代反应
B.1 mol该化合物与NaOH溶液反应时最多消耗3 mol NaOH
C.该化合物能使酸性高锰酸钾溶液褪色
D.该化合物能和Na2CO3溶液反应放出CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置,能完成很多电化学实验.下列有关此装置的叙述中,不正确的是( ) 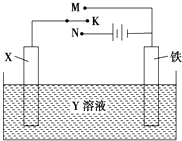
A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法
B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,这种方法称为外加电流阴极保护法
C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个体积均为2.0L的恒容密闭容器中发生如下反应:PCl5(g)PCl3(g)+Cl2(g)
编号 | 温度(℃) | 起始物质的量 | 平衡物质的量 | 达到平衡所需时间 | |
PCl5(g) | PCl3(g) | Cl2(g) | |||
Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t1 |
Ⅱ | 320 | 0.80 | t2 | ||
Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t3 |
下列说法正确的是( )
A.平衡常数K:容器Ⅱ>容器Ⅲ
B.反应到达平衡时,PCl5的转化率:容器Ⅱ<容器Ⅰ
C.反应到达平衡时,容器I中的平均速率为v(PCl5)= ![]() mol/(L?s)
mol/(L?s)
D.起始时向容器Ⅲ中充入PCl5 0.30 mol、PCl30.45 mol和Cl20.10 mol,则反应将向逆反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚和乙醇是同分异构体,其鉴别可采用化学方法及物理方法,下列鉴别方法中不能对二者进行鉴别的是( )
A.利用金属钠或者金属钾
B.利用质谱法
C.利用红外光谱法
D.利用核磁共振氢谱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各条件下可能共存的离子组是( )
A. 某无色溶液中: ![]() 、Na+、Cl-、
、Na+、Cl-、![]()
B. 由水电离出的c(H+)=1×10-13mol·L-1的溶液中:Na+、K+、![]() 、
、![]()
C. 在c(H+)=1×10-13 mol·L-1的溶液中: ![]() 、Al3+、
、Al3+、![]() 、
、![]()
D. 在pH=1的溶液中:K+、Fe2+、Cl-、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据电解质溶液的知识,回答下列问题:
已知0.1mol·L-1的NaHSO4溶液中H+的浓度为0.1mol·L-1,
(1)写出NaHSO4在水溶液中的电离方程式:________________________________________。
(2)若将NaHSO4与Ba(OH)2在溶液中按照物质的量之比1:1混合,离子方程式为_______________。
(3)若向Ba(OH)2溶液中滴加NaHSO4溶液至溶液恰好呈中性,反应的离子方程式为___。
(4)向NaAlO2中滴加NaHSO4溶液,现象为:________________;请你用离子方程式解释产生上述现象的原因______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾可用于生活消毒,是中学化学常见的氧化剂。工业上,用软锰矿( 主要成分MnO2)制高锰酸钾的流程如下(部分条件和产物省略):
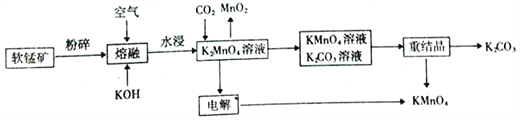
请回答下列问题:
(1)在“水浸”过程中,提高K2MnO4浸出率(浸出的K2MnO4质量与“熔块”质量之比)的措施有_______( 至少写出两点)。
(2)“熔融”过程中发生反应的化学方程式为___________。
(3)CO2 与K2MnO4反应的离子方程式为___________。
(4)“电解”过程中使用的是惰性电极,则:
①阳极反应的方程式为__________。
②阴极附近溶液的pH将__________。(填“增大”“减小” 或“ 不变”)。
(5)在上述过程中产生的Mn2+会对环境造成污染。工业上,通过调节pH使废水中的Mn2+形成Mn(OH)2 沉淀。当pH=10时,溶液中的c(Mn2+)=______(已知:Ksp[Mn(OH)2]=2.0×10-13。相关数据均在常温下测定)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com