
【题目】以铬铁矿[主要成分为Fe(CrO2)2],含有Al2O3、Fe2O3、SiO2等杂质为主要原料生产重铬酸钠晶体(Na2Cr2O7·2H2O)的主要工艺流程如下,关于该流程说法错误的是( )

A.煅烧生成Na2CrO4的化学方程式为:4Fe(CrO2)2+8Na2CO3+7O2![]() 2Fe2O3+8Na2CrO4 +8CO2
2Fe2O3+8Na2CrO4 +8CO2
B.SiO2在“浸出过滤”步骤中和Fe2O3一起除去
C.Na2CrO4到Na2Cr2O7转化的原理为:2H++2CrO42-![]() Cr2O72-+H2O
Cr2O72-+H2O
D.该工艺中“煅烧”产生的CO2可用于“除杂”步骤以节约生产成本,为完全除去AlO2-,发生的离子反应为:CO2+AlO2-+2H2O=Al(OH)3↓+HCO3-
科目:高中化学 来源: 题型:
【题目】如图所示为 A、B、C、D、E 五种含同一元素物质之间的相互转化关系。其中A、B、C、D 在常温下都是气体,且 B 为红棕色气体。
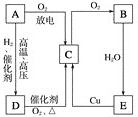
(1)①A、D、E三种物质中从相同元素化合价的角度分析既具有氧化性又具有还原性是(填化学式)____________;
②写出B的化学式:_______________, D的一种常见用途 _____________;
(2)按要求写出下列化学方程式或离子方程式
①写出 E 的稀溶液与 Cu 反应的离子方程式:_______________________;
②写出 D 的实验室制法的化学方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2是一种重要的清洁能源。
(1)已知:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH2=-49.0kJmol-1
CH3OH(g)+H2O(g) ΔH2=-49.0kJmol-1
CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH3=-41.1kJmol-1
CO2(g)+H2(g) ΔH3=-41.1kJmol-1
H2还原 CO反应合成甲醇的热化学方程式为:CO(g)+2H2(g)![]() CH3OH(g) ΔH1,则ΔH1=___kJmol-1,该反应自发进行的条件为___
CH3OH(g) ΔH1,则ΔH1=___kJmol-1,该反应自发进行的条件为___
A.高温 B.低温 C.任何温度条件下
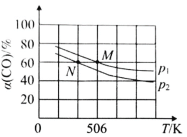
(2)恒温恒压下,在容积可变的密闭容器中加入 1molCO和2.2mol H2,发生反应CO(g)+2H2(g)![]() CH3OH(g),实验测得平衡时CO的转化率随温度、压强的变化如图所示。则P1__P2,判断的理由是_____。
CH3OH(g),实验测得平衡时CO的转化率随温度、压强的变化如图所示。则P1__P2,判断的理由是_____。
(3)若反应 CO(g)+2H2(g)![]() CH3OH(g)在温度不变且体积恒定为1的密闭容器中发生,反应过程中各物质的物质的量随时间变化如表所示:
CH3OH(g)在温度不变且体积恒定为1的密闭容器中发生,反应过程中各物质的物质的量随时间变化如表所示:
时间/min | 0 | 5 | 10 | 15 |
H2 | 4 | 2 | ||
CO | 2 | 1 | ||
CH3OH(g) | 0 | 0.7 |
①下列各项能作为判断该反应达到平衡标志的是____(填字母);
C.混合气体的相对分子质量保持不变 D.混合气体的密度保持不变
②若起始压强为P0 kPa,则在该温度下反应的平衡常数Kp=___(kPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③反应速率若用单位时间内分压的变化表示,则10min内H2的反应速率v(H2)=___kPamin-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置及操作均正确的是( )
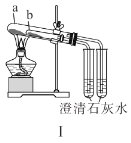

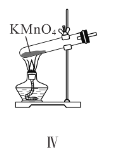
A.装置Ⅰ中![]() 盛放碳酸氢钠,
盛放碳酸氢钠,![]() 盛放碳酸钠,可对比二者的热稳定性
盛放碳酸钠,可对比二者的热稳定性
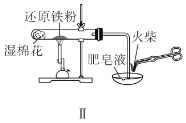
B.装置Ⅱ用于检验铁粉与水蒸气反应产生的氢气
C.装置Ⅲ用于制备氢氧化铁胶体
D.装置Ⅳ用于制备氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
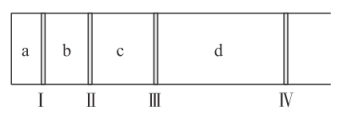
【题目】某温度下,向如图所示装置中分别通入等质量的![]() 四种气体(已知:密封隔板Ⅰ、Ⅱ、Ⅲ、Ⅳ可自由滑动,且与容器内壁摩擦不计),下列说法中正确的是( )
四种气体(已知:密封隔板Ⅰ、Ⅱ、Ⅲ、Ⅳ可自由滑动,且与容器内壁摩擦不计),下列说法中正确的是( )
A.![]() 中装的是
中装的是![]() B.
B.![]() 和
和![]() 中气体物质的量之比为
中气体物质的量之比为![]()
C.![]() 和
和![]() 中气体分子数相等D.
中气体分子数相等D.![]() 和
和![]() 中气体密度之比为
中气体密度之比为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组同学用下图装置测定氧化铁样品(含![]() 和
和![]() )中
)中![]() 的质量分数,下列说法正确的是( )
的质量分数,下列说法正确的是( )
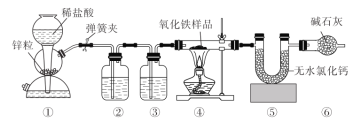
A.实验室用![]() 和浓盐酸制备
和浓盐酸制备![]() 时也可用装置①
时也可用装置①
B.实验开始时先点燃④处酒精灯,再打开弹簧夹
C.装置⑥的作用是吸收④中生成的水蒸气
D.装置②③盛装的试剂分别为![]() 溶液和浓硫酸
溶液和浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:①101kPa时,C(s)+1/2O2(g)=CO(g) △H1=-110.5kJ/mol②稀溶液中,H+(aq)+OH-(aq)=H2O(l) △H2=-57.3kJ/mol。下列结论中正确的是
A.若碳的燃烧热用△H3来表示,则△H3<△H1
B.若碳的燃烧热用△H3来表示,则△H3>△H1
C.稀硫酸与稀Ba(OH)2溶液反应生成2mol水,放出2×57.3kJ的热量
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前碘酸钾被广泛应用于食盐加碘。一种由含碘废水制取碘酸钾的工艺如下:
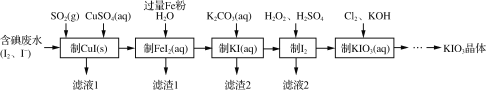
(1)检验“含碘废水”中是否含有单质I2,常用的试剂是______。
(2)通入SO2的目的是将I2还原为I-,该反应的离子方程式为________。
(3)滤渣1的成分为______。(写化学式)
(4)“制KIO3溶液”时,发生反应的离子方程式为___________。
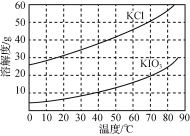
(5)KCl、KIO3的溶解度曲线如图所示。由上述流程中制得的KIO3溶液得到KIO3晶体的方法为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两同学为探究![]() 与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)。
与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)。
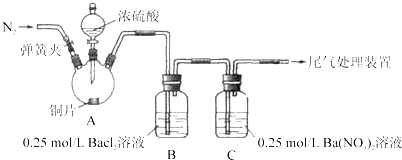
实验操作和现象:
操作 | 现象 |
关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡,B中有气泡冒出,产生大量白色沉淀,C中产生白色沉淀,液面上放略显浅棕色并逐渐消失 |
打开弹簧夹,通入N2,停止加热,一段时间后关闭 | |
从B、C中分别取少量白色沉淀,加稀盐酸 | 尚未发现白色沉淀溶解 |
(1)A中反应的化学方程式是_________________。
(2)C中白色沉淀是_______,该沉淀的生成表明SO2具有_______性。
(3)C中液面上方生成浅棕色气体的化学方程式是______。
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。
①未证实各自的观点,在原实验基础上:甲在原有操作之前增加一步操作,该操作是____;乙在A、B间增加洗气瓶D,D中盛放的试剂是______。
②进行实验,B中现象:
甲 | 大量白色沉淀 |
乙 | 少量白色沉淀 |
检验白色沉淀,发现均不溶于稀盐酸。结合离子方程式解释实验现象异同的原因:___。
(5)合并(4)中两同学的方案进行试验。B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com