
【题目】某小组为研究电化学原理,设计如图装置。下列叙述正确的是( )

A.a和b用导线连接时,铁电极上发生还原反应
B.a和b用导线连接时,电子经硫酸铜溶液从铁电极流向铜电极
C.无论a和b是否连接,铜电极质量都增加
D.无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色
【答案】D
【解析】
A.a和b用导线连接时,形成了原电池,Fe作负极,失去电子,发生氧化反应,A错误;
B.a和b用导线连接时,形成了原电池,Fe片作负极,失去电子,发生氧化反应,电子经导线流向Cu片,溶液中Cu2+在Cu片上得到电子发生还原反应,B错误;
C.a和b不连接时,铁片和硫酸铜溶液直接发生化学反应,铁将金属铜从其盐中置换出来,产生的Cu在铁片上附着,使铁片质量增加,而铜电极质量不变;当a和b用导线连接时,形成了原电池,溶液中Cu2+在Cu片上得到电子发生还原反应,产生Cu单质在Cu片上附着,使铜电极质量增加,可见Cu电极质量不一定都增加,C错误;
D.a和b不连接时,铁片和硫酸铜溶液之间发生化学反应,铁能将金属铜从其盐中置换出来,Fe变为Fe2+进入溶液;当a和b用导线连接时,形成了原电池,加快了铁将金属铜从其盐中置换出来的速度,Fe为负极,失去电子被氧化变为Fe2+进入溶液。可见无论a和b是否连接,铁片均会溶解生成+2价的Fe2+,导致溶液均从蓝色逐渐变成浅绿色,D正确;
故合理选项是D。


科目:高中化学 来源: 题型:
【题目】一种“全氢电池”的工作原理如图所示。下列说法不正确的是
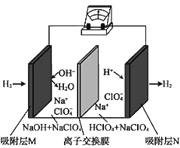
A.电子流向是从吸附层M通过导线到吸附层N
B.电池工作时,负极区pH减小
C.离子交换膜可用质子交换膜
D.负极的电极反应是:H2-2e-+2OH-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学实验室常用如图所示装置制取少量溴苯,请回答下列问题。
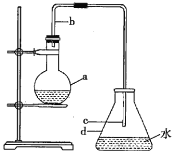
(1)烧瓶a中盛装的试剂是苯、液溴和铁屑。导管b的作用有两个:一是导气,二是起________的作用。
(2)反应过程中在导管c的下口附近可以观察到有白雾出现,这是由于反应生成的________(填化学式)遇水蒸气而形成的。
(3)反应完毕后,向锥形瓶d中滴入![]() 溶液,有________生成。
溶液,有________生成。
(4)反应完毕后,将烧瓶a中的液体倒入盛有冷水的烧杯中,可以观察到烧杯底部有棕色不溶于水的液体。这是溶解了溴的粗溴苯,可选用试剂________________除去溴。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过碳酸钠![]() 常作除污剂、清洗剂和杀菌剂。市售过碳酸钠样品一般含有碳酸钠,为了测定某过碳酸钠样品
常作除污剂、清洗剂和杀菌剂。市售过碳酸钠样品一般含有碳酸钠,为了测定某过碳酸钠样品![]() 只含
只含![]() 和
和![]() 的纯度,某小组设计如下两种实验方案:
的纯度,某小组设计如下两种实验方案:
实验原理:![]() 也可以用盐酸与过碳酸钠反应
也可以用盐酸与过碳酸钠反应![]() 。
。
方案1:液吸法。取![]() 样品于烧瓶中,加入足量的稀硫酸,实验装置如图所示。已知:在分析化学中,常用醋酸亚铬
样品于烧瓶中,加入足量的稀硫酸,实验装置如图所示。已知:在分析化学中,常用醋酸亚铬![]() 溶液作
溶液作![]() 的吸收剂。
的吸收剂。
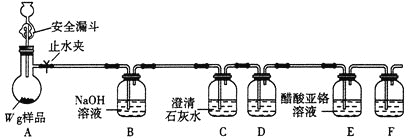
⑴安全漏斗中“安全”的含义是____________________________。
⑵装置C的作用是__________;装置D和F盛放同一种试剂,可能是________(填名称)。
⑶本实验通过装置________________(填字母)实验前后质量差可测定![]() 的质量。
的质量。
⑷实验装置气密性良好及装置内试剂足量,但实验发现测定的样品纯度总是偏低,其主要原因可能是________________________。
方案2:量气法。实验装置如图所示。
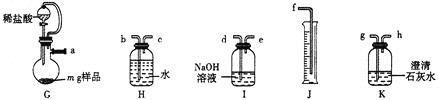
⑸气流方向由左至右,则导管口连接顺序为![]() ________
________![]() 。
。
⑹实验时向烧瓶内加入足量稀盐酸,实验完毕后,在室温下,测得J中水的体积为![]() 。已知室温下,气体摩尔体积为
。已知室温下,气体摩尔体积为![]() 。该样品纯度为__________%(用含x、y、m的代数式表示)。若其他操作都合理,读数时J中液面高于H中液面,则测得结果________(填“偏高”“偏低”或“无影响”)。
。该样品纯度为__________%(用含x、y、m的代数式表示)。若其他操作都合理,读数时J中液面高于H中液面,则测得结果________(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列营养物质在人体内发生的变化及其对人的生命活动所起的作用叙述不正确的是
A.淀粉![]() 葡萄糖
葡萄糖![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
B.纤维素![]() 葡萄糖
葡萄糖![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
C.油脂![]() 甘油和高级脂肪酸
甘油和高级脂肪酸![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
D.蛋白质![]() 氨基酸
氨基酸![]() 人体所需的蛋白质(人体生长发育)
人体所需的蛋白质(人体生长发育)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以淀粉为基本原料可制备许多物质,如:
![]()
下列有关说法正确的是( )。
A.淀粉与纤维素互为同分异构体
B.反应⑤是取代反应
C.反应①是氧化反应
D.在加热条件下,可用银氨溶液鉴别葡萄糖和乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易反应,生成一种氯化物和两种氧化物。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如下图所示:
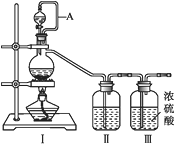
为制备纯净干燥的气体,下表中缺少的药品是:
装置Ⅰ | 装置Ⅱ | ||
烧瓶中 | 分液漏斗中 | ||
制备纯净Cl2 | MnO2 | ① | ② |
制备纯净NO | Cu | ③ | ④ |
②___________,③___________。
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:

①装置连接顺序为a→___________________(按气流自左向右方向,用小写字母表示)。
②装置Ⅶ的作用为________________,若无该装置,Ⅸ中NOCl可能发生反应的化学方程式为_______________________________。
③乙组同学认为氢氧化钠溶液只能吸收氯气和NOCl,不能吸收NO,所以装置Ⅷ不能有效除去有毒气体。为解决这一问题,可将尾气与某种气体同时通入氢氧化钠溶液中,这种气体的化学式是__________。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为___________________。
(4)丁组同学用以下方法测定亚硝酰氯(NOCl)纯度
取Ⅸ中所得液体mg溶于水,配制成250mL溶液;取出25.00mL,以K2CrO4溶液为指示剂,用c mol/LAgNO3 标准溶液滴定至终点,消耗标准溶液的体积为b mL。(已知:Ag2CrO4为砖红色固体)
①亚硝酰氯(NOCl)的质量分数为_________(用代数式表示即可)。
②若滴定前,滴定管尖嘴有气泡,滴定后气泡消失,则所测亚硝酰氯的纯度_________(偏高、偏低、无影响)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以煤为原料可合成一系列燃料。
(1)已知:①2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol,
②CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ/mol
请写出甲醇燃烧生成H2O(g)的热化学方程式_________;
(2)向1 L密闭容器中加入2 mol CO、4 mol H2,在适当的催化剂作用下,发生反应:2CO(g)+4H2(g)CH3OCH3(l)+H2O(l) ΔH=+71 kJ/mol
①该反应能否_________自发进行(填“能”、“不能”或“无法判断”)
②下列叙述能说明此反应达到平衡状态的是_________.
a.混合气体的平均相对分子质量保持不变 b.CO和H2的转化率相等
c.CO和H2的体积分数保持不变 d.混合气体的密度保持不变
e.1 mol CO生成的同时有1 mol O-H键断裂
(3)CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH<0在一定条件下,某反应过程中部分数据如下表:
反应条件 | 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) |
恒温恒容 (T1℃、2L) | 0min | 2 | 6 | 0 | 0 |
10min | 4.5 | ||||
20min | 1 | ||||
30min | 1 |
①0~10 min内,用H2O(g)表示的化学反应速率v(H2O)=_________mol/(L·min);
span>②达到平衡时,该反应的平衡常数K=_________(用分数表示),平衡时H2的转化率是_________;
③在其他条件不变的情况下,若30 min时向容器中再充入1 mol CO2(g)和1 mol H2O(g),则平衡_______移动(填“正向”、“逆向”或“不”);
(4)用甲醚(CH3OCH3)作为燃料电池的原料,请写出在碱性介质中电池负极反应式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
(1)某小组设计了如下图所示的实验装置用于制备ClO2。
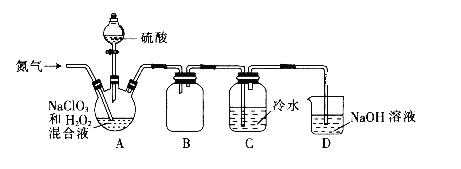
①通入氮气的主要作用有2个,一是可以起到搅拌作用,二是__________。
②装置B的作用是_________。
③当看到装置C中导管液面上升时应进行的操作是________。
(2)用0.1000mol·L-1的Na2S2O3标准液测定装置C中ClO2溶液的浓度。原理:2ClO2+10I-+8H+=5I2+2Cl-+4H2O , I2+2S2O32- = 2I- +S4O62-
①配制0.1000molL-1的Na2S2O3标准溶液时所需仪器除在如图所示的仪器中进行选择外,还需用到的玻璃仪器是________(填仪器名称)
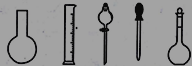
②在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度___0.1000molL-1(填“>”、“<”或“=”,下同);若Na2S2O3标准溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度___0.1000molL-1。
③取10mLC中溶液于锥形瓶中,加入足量的KI溶液和H2SO4酸化,然后加入___________作指示剂,测得标准液消耗的体积为20.00mL,通过计算可知C中ClO2溶液的浓度为________ mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com