
【题目】铁在化合物中通常是Fe(Ⅱ)、Fe(Ⅲ),现有一定量固体物质A,可能由FeSO4、Fe2(SO4)3组成,通过实验确定其成分。探究过程如下:
(1)提出假设:(请把下列假设补充完整)
假设:该固体物质是FeSO4;或该固体物质是Fe2(SO4)3;或该固体物质是___。
(2)设计实验方案:取少量固体物质A于烧杯中,加适量水溶解A,然后取两份A溶液分别进行实验,实验现象与结论如表:
实验方法 | 实验现象 | 结论 |
在溶液中加入KSCN溶液 | ___ | 固体物质中有Fe2(SO4)3 |
在酸性KMnO4溶液中加入少量A振荡 | KMnO4溶液颜色无明显变化 | 固体物质中不含___。 |
(3)若该固体A可能还存在铁,则不能证明固体物质中含___,其理由至少有两个,请分别用离子方程式表示___、___。
(4)![]() ,写出由“白色沉淀”转化为“红褐色沉淀”的化学方程式___。
,写出由“白色沉淀”转化为“红褐色沉淀”的化学方程式___。
(5)上述白色沉淀在空气中迅速变成灰绿色,最后变成红褐色,由此得出Fe(Ⅱ)的还原性强弱与___有关,FeSO4的还原性___Fe(OH)2(填“大于”“小于”或“等于”)。
【答案】FeSO4和Fe2(SO4)3 溶液变血红色(或红色) FeSO4 FeSO4 Fe +2Fe3+=3Fe2+ 5Fe+3MnO4-+24H+=3Mn2+ +5Fe3++12H2O 4Fe(OH)2 +O2+2H2O=4Fe(OH)3 溶液酸碱性或pH 小于
【解析】
(1)根据类比法,结合铁和硫酸反应的产物,产物可能为FeSO4、Fe2(SO4)3或二者的混合物;
(2)固体物质中有Fe2(SO4)3,在溶液中加入KSCN溶液,溶液应变红;在酸性KMnO4溶液中加入少量A,KMnO4溶液颜色无明显变化,说明不含还原性物质;
(3)铁具有较强的还原性,能够与铁离子或高锰酸钾反应,据此分析判断;
(4)硫酸亚铁溶液与氨水反应生成氢氧化亚铁沉淀,氢氧化亚铁容易被空气中的氧气氧化生成氢氧化铁,据此书写反应的方程式;
(5)硫酸亚铁溶液可以在空气中较长时间的存在,而氢氧化亚铁在空气中很快被氧化,据此分析解答。
(1)根据类比法,结合铁和硝酸反应的产物,产物可能为FeSO4、Fe2(SO4)3或FeSO4和Fe2(SO4)3的混合物,故答案为:FeSO4和Fe2(SO4)3;
(2)固体物质中有Fe2(SO4)3,在溶液中加入KSCN溶液,溶液应变红,在酸性KMnO4溶液中加入少量A,KMnO4溶液颜色无明显变化,说明固体A中不含还原性物质,即不含FeSO4,故答案为:溶液变血红色;FeSO4;
(3)若固体A还存在铁,由于Fe +2Fe3+=3Fe2+,或者5Fe+3MnO4-+24H+=3Mn2+ +5Fe3++12H2O,因此不能通过高锰酸钾是否褪色来证明固体物质含FeSO4,故答案为:FeSO4;Fe +2Fe3+=3Fe2+;5Fe+3MnO4-+24H+=3Mn2+ +5Fe3++12H2O;
(4)硫酸亚铁溶液与氨水反应生成氢氧化亚铁沉淀,氢氧化亚铁容易被空气中的氧气氧化生成氢氧化铁,因此白色沉淀转化为红褐色沉淀的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为: 4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(5)硫酸亚铁溶液可以在空气中较长时间的存在,而氢氧化亚铁白色沉淀在空气中迅速变成灰绿色,最后变成红褐色,由此得出Fe(Ⅱ)的还原性强弱与溶液酸碱性或pH有关,FeSO4的还原性<Fe(OH)2的还原性,故答案为:溶液酸碱性或pH;小于。


科目:高中化学 来源: 题型:
【题目】在一定温度下,可逆反应:A2(g)+B2(g)![]() 2AB(g),达到平衡的标志是( )
2AB(g),达到平衡的标志是( )
A.容器的总压强不随时间而变化
B.单位时间内生成nmolA2同时就有2nmolAB生成
C.单位时间内有nmolB2发生反应的同时有nmolAB分解
D.单位时间内有nmolA2生成的同时有nmolB2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国Lawrece Liermore国家实验室(LINL)成功地在高压下将![]() 转化为具有类似
转化为具有类似![]() 结构的原子晶体,下列关于
结构的原子晶体,下列关于![]() 的原子晶体说法,正确的是:
的原子晶体说法,正确的是:
A. ![]() 的原子晶体和分子晶体互为同分异构体
的原子晶体和分子晶体互为同分异构体
B. 在一定条件下,![]() 原子晶体转化为
原子晶体转化为![]() 分子晶体是物理变化
分子晶体是物理变化
C. ![]() 的原子晶体和
的原子晶体和![]() 分子晶体具有相同的物理性质和化学性质
分子晶体具有相同的物理性质和化学性质
D. 在![]() 的原子晶体中,每一个C原子周围结合4个O原子,每一个O原子跟两个C原子相结合
的原子晶体中,每一个C原子周围结合4个O原子,每一个O原子跟两个C原子相结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肉桂酸(![]() )常用于制取香精香料。
)常用于制取香精香料。
(1)肉桂酸的分子式是____,肉桂酸____(填“属于”或“不属于”)烃类。
(2)肉桂酸能使溴的四氯化碳溶液褪色,因为结构中含____(填官能团名称)。
(3)向肉桂酸溶液中滴加NaHCO3溶液,实验现象为____。
(4)写出肉桂酸与乙醇发生酯化反应的化学方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组进行了有关Cu、硝酸、硫酸化学性质的实验,实验过程如下图所示。下列有关说法正确的是
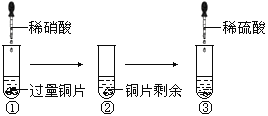
A. 实验①中溶液呈蓝色,试管口有红棕色气体产生,说明稀硝酸被Cu还原为NO2
B. 实验③中滴加稀硫酸,铜片继续溶解,说明稀硫酸的氧化性比稀硝酸强
C. 实验③发生反应的化学方程式为:3Cu+Cu(NO3)2+4H2SO4=4CuSO4+2NO↑+4H2O
D. 由上述实验可得出结论:Cu在常温下既可以和稀硝酸反应,也可以和稀硫酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用如图所示装置进行有关实验:

(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请在图上把导管补充完整_________。
(2)实验中他们取6.4 g铜片和12 mL 18 mol·L1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①写出铜跟浓硫酸反应的化学方程式:__________________;
②为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是__________________;
③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是________(填编号)。
A.铁粉 B.BaCl2溶液 C.银粉 D.Na2CO3溶液
(3)装置C中试管D内盛装的是品红溶液,当B中气体收集满后,有可能观察到的现象是_____________,待反应结束后,向C中烧杯内加入沸水,D中观察到的现象是_____________。
(4)实验装置C有可能造成环境污染,试用最简单的方法加以解决,__________________(实验用品自选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲测定金属镁的相对原子质量,请利用下图给定的仪器组成一套实验装置(每个仪器只能使用一次,假设气体的体积可看作标准状况下的体积)。

填写下列各项(气流从左到右):
(1)各种仪器连接的先后顺序是__________接________、________接________、________接________、________接________(用小写字母表示)。
(2)连接好仪器后,要进行的操作有以下几步,其先后顺序是________________(填序号)。
①待仪器B中的温度恢复至室温时,测得量筒C中水的体积为Va mL;
②擦掉镁条表面的氧化膜,将其置于天平上称量,得质量为m g,并将其投入试管B中的带孔隔板上;
③检查装置的气密性;
④旋开装置A上分液漏斗的活塞,使其水顺利流下,当镁完全溶解时再关闭这个活塞,这时A中共放入水Vb mL。
(3)根据实验数据可算出金属镁的相对原子质量,其数学表达式为___________________。
(4)若试管B的温度未冷却至室温,就读出量筒C中水的体积,这将会使所测定镁的相对原子质量数据________(填“偏大”“偏小”或“无影响”)。
(5)仔细分析上述实验装置后,经讨论认为结果会有误差,于是又设计了如下图所示的实验装置。

①装置中导管a的作用是_________________________________________。
②实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL。则产生氢气的体积为____________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠硫电池体积小、容量大、寿命长、效率高,在电力储能中广泛应用于削峰填谷、应急电源、风力发电等储能方面。Na-S电池的结构如下图所示,电池反应为2Na+![]() S8=Na2Sn。下列说法不正确的是( )
S8=Na2Sn。下列说法不正确的是( )
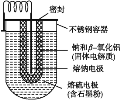
A. 熔钠电极作电池的负极B. 放电时Na+向正极移动
C. 充电时熔钠电极与电源的正极相连D. 充电时阳极反应式为8Sn2--16e-=nS8
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com