
【题目】将镁条置于 pH=8.4 的饱和 NaHCO3 溶液中,镁条表面产生气体 a,一段时间后产生白色沉淀b。继续进行如下实验:
Ⅰ.将 a 通过澄清石灰水,变浑浊,继而通过足量 NaOH 溶液,再通入肥皂液,出现气泡,点燃气泡听到爆鸣声;
Ⅱ.向沉淀 b 中加入足量的稀盐酸,沉淀完全溶解,且产生无色气泡。下列说法不正确的是
A.饱和 NaHCO3 溶液中,c(![]() )< c(H2CO3)
)< c(H2CO3)
B.沉淀 b 是 MgCO3
C.气体 a 中含有 CO2 和 H2
D.CO2 可能是 ![]() 水解被促进产生的
水解被促进产生的
【答案】B
【解析】
饱和NaHCO3溶液的pH=8.4,说明在溶液中以![]() 水解为主。实验Ⅰ,将 a通过澄清石灰水,变浑浊,表明a中含有CO2,继而通过足量 NaOH 溶液除去CO2,再通入肥皂液,出现气泡,点燃气泡听到爆鸣声,表明a中含有H2;实验Ⅱ,向沉淀 b 中加入足量的稀盐酸,沉淀完全溶解,且产生无色气泡,表明b中一定含有MgCO3,可能含有Mg(OH)2。
水解为主。实验Ⅰ,将 a通过澄清石灰水,变浑浊,表明a中含有CO2,继而通过足量 NaOH 溶液除去CO2,再通入肥皂液,出现气泡,点燃气泡听到爆鸣声,表明a中含有H2;实验Ⅱ,向沉淀 b 中加入足量的稀盐酸,沉淀完全溶解,且产生无色气泡,表明b中一定含有MgCO3,可能含有Mg(OH)2。
A.饱和NaHCO3溶液呈碱性,表明![]() 的水解趋势大于电离趋势,所以c(
的水解趋势大于电离趋势,所以c(![]() )< c(H2CO3),A正确;
)< c(H2CO3),A正确;
B.由于Mg(OH)2比MgCO3更难溶,沉淀趋向于向生成Mg(OH)2的方向转化,但沉淀与盐酸反应有气泡产生,所以沉淀 b 应为MgCO3与Mg(OH)2的混合物,B错误;
C.由以上分析知,气体 a 中含有CO2(使澄清石灰水变浑浊) 和H2(点燃气泡听到爆鸣声),C正确;
D.CO2可能是 ![]() 水解生成的H2CO3发生分解生成,所以
水解生成的H2CO3发生分解生成,所以![]() 水解被促进,D正确;
水解被促进,D正确;
故选B。


科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.石油裂化可以提高汽油等轻质油的产量和质量
B.分子式为C5H12的同分异构体共有3种
C.向2mL碘水中加入1mL苯,振荡后静置,可观察到液体分层,上层呈紫红色
D.煤中含有苯和甲苯,可用干馏的方法将它们分离开来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得推论正确的是
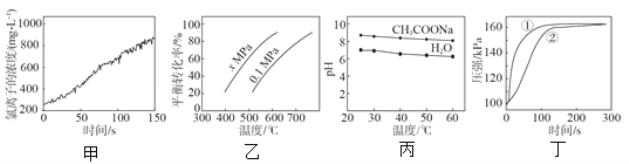
A.甲是新制氯水光照过程中氯离子浓度的变化曲线,推断次氯酸分解生成了 HCl 和 O2
B.乙是 C4H10(g)![]() C4H8(g) + H2(g)的平衡转化率与温度和压强的关系曲线,推断该反应的H>0、x>0.1
C4H8(g) + H2(g)的平衡转化率与温度和压强的关系曲线,推断该反应的H>0、x>0.1
C.丁是 0.03g 镁条分别与 2 mL 2 mol/L 盐酸和醋酸反应过程中密闭容器内气体压强随时间的变化曲线,推断①代表盐酸与镁条的反应
D.丙是 0.5 mol/L CH3COONa 溶液及水的 pH 随温度的变化曲线,说明随温度升高,CH3COONa 溶液中 c(OH-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸滴定碱时,滴定前读酸式滴定管读数时视线低于水平线,滴定结束时读数正确,这样会使测得的碱溶液的浓度
A.偏高B.偏低C.不受影响D.不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7:17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是( )
A.气态氢化物的稳定性:X﹥W
B.金属性:Y﹥Z
C.最高价含氧酸的酸性:X﹥W
D.原子半径:Y﹥Z﹥X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.10 mol/L的氨水滴定10.0 mLa mol/L的盐酸,溶液的pH与氨水体积(V)的关系如图所示。已知:N点溶液中存在:c(Cl-)=c(NH4+)+c(NH3·H2O)。下列说法不正确的是( )
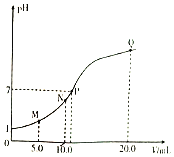
A.a=0.10
B.N、P两点溶液中水的电离程度:N<P
C.M、N两点溶液中NH4+的物质的量之比大于1:2
D.Q点溶液中存在:2c(OH-)-2c(H+)=c(NH4+)-c(NH3·H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)海水资源的利用具有广阔前景。海水中主要离子的含量如下:
成分 | 含量/(mg/L) | 成分 | 含量/(mg/L) |
Cl- | 18980 | Ca2+ | 400 |
Na+ | 10560 |
| 142 |
| 2560 | Br- | 64 |
Mg2+ | 1272 |
电渗析法淡化海水示意图如图所示,其中阴(阳) 离子交换膜仅允许阴(阳)离子通过。
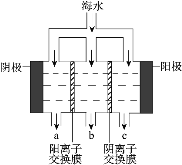
①电解氯化钠溶液的离子方程式_____。
②电解过程中阴极区碱性明显增强,用平衡移动原理 解释原因_____。 在阴极附近产生少量白色沉淀,其成分有_________和CaCO3。
③淡水的出口为_________(填“a”、“b”或“c”);a 出口物质为_____(填化学式)。
④若用下面燃料电池为电源电解 100mL1molL-1 氯化钠溶液,当电池消耗0.00025 molO2 时,常温下,所得溶液的 pH 为__________(忽略反应前后溶液体积变化)
(2)如图Ⅰ是氢氧燃料电池(电解质为 KOH 溶液)的结构示意图,
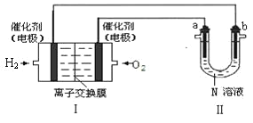
①Ⅰ中通入O2的一端为电池的_____极。 通入H2的一端的电极反应式_________
②若在Ⅱ中实现锌片上镀铜,则 b 的电极材料是_____,N 溶液为_____溶液。
③若在Ⅱ中实现 Cu+H2SO4= CuSO4+H2↑,则a 极的反应式是_____,N 溶液为 _____溶液。
(3)工业上用 Na2SO3 溶液吸收 SO2,过程中往往得到 Na2SO3 和 NaHSO3的混合溶液,溶液 pH 随 n(![]() ):n(
):n(![]() ) 变化关系如下表:
) 变化关系如下表:
n( | 91:9 | 1:1 | 9:91 |
pH | 8.2 | 7.2 | 6.2 |
当吸收液的 pH 降至约为 6 时,送至电解槽再生。再生示意图如下,结合图示回答:

①![]() 在阳极放电的电极反应式是_____。
在阳极放电的电极反应式是_____。
②当阴极室中溶液 pH升至 8 以上时,吸收液再生并循环利用。简述再生原理:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属腐蚀与防护的说法中正确的是( )
A.牺牲阳极的阴极保护法是一种基于电解池原理的金属防护法
B.钢铁的析氢腐蚀和吸氧腐蚀的负极反应式相同
C.镀锌铁制品镀层受损后形成原电池,锌作负极,比破损前更耐腐蚀
D.将变黑后的银器(表面被氧化为Ag2S)放入盛有食盐溶液的铝质容器中,黑色褪去是因为生成了AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质a、b、c、d均为中学化学中的常见单质或化合物,它们之间的转化关系如右图所示(部分产物已略去),下列各组物质中,通过一步反应就能实现图示转化的是
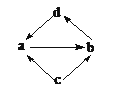
选项 | a | b | c | d |
A | SO2 | SO3 | S | H2SO4 |
B | Na2O | Na2O2 | Na | NaOH |
C | CO | CO2 | C | H2CO3 |
D | Al2O3 | NaAlO2 | Al | Al(OH)3 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com