
下列叙述正确的是( )
①热稳定性:H2O>HF>H2S
②熔点:Al>Na>K
③第ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤沸点:NH3 > PH3> AsH3
⑥已知2H2(g)+O2(g)=2H2O(l) ΔH=-571kJ·mol-1 ,则氢气的燃烧热为285.5kJ·mol-1
⑦因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,所以非金属性:P>N
A.只有②④⑥ B.只有①⑤⑥ C.只有②④⑥⑦ D.只有③⑤⑦
A
解析试题分析:①因非金属性F>O>S,则氢化物的稳定性为HF>H2O>H2S,故①错误;②因铝的半径最小,电荷最高,则熔点最高,Na与K电荷相同,但Na的半径小,则Na的熔点比K的高,即熔点为Al>Na>K,故②正确;③因IA、IIA族元素的阳离子的电子层数比原子的结构减少一个层,则IA、IIA族元素的阳离子与上一周期稀有气体元素的原子具有相同的核外电子排布,故③错误;④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素,故④正确;⑤同一主族的元素的氢化物,若为HF、H2O、NH3,由于氢键的存在,它们的沸点反常的高,无氢键的物质分子量大的沸点高故⑤错误;⑥由热化学反应方程式可知,2mol氢气燃烧生成稳定化合物放出的热量为571.6kJ,则1mol氢气燃烧放出的热量为285.8kJ,即氢气的燃烧热为285.8kJ?mol-1,故⑥正确;⑦因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,可知白磷的易被氧化,但由同主族从上到下元素的非金属性减弱可知,非金属性N>P,故⑦错误。
考点:非金属在元素周期表中的位置及其性质递变的规律;元素周期表的结构及其应用;燃烧热 。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:单选题
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D是地壳中含量最多的金属元素。下列说法正确的是
A.1 mol 由元素A、B组成的化合物一定含有18 mol e-
B.元素C、D的最高价氧化物对应的水化物之间不可能发生反应
C.含D的盐溶液既可能显酸性,也可能显碱性
D.化合物AE与CE含有相同类型的化学键
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
四种短周期元素在周期表中的位置如右图,其中只有M为金属元素。下列说法不正确的是
| A.原子半径Z<M |
| B.Y的最高价氧化物对应水化物的酸性比X 的弱 |
| C.X 的最简单气态氢化物的热稳定性比Z的小 |
| D.Z位于元索周期表中第2 周期、第ⅥA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确的是( )
| A.由mXa+与nYb-,得m+a=n-b |
| B.X2-的还原性一定大于Y- |
| C.X,Y一定不是同周期元素 |
| D.若X的原子半径大于Y,则气态氢化物的稳定性HmX一定大于HnY |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.HF、HCl、HBr、HI的热稳定性依次减弱,沸点却依次升高 |
| B.熔融状态下能导电的化合物一定含离子键;金属与非金属元素形成的化合物一定是离子化合物 |
| C.NCl3分子中所有的原子均为8电子稳定结构 |
| D.NaHSO4晶体中阴、阳离子的个数是1:2且熔化时破坏的是离子键和共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z、M、R在周期表中的相对位置如图所示。下列说法正确的是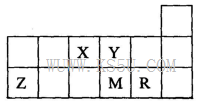
| A.元素X和M的氧化物对应的水化物均为强酸 |
| B.R的单质能与M的氢化物发生置换反应 |
| C.气态氢化物的稳定性:M>Y |
| D.元素Y、Z形成的简单离子半径大小关系为:Z>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z,其中X、Y位于同一主族,Y、Z位于同一周期。X原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比Y原子少1。下列比较正确的是
| A.元素非金属性:Z> Y > X | B.最高价氧化物水化物酸性:Z > Y |
| C.原子半径:Z < Y < X | D.气态氢化物的稳定性:Z < Y < X |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z、W、M五种元素的原子序数依次增大,且X、Y、Z、W均为短周期中的非金属元素,X元素的原子形成的阴离子核外排布与氦原子相同,Z、W在周期表中处于相邻位置,它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍,M是地壳中含量最高的金属元素。下列说法正确的是( )
| A.五种元素的原子半径从大到小的顺序是:M> W> Z>Y>X |
| B.化合物X2W2、YW2、ZW2都含有极性共价键和非极性共价键 |
| C.工业上通常用电解熔融的MCl3来冶炼金属M |
| D.Z、X两元素能形成原子个数比为1∶3和2∶4的化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com