
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | +3 | ||
| 其它 | 阳离子核外无电子 | 可做半导体材料 | 焰色反应呈黄色 |
 ;同位素;
;同位素;

科目:高中化学 来源: 题型:
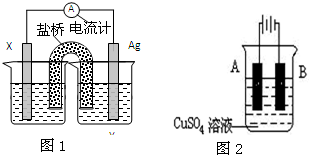 (Ⅰ)依据氧化还原反应:2Ag+(aq)+Fe(s)=Fe2+(aq)+2Ag(s)设计的原电池如图1所示.
(Ⅰ)依据氧化还原反应:2Ag+(aq)+Fe(s)=Fe2+(aq)+2Ag(s)设计的原电池如图1所示.查看答案和解析>>
科目:高中化学 来源: 题型:
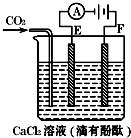 如图为持续电解含一定CaCl2水溶液的装置(以铂为电极),A为电流表.电解一段时间t1后,将CO2持续通入电解液中.
如图为持续电解含一定CaCl2水溶液的装置(以铂为电极),A为电流表.电解一段时间t1后,将CO2持续通入电解液中.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y | |
| Z | W |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeCl3溶液能够导电,所以FeCl3溶液是电解质 |
| B、CO2水溶液能够导电,所以CO2是电解质 |
| C、液态的铜导电性很好,所以铜是电解质 |
| D、NaOH固体溶于水后能导电,所以NaOH是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CH4分子的比例模型: |
| B、乙醇的分子式CH3CH2OH |
| C、苯的最简式 C6H6 |
| D、乙烯的结构简式CH2CH2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com