
【题目】依据下图中氮元素及其化合物的转化关系,回答问题:
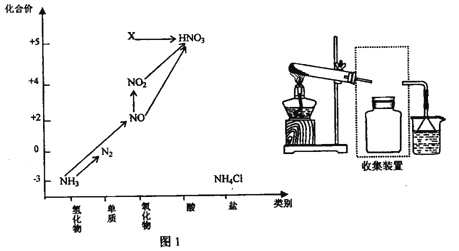
(1)实验窒常用NH4Cl 与Ca(OH)2制取氨气,该反应的化学方程式为___________。
(2)若要收集一瓶氨气,请将下列装置补充完整,在虚框内画出连接图。___________
(3)下列试剂不能用手干燥NH3的是_________。
A.浓硫酸 B.碱石灰 C.NaOH 固体
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO 化学方程式为____________。
②NO→NO2 实验现象是_______ 。
③ NO2![]() HNO3 氧 化剂 与 还原剂物质的量之比为_______。
HNO3 氧 化剂 与 还原剂物质的量之比为_______。
(5)图1中,实验室只用一种物质将NO 直接转化为硝酸且绿色环保,则该物质的化学式为_____________,
(6) 图1中,X的化学式为__________,从物质性质上看,X 属于_______氧化物。
(7)若要将NH3→N2,,从原理上看,下列试剂可行的是_______。
A.O2 B.Na C.NH4Cl D.NO2
【答案】 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O  A 4NH3+5O2
A 4NH3+5O2![]() 4NO+6H2O 无色气体变成红棕色 1:2 H2O2 N2O5 酸性 AD
4NO+6H2O 无色气体变成红棕色 1:2 H2O2 N2O5 酸性 AD
【解析】(1)实验室常用NH4Cl与Ca(OH)2制取氨气,生成氯化钙、氨气和水,化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;(2)氨气极易溶于水,比空气轻,收集方法只能用向下排空气法收集,导气管位置短进长出;
CaCl2+2NH3↑+2H2O;(2)氨气极易溶于水,比空气轻,收集方法只能用向下排空气法收集,导气管位置短进长出; (3)A.浓硫酸和氨气反应,不能干燥氨气,故A错误;B.碱石灰是氢氧化钠和氧化钙的混合物,可以干燥氨气,故B正确;C.NaOH固体吸收水分不与氨气反应,可以干燥氨气,故C正确。故选A。(4)①氨气的催化氧化:4NH3+5O2
(3)A.浓硫酸和氨气反应,不能干燥氨气,故A错误;B.碱石灰是氢氧化钠和氧化钙的混合物,可以干燥氨气,故B正确;C.NaOH固体吸收水分不与氨气反应,可以干燥氨气,故C正确。故选A。(4)①氨气的催化氧化:4NH3+5O2![]() 4NO+6H2O;②NO→NO2实验现象是无色气体变化为红棕色气体;③二氧化氮和水反应生成一氧化氮和硝酸,反应的化学方程式为:3NO2+H2O=2HNO3+NO,反应中二氧化氮化合价+4价变化为+5价和+2价,氧化剂与还原剂物质的量之比为1:2;(5)图1中,实验室只用一种物质将NO 直接转化为硝酸且绿色环保,3H2O2+2NO=2HNO3+2H2O,则该物质的化学式为H2O2;(6)图1分析可知X化合价与硝酸相同为+5价,物质类型为氧化物,X化学式为:N2O5,从物质性质上看,X 属于酸性氧化物;(7)若要将NH3→N2,,从原理上看,具有氧化性的试剂可行,A.O2具有氧化性,故A正确;B.Na只具有还原性,故B错误;C.NH4Cl与氨气不反应,故C错误;D.NO2具有氧化性,故D正确;故选AD。
4NO+6H2O;②NO→NO2实验现象是无色气体变化为红棕色气体;③二氧化氮和水反应生成一氧化氮和硝酸,反应的化学方程式为:3NO2+H2O=2HNO3+NO,反应中二氧化氮化合价+4价变化为+5价和+2价,氧化剂与还原剂物质的量之比为1:2;(5)图1中,实验室只用一种物质将NO 直接转化为硝酸且绿色环保,3H2O2+2NO=2HNO3+2H2O,则该物质的化学式为H2O2;(6)图1分析可知X化合价与硝酸相同为+5价,物质类型为氧化物,X化学式为:N2O5,从物质性质上看,X 属于酸性氧化物;(7)若要将NH3→N2,,从原理上看,具有氧化性的试剂可行,A.O2具有氧化性,故A正确;B.Na只具有还原性,故B错误;C.NH4Cl与氨气不反应,故C错误;D.NO2具有氧化性,故D正确;故选AD。


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
【题目】将0.2mol AgNO3、0.4mol Cu(NO3)2、0.6mol KCl溶于水,配成100mL溶液,用惰性电极电解一段时间后,若在一极析出0.3mol Cu,此时在另一极上产生的气体体积(标准状况)为( )
A.3.36 L
B.4.48 L
C.5.6 L
D.6.72 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 1 mol H2O 的质量是18 g/mol B. CH4 的摩尔质量是16 g
C. 1mol/LMgCl2溶液中含有Cl﹣的数目为2NA D. 3.01×1023个O2分子的质量是16 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的原电池装置,X、Y 为两电极,电解质溶液为稀硫酸,外电路中的电子流向如图,对此装置的下列说法正确的是( ) 
A.外电路的电流方向为:X→外电路→Y
B.若两电极分别为 Zn 和碳棒,则 X 为碳棒,Y 为 Zn
C.若两电极都是金属,则它们的活动性为 X>Y
D.X 极上发生的是还原反应,Y 极上发生的是氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。已知:2KMnO4+16HCl―→2KCl+5Cl2↑+2MnCl2+8H2O
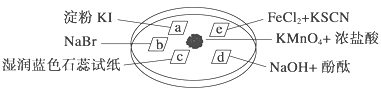
对实验现象的“解释或结论”正确的是 ( )
选项 | 实验现象 | 解释或结论 |
A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
C | d处立即褪色 | 氯气与水生成了漂白性物质 |
D | e处变红色 | 还原性:Fe2+>Cl- |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌锰干电池所含的汞、酸或碱等在废弃后进入环境中将造成严重危害.对废旧电池进行资源化处理显得非常重要.某化学兴趣小组拟采用如下处理方法回收废电池中的各种资源.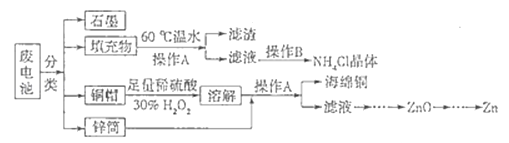
(1)碱性锌锰干电池的电解质为KOH,总反应为Zn+2MnO2+2H2O═2MnOOH+Zn(OH)2 , 其负极的电极反应式为
(2)填充物用60℃温水溶解,目的是加快溶解速率,但必须控制温度不能太高,其原因是
(3)操作A的名称为
(4)滤渣的主要成分为含锰混合物,向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止.其主要反应为2MnO(OH)+MnO2+2H2C2O4+3H2SO4═3MnSO4+4CO2↑+6H2O.
①当1mol MnO2参加反应时,共有 mol电子发生转移.
②MnO(OH)与浓盐酸在加热条件下也可发生反应,试写出其反应的化学方程式:
(5)铜帽溶解时加入H2O2的目的是 (用化学方程式表示).铜帽溶解完全后,可采用 方法除去溶液中过量的H2O2 .
(6)锌锰干电池所含的汞可用KMnO4溶液吸收.在不同pH下,KMnO4溶液对Hg的吸收率及主要产物如图所示:
根据图可知: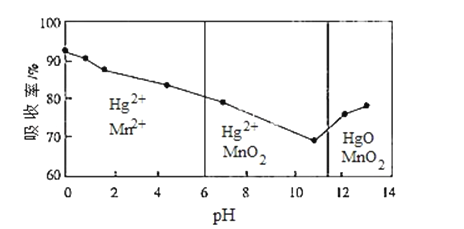
①pH对Hg吸收率的影响规律是
②在强酸性环境下Hg的吸收率高的原因可能是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 1mol H2O分子中含有6.02×1023个微粒 B. 44gCO2中含有1.204×1024个O原子
C. NH3的摩尔质量为17 D. 44.8L CH4含有2mol C原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com