
【题目】已知A、B、C、D和E是原子序数依次增大前20号元素。A原子价电子层p轨道中只有1个电子;B、C、D元素的基态原子具有相同的能层数,B、D元素原子的p能级上都有1个未成对电子,D原子得一个电子填入3p轨道后,3p轨道已充满,C原子的p轨道中有3个未成对电子;E是同周期第一电离能最小的元素。回答下列问题:
(1)A的元素符号为 ___________、 B3+的结构示意图为___________、C的最高价氧化物对应水化物为____________;E的价电子排布式为______________。
(2)上述五种元素中最高价氧化物对应水化物酸性最强的是___________,(填写化学式)碱性最强物质的电子式为_____________; D所在周期(除稀有气体元素外)第一电离能最小的元素是_________;在AD3分子中A元素原子的杂化方式是__________,分子空间构型为_______________;
(3)准晶是一种无平移周期序但有严格准周期位置序的独特晶体,可通过____________方法区分晶体、准晶体和非晶体。
(4)C单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为_____,列式表示Al单质的密度____________________g·cm﹣3(不必计算出结果)。
(5)石墨具有平面层状结构,同一层中的原子构成许许多多的正六边形,它与熔融的E单质相互作用,形成某种青铜色的物质(其中的元素E用“●”表示),原子分布如图所示,该物质的化学式为_______________。

【答案】 B ![]() H3PO4 4s1 HClO4
H3PO4 4s1 HClO4 ![]() Na sp2 平面三角形 X射线衍射 12
Na sp2 平面三角形 X射线衍射 12 ![]() KC8
KC8
【解析】A、B、C、D和E都是元素周期表中前20号的元素,它们的原子序数依次增大,B、C、D元素的基态原子具有相同的能层数,处于同一周期,B、D元素的原子的p能级上都有1个未成对电子,价层电子排布为ns2np1或ns2np5,D原子得一个电子填入3p轨道后,3p轨道已充满,故D为Cl元素,B为Al元素,C原子的p轨道中有3个未成对电子,价层电子排布为3s23p3,故C为P元素;E是同周期第一电离能最小的元素,处于第ⅠA族,原子序数最大,故E处于第四周期,为K元素,A原子的价电子层的p轨道中只有1个电子,价层电子排布为ns2np1,处于第ⅢA族,原子序数最小,故A为B元素。
(1)由上述分析可知,A为B元素,B为Al元素,Al3+的结构示意图为![]() ,C为P元素,最高价氧化物对应水化物为H3PO4,E为K元素,价电子排布式为4s1,故答案为:B;
,C为P元素,最高价氧化物对应水化物为H3PO4,E为K元素,价电子排布式为4s1,故答案为:B;![]() ;H3PO4;4s1;
;H3PO4;4s1;
(2)五种元素中Cl元素非金属性最强,最高价氧化物对应水化物酸性最强的是HClO4,K元素的金属性最强,故KOH碱性最强,电子式为![]() ,D为Cl元素,所在周期为第三周期,同周期自左而右,第一电离能增大,故第三周期中第一电离能最小的元素是Na;在BCl3分子中B原子与3个氯原子相连,没有孤对电子,杂化轨道数目为3,采用sp2杂化,空间构型为平面三角形,故答案为:HClO4,
,D为Cl元素,所在周期为第三周期,同周期自左而右,第一电离能增大,故第三周期中第一电离能最小的元素是Na;在BCl3分子中B原子与3个氯原子相连,没有孤对电子,杂化轨道数目为3,采用sp2杂化,空间构型为平面三角形,故答案为:HClO4,![]() ;sp2;平面三角形;
;sp2;平面三角形;
(3)准晶是一种无平移周期序但有严格准周期位置序的独特晶体,可通过X射线衍射方法区分晶体、准晶体和非晶体,故答案为:X射线衍射;
(4)Al单质为面心立方晶体,铝原子个数8×![]() +6×
+6×![]() =4,晶胞中铝原子的配位数为3×8÷2=12,Al单质的密度=
=4,晶胞中铝原子的配位数为3×8÷2=12,Al单质的密度=![]() =
=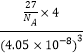 gcm-3=
gcm-3=![]() gcm-3,故答案为:12;
gcm-3,故答案为:12;![]() 。
。
(5)如图所示,K原子镶嵌在正六边形的中心,该正六边形周围有6个未镶嵌K原子的C原子正六边形结构,即每正六边形周围连接6个C原子,该碳原子为3个正六边形共有,故结构中K原子与C原子数目之比为1:(6+6×![]() )=8,故化学式为KC8,故答案为:KC8。
)=8,故化学式为KC8,故答案为:KC8。


科目:高中化学 来源: 题型:
【题目】硼和铝位于同一主族,它们可以形成许多性质类似的化合物。一种用硼镁矿(Mg2B2O5 H2O)制取单质硼的工艺流程图如下:

结合流程图回答下列问题:
(1)溶液a、溶液b中主要溶质的化学式分别为_______________、______________。
(2)写出步骤①的化学方程式_______________________________。
(3)写出步骤②的离子方程式_______________________________。
(4)步骤③中化学反应可以发生的原因是_____________________。
(5)过硼酸钠晶体(NaBO3 4H2O)是一种优良的漂白剂,在 70℃以上加热会逐步失去结晶水。实验测得过硼酸钠晶体 的质量随温度变化的情况如右图所示,则T2℃时所得晶体的化学式为 __________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙为两种不同介质的乙醇燃料电池(如下图所示)。下列说法正确的是

A. 装置甲和乙均是电能转化为化学能
B. X、Z极上分别消耗等物质的量乙醇时,流过甲、乙负载的电子数相同
C. Y、W极消耗氧气物质的量相同时,X、Z极消耗乙醇的物质的量也相同
D. Z极上发生的电极反应为:CH3CH2OH+5OH--4e-=CH3COO-+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现使用酸碱中和滴定法测定市售白醋的总酸量(g·100mL-1)。
Ⅰ.实验步骤
(1)配制100ml待测白醋溶液:用 (填仪器名称)量取10.00 mL食用白醋,在烧杯中用水稀释后转移到 (填仪器名称)中定容,摇匀即得待测白醋溶液。
(2)用酸式滴定管取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴 作指示剂。
![]()
(3)读取盛装0.1000 mol·L-1 NaOH 溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为________mL。
(4)滴定。当___________________________时,停止滴定,并记录NaOH溶液的终读数。重复滴定3次。
Ⅱ.实验记录
滴定次数实验数据(mL) | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00[ | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论
(1)按实验所得数据,可得c(市售白醋)= mol·L-1;
市售白醋总酸量= g·100 mL-1。
(2)在本实验的滴定过程中,下列操作会使实验结果偏大的是________填写序号)。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图与对应的反应情况正确的是
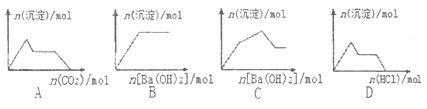
A. 含0.01molKOH和0.01molCa(OH)2的混合溶液中缓慢通入CO2
B. NaHSO4溶液中逐滴加入Ba(OH)2溶液
C. KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液
D. Na[Al(OH)4]溶液中逐滴加入盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中杂质(括号内为杂质)的除杂试剂和除杂方法都正确的是
物质及其杂质 | 除杂试剂 | 除杂方法 | |
A | CO2(SO2) | 饱和碳酸钠溶液 | 洗气 |
B | NH4Cl(I2) | 无 | 加热 |
C | Cl2 (HCl) | NaOH溶液 | 洗气 |
D | FeCl2(FeCl3) | 过量Fe粉 | 过滤 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(气)+B(气)![]() 2C(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2C(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应平均速率为0.3 mol·L-1·s-1
②用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7 mol·L-1
其中正确的是( )
A. ①③ B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前人类已发现几千万种物质,对物质进行分类,有利于我们的学习。对于H2SO4分类不合理的是( )
A. 酸 B. 含氧酸 C. 无氧酸 D. 强酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com