
| A. | Na2O2的电子式: | B. | Cl原子的结构示意图: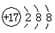 | ||
| C. | HClO分子的结构式:H-Cl-O | D. | 乙烯的结构简式:CH2CH2 |
分析 A.过氧化钠为离子化合物,其电子式中需要标出阴阳离子所带电荷;
B.氯原子的核电荷数=核外电子总数=17,最外层含有7个电子;
C.次氯酸的中心原子为O原子,分子中不存在H-Cl键;
D.乙烯的结构简式中漏掉了碳碳双键.
解答 解:A.Na2O2中含有钠离子和过氧根离子,其电子式为 ,故A正确;
,故A正确;
B.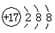 为硫离子结构示意图,氯原子的最外层电子数为7,其正确的原子结构示意图为:
为硫离子结构示意图,氯原子的最外层电子数为7,其正确的原子结构示意图为: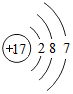 ,故B错误;
,故B错误;
C.HClO分子中含有1个H-O键和1个O-Cl键,其正确的结构式为:H-O-Cl,故C错误;
D.乙烯分子中含有1个碳碳双键,其正确的结构简式为:CH2=CH2,故D错误;
故选A.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及电子式、原子结构示意图、结构式、结构简式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的灵活应用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +2 | B. | +3 | C. | +4 | D. | +6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 物质 | 杂质 | 除杂试剂或操作方法 |
| ① | NaCl溶液 | Na2CO3 | 加入盐酸,蒸发 |
| ② | FeSO4溶液 | CuSO4 | 加入过量铁粉并过滤 |
| ③ | H2 | CO2 | 依次通过盛有NaOH溶液和浓硫酸的洗气瓶 |
| ④ | NaNO3 | CaCO3 | 加稀盐酸溶解、过滤、蒸发、结晶 |
| A. | ①②③④ | B. | ②③④ | C. | ①③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某实验小组对一含有Al3+的未知溶液进行分析:往该溶液逐滴滴加某浓度NaOH溶液,所加NaOH溶液体积(ml)与产生沉淀的物质的量(mol)的关系如下图所示:下列说法错误的是( )
某实验小组对一含有Al3+的未知溶液进行分析:往该溶液逐滴滴加某浓度NaOH溶液,所加NaOH溶液体积(ml)与产生沉淀的物质的量(mol)的关系如下图所示:下列说法错误的是( )| A. | 该未知溶液中至少含有3种阳离子 | |
| B. | 滴加的NaOH溶液的物质的量浓度为5mol•L-1 | |
| C. | 若将最终沉淀过滤、洗涤、灼烧,其质量一定为6 g | |
| D. | 若溶液中仅有两种金属阳离子,且另一种离子为二价阳离子,则a=10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室需要0.1mol•L-1NaOH溶液500mL,根据溶液的配制情况,回答下列问题:
实验室需要0.1mol•L-1NaOH溶液500mL,根据溶液的配制情况,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤族元素单质X2(X代表F、Cl、Br、I)均可以与水反应生成HX | |
| B. | 高纯度的硅单质用于制作光导纤维 | |
| C. | 将SO2通入次氯酸钙溶液可得到次氯酸 | |
| D. | 氢氧化铁溶于氢碘酸的离子方程式为:Fe(OH)3+3H+═Fe3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2和3 | B. | 3和2 | C. | 3和1 | D. | 1和3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com