
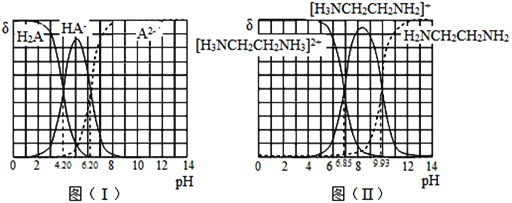
【题目】常温下,H2A和H2NCH2CH2NH2溶液中各组分的物质的量分数δ随pH的变化如图(I)、(II)所示。下列说法不正确的是已知:![]() 。
。
A.NaHA溶液中各离子浓度大小关系为:![]()
B.乙二胺(H2NCH2CH2NH2)的Kb2=10-7.15
C.[H3NCH2CH2NH3]A溶液显碱性
D.向[H3NCH2CH2NH2] HA溶液中通人HCl,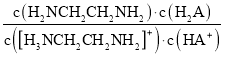 不变
不变
【答案】C
【解析】
A.由图1可知,当c(HA-)=c(A2-)时,溶液显酸性,所以NaHA溶液显酸性,电离程度大于水解程度,则各离子浓度大小关系为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-),故A正确;
B.由图2可知,当c([H3NCH2CH2NH2]+)=c[H3NCH2CH2NH3]2+)时,溶液的pH=6.85,c(OH-)=10-7.15mol·L-1,则
Kb2=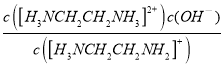 =c(OH-),Kb2=10-7.15,故B正确;
=c(OH-),Kb2=10-7.15,故B正确;
C.由图2可知,当c([H3NCH2CH2NH3]2+)=c([H3NCH2CH2NH]+)时,溶液的pH=6.85,c(OH-)=10-7.15mol·L-1,则Kb2=10-7.15,由图1可知,当c(HA-)=c(A2-)时,pH=6.2,则Ka2=10-6.2,[H3NCH2CH2NH3]2+的水解程度大于A2-的水解程度,溶液显酸性,故C错误;
D.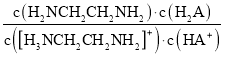 =
=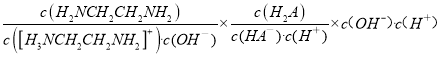
=![]() ,由于通入HCl,Kw、Kb1、Ka1都不变,所以
,由于通入HCl,Kw、Kb1、Ka1都不变,所以
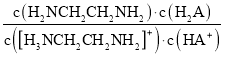 不变,故D正确。
不变,故D正确。
故选C。


科目:高中化学 来源: 题型:
【题目】根据有机化合物的命名原则,下列命名正确的是( )
A.![]() 3甲基1,3丁二烯
3甲基1,3丁二烯
B.![]() 2羟基丁烷
2羟基丁烷
C.CH3CH(C2H5)CH2CH2CH3 2乙基戊烷
D.CH3CH(NH2)CH2COOH 3氨基丁酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳捕获技术用于去除气流中的二氧化碳或者分离出二氧化碳作为气体产物,其中CO2催化合成甲酸是原子利用率高的反应,且生成的甲酸是重要化工原料。下列说法不正确的是( )

A. 二氧化碳的电子式: ![]()
B. 在捕获过程,二氧化碳分子中的共价键完全断裂
C. N(C2H5)3能够协助二氧化碳到达催化剂表面
D. CO2催化加氢合成甲酸的总反应式:H2+CO2=HCOOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z为短周期元素,X原子的质子数等于Z与Y的质子数之和;Z与Y位于同一周期,Y原子核外有3个未成对电子,非金属Z的一种固体单质可导电。回答下列问题:
(1)Y在周期表中的位置是第______周期第_____族,其原子结构示意图为_______________;Y与Z之间形成的化学键属于__________。
(2)X、Y、Z三种元素中原子半径最大的是__________(填元素符号);X单质既可与盐酸反应,又可溶于氢氧化钠溶液,产生的气体为__________(填分子式),该气体与Y单质反应的化学方程式为____________________________________。
(3)Z的最高价氧化物的电子式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗是意大利化学家(1776.08.09-1856.07.09),曾开业当律师,24岁后弃法从理,十分勤奋,终成一代化学大师。为了纪念他,人们把1 mol某种微粒集合体所含有的粒子个数,称为阿伏加德罗常数,用N![]() 表示。下列说法或表示中不正确的是
表示。下列说法或表示中不正确的是

A.科学上规定含有阿伏加德罗常数个粒子的任何微粒集合体都为1 mol
B.在K37ClO3+6H35Cl(浓)=KCl+3Cl2↑+3H2O反应中,若有212克氯气生成,则反应中电子转移的数目为5NA
C.60 克的乙酸和葡萄糖混合物充分燃烧消耗2NA个O2
D.6.02×1023mol-1 叫做阿伏加德罗常数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表示方法正确的是
A.等质量的硫蒸气和硫粉分别完全燃烧,后者放出的热量多
B.化学反应A2(g)+2B2(g)===2AB2(g)能量变化如图所示,该反应为放热反应
C.在25℃、101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)![]() 2H2O(l)△H= -285.8kJ·mol-1
2H2O(l)△H= -285.8kJ·mol-1
D.在稀溶液中,H+(aq)+OH-(aq)![]() H2O(l)△H=-57.3kJ·mol-1,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,整个过程放出的热量大于57.3kJ
H2O(l)△H=-57.3kJ·mol-1,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,整个过程放出的热量大于57.3kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】奥沙拉秦是曾用于治疗急、慢性溃疡性结肠炎的药物,其由水杨酸为起始物的合成路线如下:
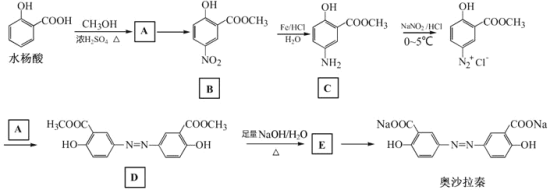
回答下列问题:
(1)A的结构简式为_________;由A制备B的反应试剂和条件为_______________。反应类型为_________。
(2)工业上常采用廉价的CO2与E反应制备奥沙拉秦,通入的CO2与E的物质的量之比至少应为_________。
(3)奥沙拉秦的分子式为_________,其核磁共振氢谱为_______组峰,峰面积比为__________。
(4)若将奥沙拉秦用HCl酸化后,分子中含氧官能团的名称为________________。
(5)W是水杨酸的同分异构体,可以发生银镜反应;W经碱催化水解后再酸化可以得到对苯二酚。W的结构简式为___________。
(6)写出下列反应的化学方程式:
由水杨酸制备A:____________________________________。
由D生成E:________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向体积为0.5L的AlCl3溶液中逐渐加入某浓度的NaOH溶液,得到的沉淀随NaOH溶液体积的变化如右图所示。下列结果不正确的是( )
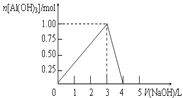
A. 反应过程中,沉淀最多时的质量为78g
B. 反应过程中,Al3+离子有1/3转化为Al(OH) 3沉淀,则加入的NaOH溶液的体积可能为3.5L
C. AlCl3溶液的浓度为2.0mol/L
D. 当V(NaOH)=4.0L时,得到的溶液中Na+、Cl-浓度一定不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2X(g)+Y(g)![]() 2Z(g)(正反应放热),在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量(n)与反应时间(t)的关系如图所示。
2Z(g)(正反应放热),在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量(n)与反应时间(t)的关系如图所示。
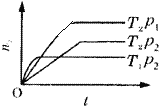
下述判断正确的是( )
A.T1>T2,p1>p2B.T1<T2,p1>p2
C.T1<T2,p1<p2D.T1>T2,p1<p2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com