
【题目】NO2、CO、CO2是对环境影响较大的气体,对它们的合理控制、利用是优化我们生存环境的有效途径。
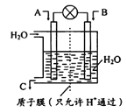
(1)如图所示,利用电化学原理将NO2 转化为重要化工原料C。
若A为NO2,B为O2,则负极的电极反应式为___________;
(2)光气 (COCl2)是一种重要的化工原料,用于农药、医药、
聚酯类材料的生产,工业上通过
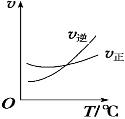
Cl2(g)+CO(g) ![]() COCl2(g)制备。左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。回答下列问题:
COCl2(g)制备。左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。回答下列问题:
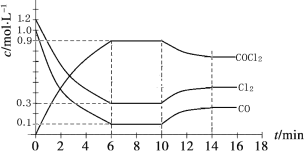
0~6 min内,反应的平均速率v(Cl2)= ;
保持温度不变,在第7min 向体系中加入这三种物质各2mol,则平衡向____________ 方向移动(填“正反应”、“逆反应”或“不”);
将初始投料浓度变为c(Cl2)=0.7mol/L、c(CO)=0.5mol/L、c(COCl2)=______ mol/L,
保持反应温度不变,则最终达到化学平衡时,Cl2的体积分数与上述第6min时Cl2的体积分数相同;
温度升高,该反应平衡常数变化的趋势是______;(填“增大”、“减小”或“不变”)
比较第8min反应温度T(8)与第15min反应温度T(15)的高低:T(8)_____T(15)
(填“<”、“>”或“=”)
【答案】30.(1)NO2-e-+H2O=NO3-+2H+
(2) ①0.15 molL-1min -1 ②平衡正向移动 ③ 0.5 ④ 减小 ⑤<
【解析】
试题分析:(1)该装置图是原电池,利用原电池原理将NO2 转化为重要化工原料C,因为A为NO2,B为O2,电解质为酸溶液,则C为硝酸,在负极,NO2失电子生成硝酸,所以负极的电极反应式为NO2-e-+H2O= NO3-+2H+。
(2)①根据图像可知,在0-6 min内,氯气的浓度减小了1.2mol/L-0.3mol/L=0.9mol/L,则反应的平均速率v(Cl2)=0.9mol/L÷6min=0.15 molL-1min -1.
②根据图像提供的数据,化学平衡常数为K=0.9÷(0.3×0.1)=30,假设容器体积为1L,保持温度不变,在第7min 向体系中加入这三种物质各2mol,Q=2.9÷(2.3×2.1)<30,平衡向正反应方向移动。
③最终达到化学平衡时,Cl2的体积分数与上述第6min时Cl2的体积分数相同,说明这两种状态属于等效平衡状态,若初始投料浓度变为c(Cl2)=0.7mol/L、c(CO)=0.5mol/L、根据等效平衡理论,c(COCl2)=1.2-0.7=0.5mol/L,
④根据图像可知,温度升高,平衡向逆反应方向移动,则化学平衡常数减小。
⑤第8min时反应处于平衡状态,在第10min时,CO和氯气的浓度增大,COCl2的浓度减小,说明平衡向逆反应方向移动,根据上述分析,温度升高,平衡向逆反应方向移动,所以T(8)< T(15)。


科目:高中化学 来源: 题型:
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
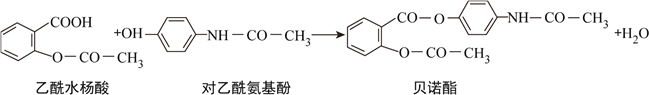
下列有关叙述正确的是( )
A. 贝诺酯分子中有三种含氧官能团
B. 可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚
C. 乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应
D. 贝诺酯与足量NaOH溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.沸水中滴入FeCl3饱和溶液:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
B.一小块钠投入水中:Na+2H2O===Na++2OH-+H2↑
C.用氢氧化钠溶液吸收过量二氧化碳:OH-+CO2===HCO![]()
D.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-===2Fe2++I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:
WO3 (s) + 3H2 (g)![]() W (s) + 3H2O (g)。请回答下列问题:
W (s) + 3H2O (g)。请回答下列问题:
(1)上述反应的化学平衡常数表达式为____________________。
(2) 某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为___________;随温度的升高,H2与水蒸气的体积比减小,则该反应为 反应(填“吸热”或“放热”)。
(3)用H2还原WO2也可得到金属钨。已知:
WO2 (s) + 2H2 (g)![]() W (s) + 2H2O (g) ΔH = +66.0 kJ·mol–1
W (s) + 2H2O (g) ΔH = +66.0 kJ·mol–1
WO2 (g) + 2H2 (g)![]() W (s) + 2H2O (g) ΔH =-137.9 kJ·mol–1
W (s) + 2H2O (g) ΔH =-137.9 kJ·mol–1
则WO2 (s)![]() WO2 (g) 的ΔH = ______________________。
WO2 (g) 的ΔH = ______________________。
(4)钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s) +2I2 (g)![]() WI4 (g)。下列说法正确的有________(填序号)。
WI4 (g)。下列说法正确的有________(填序号)。
a.灯管内的I2可循环使用 b.WI4在灯丝上分解,产生的W又沉积在灯丝上
c.WI4在灯管壁上分解,使灯管的寿命延长
d.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1﹣18号元素的离子aW3+、bX+、CY2﹣、dZ﹣都具有相同的电子层结构,则下列叙述或表示方法正确的是( )
A. 四种元素位于同一周期
B. 氢化物的稳定性H2Y>HZ
C. 离子的氧化性aW3+>bX+
D. 原子半径Z>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个氧化还原反应体系中反应物、生成物共六种粒子,Fe3+、NO![]() 、Fe2+、NH
、Fe2+、NH![]() 、H+和H2O,下列叙述正确的是( )
、H+和H2O,下列叙述正确的是( )
A.该反应说明Fe(NO3)2溶液不宜加酸酸化
B.该反应中氧化剂与还原剂物质的量之比为8∶1
C.若有1 mol NO![]() 发生氧化反应,则转移电子5 mol
发生氧化反应,则转移电子5 mol
D.若将该反应设计成原电池,则负极反应为Fe3++e-===Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016届北京东城一模】下列叙述正确的是( )
A.NaOH可用于治疗胃酸过多
B.CaO可防止月饼等食品氧化变质
C.氢弹中用到的2H、3H互为同位素
D.向海水中加入净水剂明矾可以使海水淡化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.离子键是阴、阳离子间存在的静电引力
B.只有金属和非金属化合时才能形成离子键
C.含有离子键的化合物一定是离子化合物
D.第ⅠA族和第ⅦA族元素原子化合时,一定形成离子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com