
【题目】写出下列反应的化学方程式:
(1)苯制备溴苯___________________。
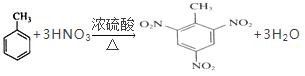
(2)制备TNT_____________________。
(3)2溴丙烷消去反应______________。
(4)实验室制乙烯__________________。
【答案】![]()
 CH3-CHBr-CH3
CH3-CHBr-CH3![]() CH2=CH-CH3↑+NaBr+H2O CH3CH2OH
CH2=CH-CH3↑+NaBr+H2O CH3CH2OH![]() CH2=CH2↑+H2O
CH2=CH2↑+H2O
【解析】
(1)苯与液溴在Fe催化下发生取代反应产生溴苯和溴化氢,反应方程式为:![]() ;
;
(2)甲苯与浓硝酸、浓硫酸混合加热,发生取代反应产生三硝基甲苯和水,三硝基甲苯俗称TNT,该反应的化学方程式为: ;
;
(3)2溴丙烷与NaOH的乙醇溶液在加热条件下发生消去反应,产生丙烯、NaBr、H2O,该反应的化学方程式为:CH3-CHBr-CH3![]() CH2=CH-CH3↑+NaBr+H2O;
CH2=CH-CH3↑+NaBr+H2O;
(4)乙醇与浓硫酸混合加热170℃,发生消去反应产生乙烯和水,反应方程式为:CH3CH2OH![]() CH2=CH2↑+H2O。
CH2=CH2↑+H2O。


科目:高中化学 来源: 题型:
【题目】有![]() 、
、![]() 、
、![]() 、
、![]() 四种元素,
四种元素,![]() 元素是地壳中含量最多的金属元素;
元素是地壳中含量最多的金属元素;![]() 元素的原子其
元素的原子其![]() 层(有电子)电子数比
层(有电子)电子数比![]() 层少1;
层少1;![]() 元素的原子得到2个电子和
元素的原子得到2个电子和![]() 元素的原子失去1个电子所得到的微粒都具有与氖原子相同的电子层结构。回答下列问题:
元素的原子失去1个电子所得到的微粒都具有与氖原子相同的电子层结构。回答下列问题:
(1)上述四种元素中![]() 元素的名称是______。
元素的名称是______。
(2)画出![]() 元素原子的结构示意图:____________。
元素原子的结构示意图:____________。
(3)写出下列化学方程式。
①单质![]() 在单质
在单质![]() 中燃烧:__________________;
中燃烧:__________________;
②![]() 的氢氧化物和
的氢氧化物和![]() 的氢氧化物在溶液中反应:________________________。
的氢氧化物在溶液中反应:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 为短周期元素,且原子序数依次递增。
为短周期元素,且原子序数依次递增。![]() 、
、![]() 同主族,
同主族,![]() 、
、![]() 同主族。
同主族。![]() 与其他非金属元素化合时易形成共价键,
与其他非金属元素化合时易形成共价键,![]() 与其他非金属元素化合时易形成离子键,且离子
与其他非金属元素化合时易形成离子键,且离子![]() 与
与![]() 的核外电子排布相同。气态分子
的核外电子排布相同。气态分子![]() 和
和![]() 具有相同的电子数,
具有相同的电子数,![]() 是空气中含量最高的物质。请回答下列问题:
是空气中含量最高的物质。请回答下列问题:
(1)![]() 位于第______周期______族;
位于第______周期______族;
(2)![]() 的简单离子结构示意图为______;
的简单离子结构示意图为______;
(3)![]() 的电子式是______;
的电子式是______;
(4)由![]() 、
、![]() 、
、![]() 三种元素形成的化合物的化学式为______,含有的化学键类型有______,属于______(填“共价”或“离子”)化合物。
三种元素形成的化合物的化学式为______,含有的化学键类型有______,属于______(填“共价”或“离子”)化合物。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《焦点访谈》栏目中曾报道“铊中毒事件”,铊再次成为公众关注的焦点。已知铊有两种天然同位素![]() 和
和![]() 。下列关于
。下列关于![]() 说法正确的是( )
说法正确的是( )
A. 中子数与质子数之差为122B. 中子数与电子数之差为122
C. 质量数与中子数之差为81D. 质量数与电子数之差为81
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用系统命名法给下列化合物命名:
(1)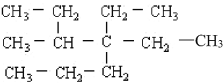 ______________________________
______________________________
(2)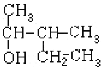 ______________________________
______________________________
(3)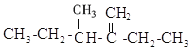 ______________________________
______________________________
(4)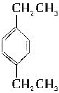 ___________________________
___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 、
、![]() 均为短周期元素,A元素的阳离子与B元素的阴离子具有相同的电子层结构,有关两元素有以下叙述:①原子序数:A>B;②原子半径:A<B;③离子半径:A>B;④原子最外层电子数:A≤B,其中正确的是( )
均为短周期元素,A元素的阳离子与B元素的阴离子具有相同的电子层结构,有关两元素有以下叙述:①原子序数:A>B;②原子半径:A<B;③离子半径:A>B;④原子最外层电子数:A≤B,其中正确的是( )
A.①②B.①④C.②③D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予在开发锂离子电池方面做出卓越贡献的三位化学家。锂离子电池的广泛应用要求处理锂电池废料以节约资源、保护环境。锂离子二次电池正极铝钴膜主要含有LiCoO2、A1等,处理该废料的一种工艺如下图所示:

回答下列问题:
(l) Li的原子结构示意图为____,LiCoO2中Co的化合价是____。
(2)“碱浸”时Al溶解的离子方程式为________。
(3)“酸溶”时加入H2O2的目的是____,调节pH后所得滤渣主要为____。
(4)“沉钴”的离子方程式为________。
(5)配制100mL l.0mol/L (NH4)2C2O4溶液,需要的玻璃仪器除玻璃棒、烧杯外,还需要____。
(6)取CoC2O4固体4.41g在空气中加热至300℃,得到钴的氧化物2.41g,则该反应的化学方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有几组物质的熔点数据如表所示。
A组 | B组 | C组 | D组 |
金刚石:3550℃ |
|
|
|
硅晶体:1410℃ |
|
|
|
硼晶体:2300℃ |
|
|
|
二氧化硅:1723℃ |
|
|
|
请回答下列问题:
(1)A组属于______晶体,其熔化时克服的微粒间的作用力是______。
(2)B组晶体共同的物理性质是______(填序号)。
A.有金属光泽 B.有导电性 C.有导热性 D.有延展性
(3)C组中酸性最弱的是______,最不稳定的是______。
(4)D组晶体可能具有的性质是______(填序号)。
A.硬度小 B.水溶液能导电 C.固体能导电 D.熔融状态下能导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对分子的性质的解释中,不正确的是
A.CH≡C-CH=CH-CH3 中σ键和π键数目之比为 10:3
B.![]() 分子中不含手性碳原子
分子中不含手性碳原子
C.硫难溶于水,微溶于酒精,易溶于 CS2,说明极性:水>酒精>CS2
D.由 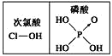 知酸性:H3PO4>HClO
知酸性:H3PO4>HClO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com