
【题目】按要求填写:
(1)二氧化碳的电子式:______________;小苏打的化学式:________________;质子数为6、中子数为6的原子结构示意图____________________。
(2)氯气与氢氧化钠溶液反应的化学方程式______________________________。
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F、G都是周期表中前四周期的元素,它们的核电荷数依次递增。其中A是形成化合物种类最多的元素;B原子核外有三个未成对电子;C是元素周期表中电负性最大的元素,化合物D2F为离子晶体,F原子核外的M层中只有两对成对电子;E单质的晶体类型在同周期的单质中没有相同的;G原子最外层电子数与D的相同,其余各层均充满电子。请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F、G用所对应的元素符号表示):
(1)C元素在元素周期表中的位置为____________________。
(2)D的氯化物的熔点比E的氯化物的熔点_____(填“高”或“低”),理由是_______。
(3)F的低价氧化物分子的立体构型是________,AO2的电子式为___________。
(4)A、B、D、E四种元素第一电离能最大的是_____。
(5)G2+能形成配离子[G(BH3)4]2+.写出该配离子的结构简式(标明配位键)_____。
(6)A能与氢、氧二种元素构成化合物AH2O,其中A原子的杂化方式为_____,1mol该分子中σ键的数目为_____,该物质能溶于水的主要原因是___________________。
(7)G晶体的堆积方式为__________________堆积,配位数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肌红蛋白(Mb)是由肽链和血红素辅基组成的可结合氧的蛋白,广泛存在于肌肉中。肌红蛋白结合氧的反应为:Mb(aq)+O2(g)![]() MbO2(aq)。肌红蛋白的结合度(即转化率α)与氧气分压p(O2)密切相关,37℃时,反应达平衡时测得的一组实验数据如图所示。回答下列问题:
MbO2(aq)。肌红蛋白的结合度(即转化率α)与氧气分压p(O2)密切相关,37℃时,反应达平衡时测得的一组实验数据如图所示。回答下列问题:

(1)37℃时,上述反应的平衡常数K=___________kPa-1(气体和溶液中的溶质分别用分压和物质的量浓度表达);
(2)平衡时,肌红蛋白的结合度α=___________[用含p(O2)和K的代数式表示];37℃时,若空气中氧气分压为20.0kPa,人正常呼吸时α的最大值为___________%结果保留2位小数);
(3)一般情况下,高烧患者体内MbO2的浓度会比其健康时___________(填“高”或“低”);在温度不变的条件下,游客在高山山顶时体内MbO2的浓度比其在山下时___________(填“高”或“低”);
(4)上述反应的正反应速率υ正=k正c(Mb)p(O2),逆反应速率υ逆=k逆c(MbO2)。k正和k逆分别是正向和逆向反应的速率常数。37℃时,上图中坐标为(1.00,50.0)的点对应的反应状态为向___________进行(填“左”或“右”),此时υ正︰υ逆=___________(填数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分元素在周期表中的分布如右图所示(虚线为金属元素与非金属元素的分界线),下列说法不正确的是

A. 虚线左侧是金属元素
B. As处于第五周期第VA族
C. Si、Ge可作半导体材料
D. Sb既有金属性又有非金属性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:[FeCl4(H2O)2]-为黄色,下列实验所得结论不正确的是
① | ② | ③ | ④ |
0.1mol/L Fe2(SO4)3溶液 |
酸化的0.1mol/L Fe2(SO4)3溶液 |
酸化的0.1mol/L Fe2(SO4)3溶液 |
0.1mol/L FeCl3溶液 |
加热前溶液为浅黄色,加热后颜色变深 | 加热前溶液接近无色,加热后溶液颜色无明显变化 | 加入NaCl后,溶液立即变为黄色,加热后溶液颜色变深 | 加热前溶液为黄色,加热后溶液颜色变深 |
注:加热为微热,忽略体积变化。
A. 实验①中,Fe2(SO4)3溶液显浅黄色原因是Fe3+水解产生了少量Fe(OH)3
B. 实验②中,酸化对Fe3+水解的影响程度大于温度的影响
C. 实验③中,存在可逆反应: Fe3+ + 4Cl-+ 2H2O ![]() [FeCl4(H2O)2]-
[FeCl4(H2O)2]-
D. 实验④,可证明升高温度,Fe3+水解平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子书写正确的是( )
A.碳酸氢钠溶液中加入盐酸:CO32﹣+2H+=CO2↑+H2O
B.向沸水中滴加饱和的FeCl3溶液制备Fe(OH)3胶体: Fe3++ 3H2O ![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
C.氢氧化铜与稀硫酸反应:H++OH﹣=H2O
D.澄清的石灰水与碳酸钠溶液反应:CO32﹣+Ca2+=CaCO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式正确的是
A. 甲烷的标准燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B. 500 ℃、30 MPa 下,将0.5 mol N2 和 1.5 mol H2 置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g) ![]() 2NH3(g)ΔH=-38.6 kJ·mol-1
2NH3(g)ΔH=-38.6 kJ·mol-1
C. 已知在120 ℃、101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为:H2(g)+![]() O2(g)
O2(g)![]() H2O(g) ΔH=-242 kJ/mol
H2O(g) ΔH=-242 kJ/mol
D. CO(g)的燃烧热是283.0 kJ·mol-1,则2CO2(g)===2CO(g)+O2(g)反应的ΔH=+283.0 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应X(g)+Y(g)![]() 2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A. 反应前2 min的平均速率v(Z)=2.0×10-3 mol·(L·min)-1
B. 其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C. 该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如下:
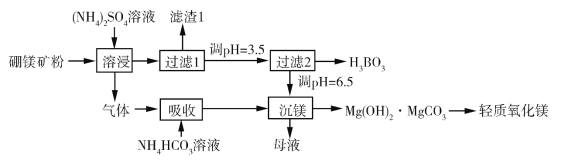
回答下列问题:
(1)在95 ℃“溶侵”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式为_________。
(2)“滤渣1”的主要成分有_________。为检验“过滤1”后的滤液中是否含有Fe3+离子,可选用的化学试剂是_________。
(3)根据H3BO3的解离反应:H3BO3+H2O![]() H++B(OH)4,Ka=5.81×1010,可判断H3BO3是_______酸;在“过滤2”前,将溶液pH调节至3.5,目的是_______________。
H++B(OH)4,Ka=5.81×1010,可判断H3BO3是_______酸;在“过滤2”前,将溶液pH调节至3.5,目的是_______________。
(4)在“沉镁”中生成Mg(OH)2·MgCO3沉淀的离子方程式为__________,母液经加热后可返回___________工序循环使用。由碱式碳酸镁制备轻质氧化镁的方法是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com