
【题目】在室温下,下列五种溶液:①0.1mol/L NH4Cl②0.1mol/L CH3COONH4 ③0.1mol/LNH4HSO4④0.1mol/L NH3H2O和0.1mol/L NH4Cl混合液 ⑤0.1mol/L NH3H2O。
请根据要求填写下列空白:
(1)溶液①呈_____性(填“酸”、“碱”或“中”),其原因是________(用离子方程式表示)。
(2)比较②③溶液中,c(NH4+)的大小关系是②______③(填“>”“<”或“=”)。
(3)在溶液④中,_____ 离子的浓度为0.1mol/L;NH3H2O和_____离子的物质的量浓度之和为0.2mol/L。
(4)室温下,测得溶液②的pH=7,则CH3COO-的水解程度_____(填“>”“<”或“=”)NH4+-的水解程度。CH3COO-与NH4+浓度的大小关系是:c(CH3COO-)_____c(NH4+)(填“>”“<”或“=”)。
【答案】酸 NH4++H2O![]() NH3H2O+H+
NH3H2O+H+ ![]() Cl- NH4+ = =
Cl- NH4+ = =
【解析】
(1)氯化铵溶液中铵根离子水解显酸性;
(2)酸溶液中氢离子浓度越大,溶液pH越小,结合铵根离子水解的影响因素分析;
(3)0.1mol/L NH3H2O和0.1mol/L NH4Cl混合液中,氯离子不变,铵根离子水解,依据离子性质和物料守恒分析;
(4)醋酸根离子水解程度和铵根离子水解程度几乎相同。
(1)氯化铵溶液中铵根离子水解显酸性,NH4++H2O![]() NH3H2O+H+;
NH3H2O+H+;
(2)②0.1mol/L CH3COONH4中CH3COO-水解会促进NH4+的水解;
③0.1mol/L NH4HSO4 溶液中电离出氢离子显酸性,抑制铵根离子水解;
上述分析可知酸性最强的是0.1mol/L NH4HSO4溶液,铵根离子浓度c(NH4+):②<③;
(3)在④中0.1mol/L NH3H2O和0.1mol/LNH4Cl混合液中,氯离子物质的量不变,浓度不变,浓度为0.1mol/L,铵根离子水解,一水合氨电离,一水合氨的电离作用大于铵根离子的水解作用,使溶液呈碱性,根据溶液中料守恒可知,c(NH3H2O)+c(NH4+)=0.2mol/L;
(4)测得溶液②的pH=7,醋酸根离子水解程度和铵根离子水解程度几乎相同,则CH3COO-与NH4+浓度的大小关系是相同。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】向1L的密闭容器中加入1molX、0.3molZ和一定量的Y三种气体。一定条件下发生反应,各物质的浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。下列说法不正确的是
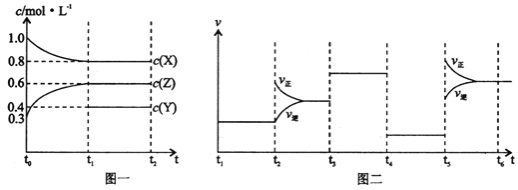
A.Y的起始物质的量为0.5mol
B.该反应的化学方程式为:2X(g)+Y(g)![]() 3Z(g)H<0
3Z(g)H<0
C.若t0=0,t1=10s,则t0~t1阶段的平均反应速率为v(Z)=0.03mol/(L·s)
D.反应物X的转化率t6点比t3点高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种钌(Ru)基配合物光敏染料敏化太阳能电池的原理及电池中发生的主要反应如图所示。下列说法正确的是

A. 镀铂导电玻璃的作用是传递I-
B. 电池工作时,光能转变为电能,X为电池的正极
C. 电池的电解质溶液中I-和I3-的浓度均不断减小
D. 电解质溶液中发生反应2Ru3++3I-═2Ru2++I3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ,且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1mol H-O键形成时放出热量463 kJ,则氢气中1mol H-H键断裂时吸收热量为
A.920 kJB.557 kJC.436 kJD.188 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。 回答下列问题:

(1)外电路的电流方向是由________极流向________极(填字母)。
(2)电池正极反应式为___________________________________。
(3)是否可用水代替电池中的混合有机溶剂?________(填“是”或“否”),原因是________________________________________________________________。
(4)MnO2可与KOH和KClO3在高温下反应,生成K2MnO4,反应的化学方程式为_______________________________________________。K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关同分异构体的叙述正确的是( )
A.![]() 苯环上的一氯取代物有5种
苯环上的一氯取代物有5种
B.丁烷(C4H10)的二氯取代物最多有4种
C.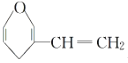 和
和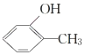 互为同分异构体
互为同分异构体
D.菲的结构简式为![]() ,其一硝基取代物有10种
,其一硝基取代物有10种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体血液存在![]() 、
、![]() 等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值lgx[x表示
等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值lgx[x表示![]() 或
或![]() ]与
]与![]() 的关系如图所示。已知碳酸
的关系如图所示。已知碳酸![]() 、磷酸
、磷酸![]() 。则下列说法正确的是
。则下列说法正确的是

A.曲线![]() 表示lg(
表示lg(![]() )与
)与![]() 的变化关系
的变化关系
B.![]() 的过程中,水的电离程度逐渐减小
的过程中,水的电离程度逐渐减小
C.当![]() 时
时![]()
D.当![]() 增大时,
增大时,![]() 逐渐减小
逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是制造新型信息材料的中间体,B是制备血管紧张素抑制剂卡托普利的原料,它们有如下的转化关系:
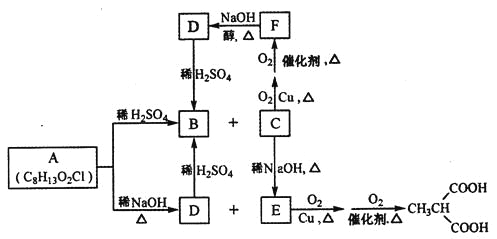
试回答下列问题:
(1)B的名称是______________,C含有的官能团名称是_____________。
(2)C→E的反应类型是_____________,C→F的反应类型是______________。
(3)A的结构简式为____________。
(4)写出与F具有相同官能团的F的所有同分异构体_____________(填结构简式)
(5)已知![]() ,请以2一甲基丙醇和甲醇为原料,设计制备有机玻璃(聚甲基丙烯酸甲酯)的合成路线.合成路线流程图示例如下:___________________
,请以2一甲基丙醇和甲醇为原料,设计制备有机玻璃(聚甲基丙烯酸甲酯)的合成路线.合成路线流程图示例如下:___________________![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在Fe(NO3)3和Cu(NO3)2的混合液中逐渐加入铁粉,溶液中Fe2+的物质的量浓度和加入铁粉的物质的量之间关系如图所示,则该溶液中Fe(NO3)3与Cu(NO3)2的物质的量浓度之比为
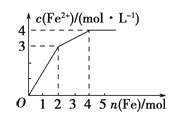
A.3∶1 B.1∶2 C.2∶1 D.1∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com