
【题目】有机物 A 是未成熟葡萄中含有的一种物质,由 C、H、O 三种元素组成,A 在气态时的密度是相同条件下氢气密度的 38 倍。在一定条件下 A 既可以与乙醇反应生成酯又可以与乙酸反应生成酯。已知 0.1mol A 完全燃烧时生成 0.2mol CO2 和 0.2mol H2O;1mol A 可与 2mol Na 或 1mol NaOH 反应。试确定:
(1)有机物 A 的分子式_________________;
(2)写出在浓硫酸作用下,两分子 A 相互反应生成六元环状物质的化学方程式______________。
【答案】C2H4O3 
【解析】
根据密度与相对分子质量成正比,求出相对分子质量,再根据生成的CO2 和 H2O的物质的量,求出碳原子和氢原子的个数,最后求出氧原子的个数,得到分子式;根据与 Na 或 NaOH 反应,得到含有的官能团和官能团的个数,得到结构式,由此解题。
(1) 根据相同条件下,气体的密度比等于相对分子质量之比,得A的相对分子质量是38×2 =76,由0.1mol A 完全燃烧时生成0.2mol CO2和0.2mol H2O得每个分子中含有2个碳原子和4个氢原子,设A 的分子式为C2H4Ox,则2×12+4×1+x×16=76,得x=3,分子式为C2H4O3;
(2) 由1mol A 可与 2mol Na 或 1mol NaOH 反应,可知分子中含有一个羟基和一个羧基,则A结构为 ,在浓硫酸作用下,两分子A 相互间发生酯化反应形成六元环状物质,化学方程式为
,在浓硫酸作用下,两分子A 相互间发生酯化反应形成六元环状物质,化学方程式为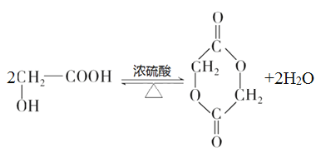 。
。


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
【题目】工业上用CO和H2生产燃料甲醇。一定条件下密闭容器中发生反应,测得数据曲线如下图所示(反应混合物均呈气态)。下列说法错误的是
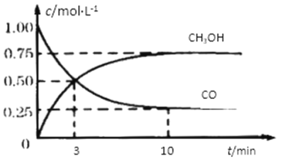
A.反应的化学方程式:CO+2H2![]() CH3OH
CH3OH
B.反应进行至3分钟时,正、逆反应速率相等
C.反应至10分钟,(CO) = 0.075 mol/L·min
D.增大压强,平衡正向移动,K不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温下,物质的量之比为2∶1的SO2和O2的混合气体在容积为2 L的恒容密闭容器中发生反应:2SO2(g)+O2(g)![]() 2SO3(g)(正反应为放热反应),n(SO2)随时间变化关系如下表:
2SO3(g)(正反应为放热反应),n(SO2)随时间变化关系如下表:
时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
下列说法正确的是( )
A. 当容器中气体的密度不变时,该反应达到平衡状态
B. 该反应进行到第3分钟时,逆反应速率小于正反应速率
C. 从反应开始到达到平衡,用SO3表示的平均反应速率为0.01 mol/(L·min)
D. 容器内达到平衡状态时的压强与起始时的压强之比为5∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说法不正确的是( )
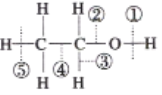
A. 和金属钠反应时键①断裂,发生置换反应
B. 在铜催化下与O2共热反应时断裂①和③,发生氧化反应
C. 与浓硫酸共热170°C下,主要断裂①和②,发生取代反应
D. 在空气中完全燃烧时断裂①②③④⑤,发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10.00 mL 0.1mol/L某二元酸H2X溶液中逐滴加入0.1 mol/L NaOH溶液,其pH变化如图所示(忽略温度变化),已知:常温下,H2X的电离常数Ka1=1.1×10-5,Ka2=1.3×10-8。下列叙述正确的是
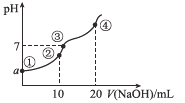
A.a近似等于3
B.点②处c(Na+)+2c(H+)+c(H2X)=2c(X2-)+c(HX-)+2c(OH-)
C.点③处为H2X和NaOH中和反应的滴定终点
D.点④处c(Na+)=2c(X2-)>c(OH-)>c(HX-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 可简写为
可简写为![]() ,降冰片烯的分子结构可表示为:
,降冰片烯的分子结构可表示为: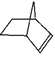
(1)降冰片烯属于__________。
A.环烃 B.烷烃 C.不饱和烃 D.芳香烃
(2)降冰片烯的分子式为____________.
(3)降冰片烯的一种同分异构体(含有一个六元环的单环化合物)的结构简式为________.
(4)推断降冰片烯应该具有的性质是__________。
A.能溶于水 B.能使高锰酸钾溶液褪色
C.能与氢气发生加成反应 D.常温常压下为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C为短周期元素,在周期表中所处的位置如图所示。A、C两元素的原子核外电子数之和等于B原子的电子数。B原子核内质子数和中子数相等。
![]()
(1)写出A、B、C三元素名称:________、________、________。
(2)C在元素周期表中的位置是________
(3)B的原子结构示意图为____,C的氢化物与B的氢化物的稳定性强弱顺序为___>___(填化学式)。
(4)比较A、C的原子半径:A________(填“>”或“<”)C,写出A的气态氢化物与A的最高价氧化物对应水化物反应的化学方程式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PBAT(聚已二酸对苯二甲酸丁酯)可被微生物几乎完全降解,成为包装、医疗和农用薄膜等领域的新兴材料,它可由聚合物PBA和PBT共聚制得,一种合成路线如下:

已知: 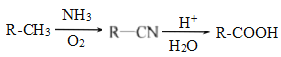
![]()
回答下列问题:
(1)G的官能团的名称为________。
(2)①的反应类型为___________;反应②所需的试剂和条件是___________。
(3)D的结构简式为___________;H的化学名称为___________。
(4)⑤的化学方程式为_______________________________________________。
(5)M与G互为同系物,M的相对分子质量比G大14;N是M的同分异构体,写出同时满足以下条件的N的结构简式:___________________(写两种,不考虑立体异构)。
Ⅰ、既能与FeCl3发生显色反应,又能发生水解反应和银镜反应;
Ⅱ、与NaOH溶液反应时,1mol N能消耗4molNaOH;
Ⅲ、核磁共振氢谱有五组峰,峰面积比为1:2:2:2:1。
(6)设计由丙烯为起始原料制备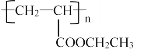 的单体的合成路线(其它试剂可任选)________________________________________________________________。
的单体的合成路线(其它试剂可任选)________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com