
【题目】已知A、F为金属单质,C是淡黄色粉末,回答下题。
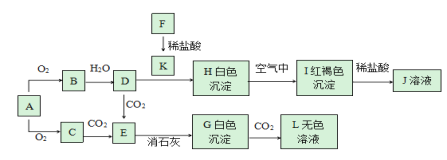
(1)实验室中A常常保存在__中,若将0.1molC直接转化成D,转移电子数为__个。
(2)写出D与J混合的离子反应方程式__。
(3)用化学方程式表示沉淀H转化成I颜色发生变化的原因:__。
(4)直接向K溶液中加入C固体,写出可能出现的现象:__。
(5)向盛有L溶液的水槽中加入一小块金属A,下列现象描述不符合实际情况的是__。
a.金属A浮在液面,并四处游动
b.金属A会熔化成一个小球
c.反应开始后,溶液由无色变成红色
d.恢复到室温时,烧杯底部有固体物质析出
(6)0.12molFeCl2加入100mLK2Cr2O7溶液中,恰好使溶液中Fe2+全部转化为Fe3+,Cr2O72-被还原为Cr3+。则K2Cr2O7溶液的物质的量浓度为__。
【答案】煤油 0.1NA(或6.02×1022) Fe3++3OH-=Fe(OH)3↓ 4Fe(OH)2+O2+2H2O=4Fe(OH)3 有无色气体生成,产生红褐色沉淀 c 0.2mol·L-1
【解析】
A为金属单质,A与氧气反应生成的C是淡黄色粉末,则A为Na,C为Na2O2。由转化关系可知B是Na2O、D是NaOH、E是Na2CO3、G是CaCO3、L是Ca(HCO3)2。金属F与盐酸反应生成K,而K能与NaOH反应生成白色沉淀H,H在空气中可以转化为红褐色沉淀I,则F为Fe、K为FeCl2、H为Fe(OH)2、I为Fe(OH)3、J为FeCl3;Fe2+转化为Fe3+,Cr2O72-被还原为Cr3+,根据电子守恒列式计算。
(1)实验室中Na常常保存在煤油中。C转变成D的化学方程式:2Na2O2+2H2O=4NaOH+O2↑,反应中过氧化钠既是氧化剂又是还原剂,各占一半,0.1mol 过氧化钠参与该反应,转移电子的个数为:0.1mol×1/2×2×6.02×1023 mol-1=6.02×1022;
(2)D与J混合的离子反应方程式为:Fe3++3OH-=Fe(OH)3↓;
(3)用化学方程式表示沉淀H转化成I颜色发生变化的原因:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(4)直接向FeCl2溶液中加入Na2O2固体,过氧化钠能与水反应生成氢氧化钠与氧气,过氧化钠具有强氧化性,会得到Fe(OH)3,可能出现的现象:有无色气体生成,产生红褐色沉淀;
(5)向盛有Ca(HCO3)2溶液的水槽中加入一小块金属Na,Na与水反应生成NaOH与氢气,NaOH再与Ca(HCO3)2反应生成CaCO3,可以看到的现象:金属Na浮在液面,熔化成一个小球,发出嘶嘶声响,并四处游动,最后消失,恢复到室温时烧杯底白色沉淀,故答案为c;
(6)FeCl2失去电子的物质的量为:0.12mol×(3-2)=0.12mol,设K2Cr2O7溶液的物质的量浓度为cmol/L,K2Cr2O7得电子的物质的量为:0.1L×2×(6-3)cmol/L=0.6cmol,根据得失电子守恒可知:0.6cmol=0.12mol,解得:c=0.2mol/L。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(1)某无色溶液中只含有下列7种离子中的某几种:Mg2+、H+、Ag+、Na+、Cl-、HCO3-、OH-,已知该溶液与铝反应放出氢气,若反应后生成AlO2-,则溶液中一定存在的离子有______________,一定不存在的离子有______________,可能存在的离子有__________________,该溶液与铝反应放出氢气的离子方程式为_____________________________________。
(2)铁、铜单质及其化合物应用范围很广。现有含氯化亚铁杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,某兴趣小组首先将其制成水溶液。
①通常将氢氧化钠溶液加入氯化亚铁溶液的实验现象是___,
②书写氢氧化亚铁在空气中转化为氢氧化铁的化学方程式___。
(3)在所得的FeCl3、CuCl2混合溶液中加入镁粉,产生的气体是___。试解释原因:___。有同学提出加入CuO以除去Fe3+。你认为理由是___。
(4)能不能直接蒸发CuCl2溶液得到CuCl2·2H2O晶体?___(填“能”或“不能”)。若能,不用回答;若不能,说明理由___。
(5)将FeCl3固体溶于蒸馏水配制溶液时常会出现浑浊,得不到澄清的氯化铁溶液,其原因是___,如果要得到澄清的氯化铁溶液,可采取的措施是___。
(6)泡沫灭火器使用NaHCO3和Al(SO4)3溶液反应产生CO2来灭火。试从平衡移动的角度分析以上两种溶液反应产生CO2的原因:____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在抗击新冠肺炎的过程中,科研人员研究了法匹拉韦、利巴韦林、氯硝柳胺等药物的疗效,三种药物主要成分的结构简式如下。下列说法不正确的是
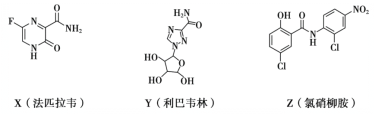
A.X的分子式为C5H4O2N3F
B.Z中含有6种官能团
C.Y和Z都有羟基,但性质不完全相同
D.X和Z都能发生加成反应和水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用煤油作溶剂,二(2-乙基己基)磷酸酯作流动载体,H2SO4 作内相酸处理含铜废水。 在其他条件相同时,Cu2+萃取率[萃取率=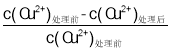 ×100% ]与初始 Cu2+浓度关系如图 1 所示;在其他条件相同时,处理前初始 Cu2+浓度为 200 mg·L-1,Cu2+萃取率与废水 pH 的关系如图 2 所示。下列说法错误的是
×100% ]与初始 Cu2+浓度关系如图 1 所示;在其他条件相同时,处理前初始 Cu2+浓度为 200 mg·L-1,Cu2+萃取率与废水 pH 的关系如图 2 所示。下列说法错误的是
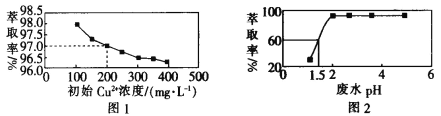
A.根据图 1 可知,废水中初始 Cu2+浓度越大,Cu2+的萃取效果越好
B.根据图 2 可知,废水初始 pH>2 时,去除 Cu2+的效果较好
C.根据图 1 可知,Cu2+初始浓度为 200 mg·L-1 时,Cu2+的萃取率为 97.0%
D.根据图 2 可知,若取 800 mL 初始 Cu2+浓度为 200 mg·L-1 的废水,在 pH=1.5 时处理废水,则处理后的废水中剩余 Cu2+的物质的量为 1.5×10-3mol(假设体积不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的化合物是造成大气污染的主要物质,研究有关反应机理对于消除环境污染有重要意义。
(1)NO在空气中存在如下反应:2NO(g)+O2(g)![]() 2NO2(g)△H,上述反应分两步完成,其反应历程如图所示:回答下列问题:
2NO2(g)△H,上述反应分两步完成,其反应历程如图所示:回答下列问题:
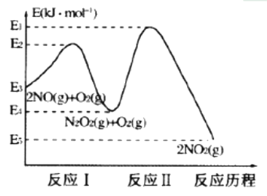
①写出反应I的热化学方程式______________。
②升高温度发现总反应2NO(g)+O2(g)![]() 2NO2(g)的速率反而变慢,结合上图判断下列说法中正确的有_______(反应未使用催化剂)。
2NO2(g)的速率反而变慢,结合上图判断下列说法中正确的有_______(反应未使用催化剂)。
A 反应I是快反应,反应II是慢反应 B 总反应的速率由反应I决定
C 升高温度平衡I、II均向逆反应方向移动 D 对于反应II,浓度的影响大于温度的影响
(2)用焦炭还原NO2的反应为2NO2(g)+2C(s)![]() N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
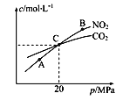
①A、B两点的浓度平衡常数关系:Kc(A)___Kc(B)(填“<”“>”或“=”)
②A、B、C三点中NO2的转化率最低的是___(填“A”“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp(C)=_______(Kp是用平衡分压代替平衡浓度计算)
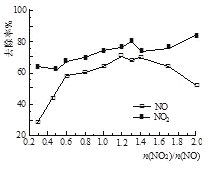
(3)一定条件下,将一定浓度NOx(NO2和NO的混合气体)通入0.05 mol·L1的Ca(OH)2乳浊液中,发生的反应为:3NO2 + 2OH-= NO +2NO3-+ H2O;NO + NO2 +2OH-= 2NO2- + H2O。改变![]() ,NOx的去除率如图所示:
,NOx的去除率如图所示:
 。
。
①![]() 的合适范围是____。
的合适范围是____。
②当![]() 大于1.4时,NO2去除效率升高,但NO去除效率却降低。其可能的原因是____ 。
大于1.4时,NO2去除效率升高,但NO去除效率却降低。其可能的原因是____ 。
③O3和NO发生的主要反应为:NO + O3 = NO2 + O2。保持NO的初始浓度不变,改变![]() ,将反应后的混合气体通入0.05mol·L1Ca(OH)2乳浊液中吸收。为节省O3的用量,又能保持NOx去除效果,则
,将反应后的混合气体通入0.05mol·L1Ca(OH)2乳浊液中吸收。为节省O3的用量,又能保持NOx去除效果,则![]() 合适的值约为_________。
合适的值约为_________。
a 0.6 b 0.8 c 1.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于四大基本反应类型,但属于氧化还原反应的是
A. 2Na+2H2O===2NaOH+H2↑
B. Cl2+H2O===HCl+HClO
C. CaCO3![]() CaO+CO2↑
CaO+CO2↑
D. Ca(ClO)2+2HCl===CaCl2+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类推思维是化学解题中常用的一种思维方法,下列有关反应方程式(或离子方程式)的类推正确的是( )
已知 | 类推 | |
A | 将Fe加入CuSO4溶液中: Fe + Cu2+ = Cu + Fe2+ | 将Na加入到CuSO4溶液中: 2Na + Cu2+ = Cu + 2Na+ |
B | 稀硫酸与Ba(OH)2溶液反应至溶液呈中性: 2H++SO42﹣+Ba2++2OH﹣=BaSO4↓+2H2O | NaHSO4溶液与Ba(OH)2溶液反应呈中性: 2H++SO42﹣+Ba++2OH﹣=BaSO4↓+2H2O |
C | 铁和氯气反应2Fe+3Cl2 | 铁和单质反应2Fe+3I2 |
D | 向Ca(ClO)2溶液中通入少量CO2: Ca2++2ClO﹣+CO2+H2O=CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2: Ca2++2ClO﹣+SO2+H2O=CaSO3↓+2HClO |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法错误的是( )
A.石油和天然气的主要成分都是碳氢化合物
B.乙酸和乙酸乙酯都能与氢氧化钠溶液反应
C.糖类、油脂和蛋白质都是人体重要的营养物质
D.一定条件下,苯能发生加成反应、取代反应、氧化反应、加聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种化合物,均含有常见元素,它们的转化关系如图所示,其中A为澄清溶液,C为难溶的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。
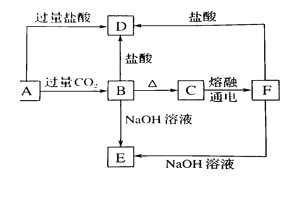
(1)写出化学式;
A______ ,C______ ,D______ ,E______
(2)写出下列反应的离子方程式:
①A→B: _____________________________________________
②B→E: _____________________________________________
③C→E: _____________________________________________
④F→E: _____________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com