
| A、蒸馏水 | B、人的胃液 |
| C、醋酸钠溶液 | D、氯化铵溶液 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
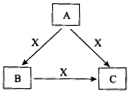 A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.若A、B、C的焰色反应均呈黄色,水溶液均为碱性.
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.若A、B、C的焰色反应均呈黄色,水溶液均为碱性.查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)常温下,CH3COONa溶液呈
(1)常温下,CH3COONa溶液呈查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol?L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
| c(S2O82-/mol?L-1) | 0.040 | 0.040 | 0.080 | 0.080 | 0.040 |
| t/s | 88 | 44 | 22 | 11 | t1 |
| 催化剂 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH<7的溶液一定呈酸性 |
| B、0.1mol/LKOH溶液和0.1mol/L氨水中,其c(OH-)相等 |
| C、pH为1的盐酸的c(H+)是pH为3的盐酸的100倍 |
| D、Na2 CO3溶液中,c(Na+)是c(CO32-)的两倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化镁固体之所以不导电的原因是氯化镁固体中不含阴、阳离子 |
| B、在电流作用下氯化钠在水溶液中电离成钠离子和氯离子 |
| C、氯化钾固体不能导电而其水溶液能导电的原因是氯化钾与水发生反应产生了钾离子和氯离子 |
| D、氯化钾固体不能导电的原因是构成氯化钾固体的钾离子和氯离子不能自由移动,而溶于水后在水分子的作用下产生自由移动的钾离子和氯离子,所以其水溶液能导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等量的硫蒸汽和硫固体分别完全燃烧,后者放出热量多 |
| B、在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(l);△H=-285.8kJ/mol |
| C、在稀溶液中:H+(aq)+OH-(aq)═H2O(l);△H=-57.3kJ/mol,则稀醋酸溶液与稀氢氧化钠溶液混合,中和热仍为57.3kJ/mol |
| D、由C(石墨)→C(金刚石):△H=+119kJ/mol可知,石墨比金刚石稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com