
【题目】Y是合成香料、医药、农药及染料的重要中间体,可由X在一定条件下合成,下列说法不正确的是( )

A.Y的分子式为C10H8O3
B.制备过程中发生的反应类型有消去反应、取代反应
C.由X制取Y的过程中可得到乙醇
D.等物质的量的X、Y分别与NaOH溶液反应,最多消耗NaOH的物质的量之比为3:2
【答案】D
【解析】
A.根据Y的结构式可以看出分子式为C10H8O3,A正确;
B.根据题意,由X制Y需要两步,化合物X(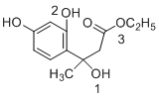 )中,1位置处的羟基在Y物质中消失,相应位置生成一条碳碳双键,故发生消去反应,X中2位置处的酚羟基与3位置处的酯基发生取代反应,形成Y物质相应位置的酯基,故两步反应中既有消去反应,又有取代反应,B正确;
)中,1位置处的羟基在Y物质中消失,相应位置生成一条碳碳双键,故发生消去反应,X中2位置处的酚羟基与3位置处的酯基发生取代反应,形成Y物质相应位置的酯基,故两步反应中既有消去反应,又有取代反应,B正确;
C.根据B的分析,X中2位置处的酚羟基与3位置处的酯基发生取代反应,生成乙醇,C正确;
D.等物质的量的X、Y分别与NaOH溶液反应,X物质有两个酚羟基,一个酯基,需要消耗3molNaOH,Y有一个酚羟基,一个酯基,但酯基水解后又会得到一个酚羟基,故总共也消耗3molNaOH,所以消耗NaOH的物质的量之比为1:1,D错误;
故选D。


科目:高中化学 来源: 题型:
【题目】富硼渣中含有镁硼酸盐(2MgO·B2O3)、镁硅酸盐(2MgO·SiO2)及少量Al2O3、FeO 等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H3BO3)晶体的一种工艺流程如下:
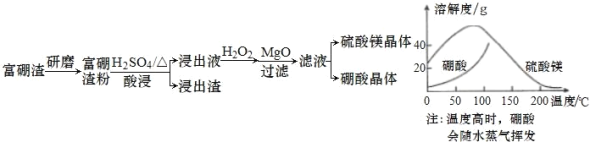
为了获得晶体,会先浓缩溶液接近饱和,然后将浓缩液放入高压釜中,控制温度进行结晶(硫酸镁与硼酸溶解度随温度的变化如图)。下列说法错误的是
A.该工艺流程中加快反应速率的措施有 2 种
B.在高压釜中,先降温结晶得到硼酸晶体,再蒸发结晶得到硫酸镁晶体
C.“酸浸”中镁硼酸盐发生反应2MgO·B2O3+2H2SO4+H2O![]() 2MgSO4+2H3BO3
2MgSO4+2H3BO3
D.加入“MgO”后过滤,所得滤渣主要是Al(OH)3 和Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
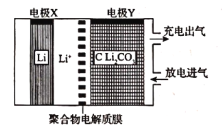
【题目】利用锂电池“固定![]() ”的电化学装置如图所示,在催化剂的作用下,该电化学装置放电时可将
”的电化学装置如图所示,在催化剂的作用下,该电化学装置放电时可将![]() 转化为
转化为![]() 和
和![]() ,充电时选用合适的催化剂,只有
,充电时选用合适的催化剂,只有![]() 发生氧化反应,释放出
发生氧化反应,释放出![]() 和
和![]() 。下列说法正确的是( )
。下列说法正确的是( )
A.该电池放电时,![]() 向电极
向电极![]() 方向移动
方向移动
B.该电池充电时,每转移![]() 的电子,理论上阳极产生
的电子,理论上阳极产生![]()
C.该电池放电时,每转移![]() 电子,理论上有
电子,理论上有![]() 参加反应
参加反应
D.该电池充电时,阳极电极反应式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三硫化磷(P4S3)是黄绿色针状晶体,易燃、有毒,分子结构之一如图所示,已知其燃烧时P被氧化为P4010,下列有关P4S3的说法中不正确的是

A. P4S3中磷元素为+3价
B. P4S3属于共价化合物
C. P4S3充分燃烧的化学方程式为P4S3+8O2=P4O10+3SO2
D. 1mol P4S3分子中含有9mol共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子的电子层结构,电子式为如图所示:下列说法正确的是( )
![]()
A.NH5属于离子化合物
B.NH5属于共价化合物
C.NH5只含有离子键
D.NH5只含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH1=+489.0 kJ·mol-1
C(石墨)+CO2(g)=2CO(g) ΔH2=+172.5 kJ·mol-1
则CO还原Fe2O3的热化学方程式为___________________________
(2)某实验将CO2和H2充入一定体积的密闭容器中,在两种不同温度条件下反应:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1
测得CH3OH的物质的量随时间变化如图所示,回答问题:
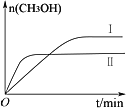
①该反应的平衡常数表达式K=_______________;
②曲线Ⅰ、Ⅱ对应的平衡常数大小关系为:KⅠ_________KⅡ(填“>”、“=”或“<”)。
③下列措施中能增大CO2转化率的是____________。(填序号)
A.升高温度 | B.充入He(g)使体系压强增大 |
C.将H2O(g)从体系中分离 | D.再充入一定量CO2 |
④下列图像正确且能表明在t时刻反应一定处于平衡状态的是__________。(填序号)
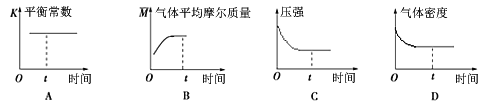
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】厌氧性硫酸盐还原菌(SRB)是导致金属微生物腐蚀最为普遍的菌种,腐蚀图解如图所示。下列说法正确的是( )
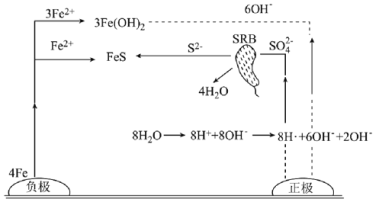
A.正极的电极反应式为8H++8e-=8H·(吸附)、SO42-+8H·(吸附)![]() S2-+4H2O
S2-+4H2O
B.正极区溶液的pH变小
C.生成1molFeS,转移6mol电子
D.若引入新细菌,一定会加速金属的腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有短周期主族元素X、Y、Z、R、T,R原子的最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Y与T同主族。五种元素原子半径与原子序数之间的关系如图所示。下列推断正确的是( )

A. 离子半径:Y<Z
B. 氢化物的沸点:Y<T
C. 最高价氧化物对应水化物的酸性:T<R
D. 由X、Y、Z、R四种元素组成的常见化合物中含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氧化铁样品中含有少量的硫酸亚铁。某同学要测定其中铁元素的质量分数,设计了如下实验方案。

(1)操作Ⅰ中配制溶液时,所用到的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管以外,还必须有__________(填仪器名称)。
(2)反应①中加入足量H2O2溶液,反应的离子方程式:_______________________________。
(3)检验沉淀中![]() 是否洗涤干净的操作是_______________________________________。
是否洗涤干净的操作是_______________________________________。
(4)将沉淀加热,冷却至室温,用天平称量坩埚与加热后固体的总质量为b1g,再次加热并冷却至室温称其质量为b2g,若b1-b2=0.3,还应进行的操作是_____________________。
(5)坩埚的质量为42.6 g,最终坩埚与加热后的固体的总质量为45.8 g,则样品中铁元素的质量分数为________________。
(6)有同学认为上述方案的实验步骤太繁琐,他认为,只要将样品溶于水充分搅拌,加热、蒸干、灼烧称量即可测得样品中铁元素的质量分数,你认为他的这个方案是否可行?__________(填“可行”或“不可行”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com