
【题目】热还原法制备MgO材料的原理为MgSO4(s)+CO(g)![]() MgO(s)+SO2(g)+CO2(g) △H>0,T℃时,在一恒容密闭容器中加入一定量的MgSO4(s)和CO(g),一段时间后达到平衡状态。下列说法正确的是( )
MgO(s)+SO2(g)+CO2(g) △H>0,T℃时,在一恒容密闭容器中加入一定量的MgSO4(s)和CO(g),一段时间后达到平衡状态。下列说法正确的是( )
A. 活化能:E正>E逆
B. 其他条件不变,加入催化剂,△H减小
C. 其他条件不变,降低温度,化学平衡常数增大
D. 其他条件不变,向容器中通入Ar(g),平衡逆向移动
 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
【题目】(1)在①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,⑦(NH4)2SO4,⑧乙醇中,由极性键形成的非极性分子有_______(填序号,以下同),含有金属离子的物质是__,分子间可形成氢键的物质是________,属于离子晶体的是__,属于原子晶体的是__,①~⑤五种物质的熔点由高到低的顺序是__。
(2)A,B,C,D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3500 ℃
试推断它们的晶体类型:A.__;B.__;C.__;D.__。
(3)下图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:A.__;B.__;C.__D.____。
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用该浓硫酸配制100 mL 1 mol/L的稀硫酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平。请回答下列问题:
(1)配制稀硫酸时,上述仪器中不需要使用的有__________(填序号),还缺少的仪器有____________________(写仪器名称);
(2)经计算,配制100mL1mol/L的稀硫酸需要用量筒量取上述浓硫酸的体积为____________________________________________mL(保留一位小数),量取浓硫酸时应选用_________(选填10mL、50mL 、100mL)规格的量筒;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化钾溶液常用作利尿剂及防治缺钾症的药物,某医疗实验小组需要用到480 mL物质的量浓度为0.5 mol·L-1的氯化钾溶液。回答下列问题:
(1)配制该溶液,需称量氯化钾晶体的质量是________。
(2)配制上述氯化钾溶液,需要使用的玻璃仪器是量筒、烧杯、玻璃棒、________、________。
(3)如图Ⅰ表示10 mL量筒中液面的位置,刻度A与B,B与C间均相差1 mL,如果刻度A为9,则量筒中液体的体积是________mL。

(4)定容时,某同学操作示意图如图Ⅱ所示,则其所配氯化钾溶液的浓度________(填“大于”“等于”或“小于”)0.5 mol·L-1;某同学由于操作不慎,定容时导致液面高于刻度线,他立即用胶头滴管将液体吸出,使液面恰好达到刻度线,请你评价该同学的做法:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)一年前8月我国自主研制的“海斗”号无人潜水器成功进行万米级下潜应用,这标志着我国研制无人潜水器能力已进入先进国家行列之中。

①无人潜水器耐压壳使用的是钛铝合金材料。下列不属于钛铝合金性质的是_______(填字母)。
a.密度大 b.硬度大 c.抗腐蚀
②无人潜水器通信传输系统中采用PC(聚碳酸酯)及PC合金板材,PC属于_______(填字母)。
a. 金属材料 b. 无机非金属材料 c. 有机高分子材料
③无人潜水器中的管道通常用塑胶为原料生产。塑胶主要含聚乙烯、聚丙烯、涤纶、聚酯、氯纶、聚氯乙烯等,聚丙烯属于______塑料(填“热固性”或“热塑性”)。
(2)营养平衡,合理用药是保证人体健康和生活质量的重要途径。
①人体必需从食物中获取多种营养元素和维生素。钙、铁、碘中不属于微量元素的是_____(填元素符号);新鲜蔬菜富含维生素C,蔬菜生吃比熟吃时维生素C的损失小,原因是____。
②人体摄入的油脂、蛋白质,都能在酶的催化作用下发生水解反应。油脂水解的最终产物是高级脂肪酸和_________(填名称);蛋白质完全水解的产物A中一定含有的官能团为-COOH和___________(用化学用语填空)。预测A不具有的化学性质为__________;
a.与氢氧化钠溶液反应 b.发生水解反应 c.发生成肽反应
③雾霾会刺激呼吸道,使人易患流行性感冒。治疗该病应该给病人服用______药品(填字母)。
a.麻黄碱 b.抗酸药 c.阿司匹林
④Mg2Si3O8·nH2O(三硅酸镁)具有治疗胃酸过多的作用,写出其与胃酸反应生成SiO2·H2O等物质的化学方程式_______
(3)“十三五”规划纲要明确提出,积极构建智慧能源系统,其中控制传统能源的生产和合理使用尤为重要。
①往燃煤中加入____可减少烟气中的SO2的含量,燃煤产生的SO2用NH3处理可生产多种化工产品。用氨水吸收SO2可制得亚硫酸氢铵(NH4HSO3)写出该反应的化学方程式_______
②天然水中杂质较多,常需要加入明矾,ClO2等物质处理后才能饮用。加入ClO2的作用是____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各步制取物质,最终无法达到目的的有
A. Al![]() Al2O3
Al2O3![]() Al(NO3)3
Al(NO3)3![]() Al(NO3)3晶体
Al(NO3)3晶体
B. Cu![]() CuO
CuO![]() CuSO4溶液
CuSO4溶液![]() CuSO4·5H2O
CuSO4·5H2O
C. Fe![]() FeCl3
FeCl3![]() Fe(OH)3
Fe(OH)3![]() Fe2O3
Fe2O3
D. CuSO4溶液![]() CuS
CuS![]() CuS
CuS
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼及其化合物在工农业生产中具有广泛应用。
请回答下列问题:
(1)基态B原子的价电子排布图___,B属于元素周期表中的___区元素。
(2)NaBO2可用于织物漂白。
①第二周期中第一电离能介于B和O之间的元素为___(填元素符号)。
②BO2-的空间构型为____,写出两种与其互为等电子体的分子的化学式:____。
(3)BF3和F-可以形成BF4-,BF3和BF4-中B原子的杂化方式分别为_____、____。
(4)立方BN和立方AlN均为原子晶体,结构相似,BN的熔点高于AlN的原因为______。
(5)一种新型轻质储氢材料的晶胞结构如图所示:
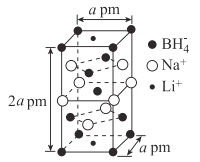
①该化合物的化学式为____。
②设阿伏加德罗常数的值为NA,该晶体的密度为___g·cm-3(用含a、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在 2 L 密闭容器中,A、B、C 三种气体的物质的量随时间变化的曲线如图所示。下列说法正确的是( )
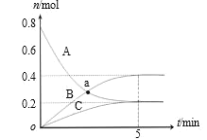
A.反应开始到 5min,υ(C)=0.2 mol/(L·min)
B.反应开始到 5min,B 的物质的量浓度增加了 0.4 mol/L
C.反应的化学方程式为:2B(g)+C(g)![]() 3A(g)
3A(g)
D.a 点时,c(A)=c(B)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的资源,下图为海水资源利用的部分过程。
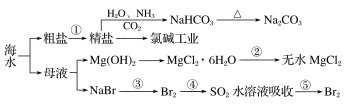
下列有关说法正确的是
A.工业上通过电解饱和MgCl2溶液制取金属镁
B.含氮、磷的大量废水排入海洋,易引发赤潮
C.反应④的离子方程式为:Br2+SO2+2H2O=2HBr+2H++ SO42-
D.在第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入药品的顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com