
����Ŀ����1��һ��ǰ8���ҹ��������Ƶ���������������DZˮ���ɹ�����������DZӦ�ã����־���ҹ���������DZˮ�������ѽ����Ƚ���������֮�С�

������DZˮ����ѹ��ʹ�õ��������Ͻ���ϡ����в����������Ͻ����ʵ���_______������ĸ����
a���ܶȴ� b��Ӳ�ȴ� c������ʴ
������DZˮ��ͨ�Ŵ���ϵͳ�в���PC(��̼����)��PC�Ͻ��ģ�PC����_______(����ĸ)��
a. �������ϡ���������b. ���ǽ������ϡ���������c. �л��߷��Ӳ���
������DZˮ���еĹܵ�ͨ�����ܽ�Ϊԭ���������ܽ���Ҫ������ϩ���۱�ϩ�����ڡ����������ڡ�������ϩ�ȣ��۱�ϩ����______���ϣ������ȹ���������������������
��2��Ӫ��ƽ�⣬������ҩ�DZ�֤���彡����������������Ҫ;����
����������ʳ���л�ȡ����Ӫ��Ԫ�غ�ά���ء��ơ��������в�������Ԫ�ص���_____����Ԫ�ط��ţ��������߲˸���ά����C���߲����Ա����ʱά����C����ʧС��ԭ����____��
�������������֬�������ʣ�������ø�Ĵ������·���ˮ�ⷴӦ����֬ˮ������ղ����Ǹ�֬�����_________�������ƣ�����������ȫˮ��IJ���A��һ�����еĹ�����Ϊ��COOH��___________���û�ѧ������գ���Ԥ��A�����еĻ�ѧ����Ϊ__________��
a��������������Һ��Ӧ b������ˮ�ⷴӦ c���������ķ�Ӧ
��������̼���������ʹ���������Ը�ð�����Ƹò�Ӧ�ø����˷���______ҩƷ������ĸ����
a����Ƽ� b������ҩ c����˾ƥ��
��Mg2Si3O8��nH2O(������þ)��������θ������������д������θ�ᷴӦ����SiO2��H2O�����ʵĻ�ѧ����ʽ_______
��3����ʮ�������滮��Ҫ��ȷ��������������ǻ���Դϵͳ�����п��ƴ�ͳ��Դ�������ͺ���ʹ����Ϊ��Ҫ��
����ȼú�м���____�ɼ��������е�SO2�ĺ�����ȼú������SO2��NH3�������������ֻ�����Ʒ���ð�ˮ����SO2���Ƶ���������泥�NH4HSO3��д���÷�Ӧ�Ļ�ѧ����ʽ_______
����Ȼˮ�����ʽ϶࣬����Ҫ����������ClO2�����ʴ�����������á�����ClO2��������____
���𰸡�a c ������ Ca ά����C����ʱ�ױ����� ����������� -NH2 b c Mg2Si3O8��nH2O��4HCl=2MgCl2��3 SiO2��H2O��(n��1)H2O ��ʯ�һ�ʯ��ʯ��CaCO3�� NH3+SO2+H2O=NH4HSO3 ����ɱ��
��������
��1���ٸ��ݺϽ�����ʷ������
�ڸ��ݲ��ϵķ�����з�����
�۸��ݲ��ϵ����ʽ��з�����
��2���������е���Ԫ����Ҫ�������ܡ�ͭ��п�������̡��⡢�����⡢���ȣ�ά����C�ױ�����������������
����֬��ø�Ĵ������·���ˮ�ⷴӦ���ɸ�֬����ͱ����������ͣ�����������ø�Ĵ������·���ˮ�ⷴӦ���ɰ����
�۸�ð����ʱӦ�������ס�ֹ�ȵ�ҩ�
��Mg2Si3O8��nH2O��θ���е����ᷴӦ����MgCl2��SiO2��H2O��ˮ��
��3����ú�к�����ȼ��ʱ�����ɶ��������������ܺ������Ʒ�Ӧ��
��ClO2����ǿ�����ԣ��ܽ�����������ɱ��������
��1���������Ͻ����ʵ���Ӳ�ȴ���ʴ���ܶ�С���ʴ�Ϊ��a��
��PC�Ǿ�̼�����ļ�ƣ�PC������һ��ǿ�͵���������֬���������ǿ��ǿ�Ⱥ����Ժܺã������л��߷��Ӳ��ϣ��ʴ�Ϊ��c��
���۱�ϩ���ɱ�ϩ�ۺ϶��Ƶõ�һ����������֬���ʴ�Ϊ����������
��2���������еij���Ԫ����Ҫ������̼���⡢�����ơ��ס��ء����ơ��ȡ�þ����Ԫ����Ҫ�������ܡ�ͭ��п�������̡��⡢�����⡢���ȣ����Բ�������Ԫ�ص��Ǹƣ�ά����C�ױ������������������߲����Ա����ʱά����C����ʧС���ʴ�Ϊ��Ca��ά����C����ʱ�ױ�������
����֬��ø�Ĵ������·���ˮ�ⷴӦ���ɸ�֬����ͱ����������ͣ�����������ø�Ĵ������·���ˮ�ⷴӦ���ɰ����ᣬ������Ĺ�����Ϊ�Ȼ��Ͱ�����������������ԣ��ܹ�����ͼӦ���ܹ��������ķ�Ӧ���ɶ��ĺ͵����ʣ��ʴ�Ϊ�������������ͣ���-NH2��b��
�۸�ð����ʱӦ�������ס�ֹ�ȵ�ҩ���ҩ��Ϊ��˾ƥ�֣��ʴ�Ϊ��c��
��Mg2Si3O8��nH2O��θ���е����ᷴӦ����MgCl2��SiO2��H2O��ˮ����Ӧ�Ļ�ѧ����ʽΪ
Mg2Si3O8��nH2O��4HCl=2MgCl2��3 SiO2��H2O��(n��1)H2O���ʴ�Ϊ�� Mg2Si3O8��nH2O��4HCl=2MgCl2��3 SiO2��H2O��(n��1)H2O��
��3����úȼ�չ����������ɶ��������������ж�������Ⱦ�������������ܹ������ɵĶ�������Ӧ���Ӷ���ֹ����������Ⱦ��������ȼú�м�����ʯ�һ�̼��Ƽ��������е�SO2�ĺ�������ˮ�������SO2��Ӧ������������泥���Ӧ�Ļ�ѧ����ʽΪNH3+SO2+H2O=NH4HSO3���ʴ�Ϊ��ʯ��ʯ��CaCO3������ʯ�ң�CaO����NH3+SO2+H2O=NH4HSO3��
��ClO2����ǿ�����ԣ��������ڵ����ʣ�ǿ������ClO2�ܽ�����������ʹ�������ԣ��Ӷ���ɱ�����������ã��ʴ�Ϊ��ɱ��������


 53���ò�ϵ�д�
53���ò�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ:NO2(g) + SO2(g)![]() SO3(g) + NO(g) ����ʼʱ��ij�ܱ�������ͨ��1 mol NO2 �� 2 mol S18O2��.��Ӧ�ﵽƽ��������й�˵����ȷ����:
SO3(g) + NO(g) ����ʼʱ��ij�ܱ�������ͨ��1 mol NO2 �� 2 mol S18O2��.��Ӧ�ﵽƽ��������й�˵����ȷ����:
A.NO2�в����ܺ�18OB.��1 mol N18O����
C.S18O2�����ʵ���������Ϊ0. 8 molD.SO2��SO3��NO��NO2����18Oʱ��˵���÷�Ӧ�ﵽƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʫ�䡢������뻯ѧ�����йأ�˵������ȷ����
A. ��ˮ�齻�ڣ����Ͻ�����ǰ�߰��������仯�������߰�����ѧ�仯
B. �������з�ź������϶������˻�ѧ�仯
C. ����ˮʯ��������ľ������������ѧ�仯
D. �����Ʒ�ƽ�˾���ʵ����ӿ����������������ܽ�ƽ���״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ���ʼ�ֻ������Ԫ�أ�Ϊ̽�����ʼ���ɺ����ʣ���Ʋ��������ʵ�顣������̬�⻯�����ڱ���µ��ܶ�Ϊ 1.518 g��L-1����������ͬԪ�صĻ��ϼ���ͬ��
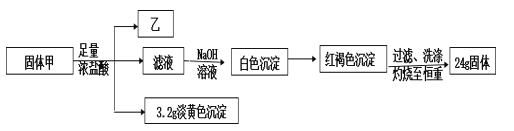
��1�������Ԫ��_____________��
��2��д����������Ũ���ᷴӦ�����ӷ���ʽ______________��
��3���������ڹ��������г��ȼ�պ��ٽ��������ͨ��BaCl2��Һ�����ְ�ɫ������д���ù������ܷ�Ӧ�����ӷ���ʽ_________________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ڵ綯��������������ȼ�ϵ�أ�ͨ����NaCl��Һ��NaOH��ҺΪ���Һ�����Ͻ�Ϊ�����������缫Ϊ��������֪����ص������۱�������ָ��λ�����ĵ缫�������������ͷų��������ܡ�����˵����ȷ����
A.�Ƚ��ơ�þ�������ֽ���������أ�Na-������ص����۱��������
B.��NaOH��ҺΪ���Һʱ��������ӦΪAl��3OH����3e��=Al(OH)3��
C.��NaOH��ҺΪ���Һʱ������ڹ��������е��Һ�ļ��Ա��ֲ���
D.��NaCl��Һ��NaOH��ҺΪ���Һʱ��������Ӧ��ΪO2��2H2O��4e��=4OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ�ԭ���Ʊ�MgO���ϵ�ԭ��ΪMgSO4��s��+CO��g��![]() MgO��s��+SO2��g��+CO2��g�� ��H>0��T��ʱ����һ�����ܱ������м���һ������MgSO4��s����CO��g����һ��ʱ���ﵽƽ��״̬������˵����ȷ���ǣ� ��
MgO��s��+SO2��g��+CO2��g�� ��H>0��T��ʱ����һ�����ܱ������м���һ������MgSO4��s����CO��g����һ��ʱ���ﵽƽ��״̬������˵����ȷ���ǣ� ��
A. ��ܣ�E��>E��
B. �����������䣬�����������H��С
C. �����������䣬�����¶ȣ���ѧƽ�ⳣ������
D. �����������䣬��������ͨ��Ar��g����ƽ�������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����Ũ��Ϊ0.01mol��L-1��HA��Һ�ζ�20mLŨ��Ϊ0.01mol��L-1��NaOH��Һ���ζ�������ͼ��ʾ������˵���������ǣ� ��

A. Ӧѡ�÷�̪��ָʾ��
B. M����Һ�д��ڣ�c��Na+��>c��A-��
C. Ka��HA����2��10-8
D. N����Һ�д��ڣ�c��OH-��-c��H+��=c��HA��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ���±���������ݣ����㡢�������жϸ������ۣ���Ŀ�������ݺ�������Ϊ�����£�
NH3H2O | Kb=1.8��10-5 |
H2CO3 | Ka1=4.4��10-7 Ka2=4.7��10-11 |
HF | Ka=6.8��10-4 |
H2S | Ka1=1.3��10-7 Ka2=7.1��10-15 |
H2O | Kw=10-14 |
Cu(OH)2 | Ksp=2.2��10-20 |
Fe(OH)3 | Ksp=4.0��10-38 |
CuS | Ksp=6.3��10-36 |
FeS | Ksp=3.6��10-18 |
���ö��� | lg2=0.3 lg2.2=0.34 lg3=0.48 |
��1��NH4F ��Һ��____�ԣ��������ҺӦ�÷���__________�С�
��2��NH4HCO3 ��Һ������ NaOH ��Һ��Ӧʱ��_____ (�����ӷ���)���� NaOH ��Һ�е� OH-��Ӧ��
��3����Fe3+��Cu2+��Ϊ0.1mol/L����Һ�м���ij�����pH=___ʱ��Fe3+��ȫ��������pH=_____ʱ��Cu2+��ʼ������
��4����Ӧ CuS(s) + H2SO4(aq)![]() H2S(aq) + CuSO4��aq���� K= _____________����Ӧ FeS(s) + H2SO4(aq)
H2S(aq) + CuSO4��aq���� K= _____________����Ӧ FeS(s) + H2SO4(aq) ![]() H2S(aq) + FeSO4 (aq)�� K=___________����Ӧ CuS(s)+Fe2+(aq)
H2S(aq) + FeSO4 (aq)�� K=___________����Ӧ CuS(s)+Fe2+(aq)![]() FeS(s)+Cu2+(aq)�� K=_______
FeS(s)+Cu2+(aq)�� K=_______
�ɼ���������֪����ʵ�����Ʊ�H2S����Ӧѡ��_________������H2S����Ӧѡ��_________������������Ӧ�е�������������
��ȥ��ˮ�е� Cu2+ʹ�� ������ FeS ������ŵ�����
a�����Գ�ȥ��ˮ�е� Cu2+�������� FeS �����ɵ� CuS ����ͨ������һ����ȥ
b��____________________________________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������H�ĺϳ�·����ͼ��
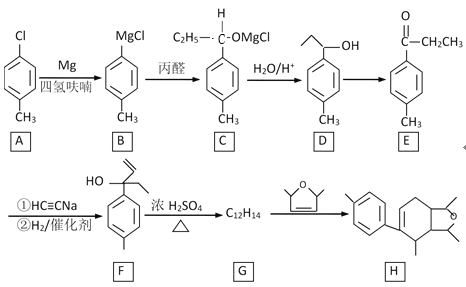
��֪CH��CH��NaNH2Һ�������¿�����CH��CNa��NaC��CNa��
(1)A�Ļ�ѧ������________��B��C�ķ�Ӧ������__________��
(2)D��E�ķ�Ӧ�Լ���������_______��F��������������������_______��
(3)H�ķ���ʽ��________��
(4)F��G�Ļ�ѧ����ʽ��_________��
(5)W��E��ͬϵ���E��һ��̼ԭ�ӣ����������������W��ͬ���칹��Ľṹ��ʽ��________��дһ�֣���
�������ֹ�����
����FeCl3��Һ����ɫ
�ۺ˴Ź�������������壬�����֮����3�U2�U2�U2�U1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com