
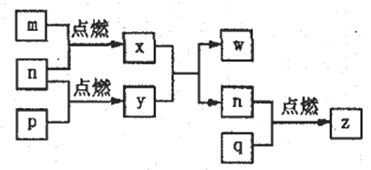
����Ŀ������������Ԫ��a��b��c��d��ԭ����������������������Ԫ���γɵĵ�������Ϊm��n��p��q��x��y��z������ЩԪ����ɵĶ�Ԫ������������zΪ�γ��������Ҫ����֮һ��25��ʱ��0.01mol��L-lw��Һ����![]() =1.0��10-10���������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ����
=1.0��10-10���������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ����
A. ԭ�Ӱ뾶�Ĵ�С��a<b<c<d
B. ���⻯��ķе���b>d
C. y�ĵ���ʽ��![]()
D. y��w���еĻ�ѧ��������ȫ��ͬ
���𰸡�B
��������������������֪��aΪH��bΪO��cΪNa��dΪS��m��n��p��q�ֱ���H2,O2��Na��S��x��y�ֱ���H2O��Na2O2��w��NaOH��z��SO2��A�����Ӳ�Խ�࣬���Ӱ뾶Խ������ͬ�����Ų���������ԭ������������Ӱ뾶С�������Ӱ뾶�Ĵ�С��a<c<b<d����A����B��ˮ���Ӽ京�������b�⻯��ķе������������Ԫ���⻯��ķе㣬��B��ȷ��C��y��Na2O2��Ӧ��������Na+��O22-��ɣ���C����D��yΪNa2O2�������Ӽ���O-O�Ǽ��Լ���wΪNaOH�������Ӽ���O-H���Թ��ۼ�����D����ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E����ԭ���������������ǰ������Ԫ�أ�����A��CΪͬһ���壬C�����������뵼�������ͼ��ɵ�·��B�ļ��⻯���ˮ��Һ�ʼ��ԣ�EԪ�ص����������ӵ�3d�Dz�Ϊ�������D����Ϊ��δ�����������������ᡢǿ�ȸߡ���ʴ���������ڱ���λ�ڵ�4���ڡ��ڢ�B�塣
��1��A��B��C����Ԫ�صĵ�һ��������С�����˳��Ϊ______________________���縺����С�����˳��Ϊ____________________��
��2��B�ļ��⻯����Һ����ԭ����_______________��BH4+��Bԭ�ӵ��ӻ���ʽΪ___________���ռ乹��Ϊ__________________��
��3��EԪ�ػ�̬ԭ�ӵĵ����Ų�ʽΪ____________________________________��
��4��B��C�γɵĻ����ﳣ���������ͻ���ϣ���ѧ�����ȶ����ݴ��Ʋ���Ӧ����__________________���塣
��5��D�ж������������һ��������ľ����ṹ��ͼ1��ʾ����þ�����D����λ��Ϊ__________________��ͼ2ΪE��һ���������������ṹ���������ı߳�Ϊacm��NA��ʾ�����ӵ�������ֵ����E���ܶ�Ϊ__________________g��cm-3(�ú�a��NA�Ĵ���ʽ��ʾ)��
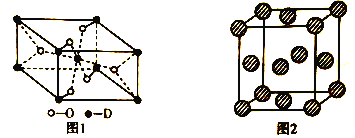
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ϡ��Һ�У��������кͷ�Ӧ����1 molˮʱ�ķ�Ӧ�Ƚ����к��ȡ���������ͼװ�ý����к��ȵIJⶨ����ش��������⣺

��1��ͼʾװ����������Ҫ��ɲ���δ������������____________ ��_______________��
��2���ձ�����������ĭ���ϵ������� ________________��
��3��������ʱ�ּ���ע�뷴ӦҺ����õķ�Ӧ����ֵ_____������ƫ������ƫС��������Ӱ��������
��4����һ���������к��Ȳⶨʵ�飬�¶ȼ���ʹ��__________�Ρ�
��5����ȡ0.5 mol/L�������0.55 mol/L��NaOH��Һ��50 mL����ʵ�飬��������NaOH��Һ��ʼƽ���¶�Ϊt1������Ϸ�Ӧ������¶�Ϊt2��������Һ�ܶȾ�Ϊ1 g/mL��������Һ�ı�����c= 4.18 J/(g��)������ʽ�����к��ȣ���H= ______________kJ/mol�����û���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڽ������������ȷ���ǣ�������
A.����������������ɢϵ�ı��������Ƿ�ɢ�ʵ���ֱ����1��100nm֮��
B.����������ʱ�������пɷ��������ЧӦ
C.Fe(OH)3�����ܹ�����ˮ�������Ĺ���������������ﵽ��ˮĿ��
D.�þ۹��ֵ�Ͳ����NaCl��Һ��Fe(OH)3����ʱ��������������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�С�鷢��һ�ֻ�������һ�������Ĺ������·����ֽⷴӦ����Ӧ��Ũ���淴Ӧʱ��仯��ͼ��ʾ����Ӧ10minʱ��Ӧ���Ũ�Ⱥͷ�Ӧ4min-8min���ƽ����Ӧ���������Ӧ��
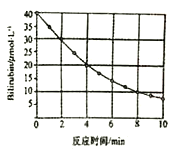
A. 7.5mol/L��2.5mol/(L��min) B. 7.5��mol/L��2.5umol/(L��min)
C. 0.75umol/L��3.0u(L��min) D. 0.75mol/L��5.0umol/(L��min)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����Ԫ�ص�ԭ�����������Ų���5s1������������ȷ����
A. �䵥�ʳ����¸�ˮ��Ӧ�����ƾ��� B. ��ԭ�Ӱ뾶�ȼ�ԭ�Ӱ뾶С
C. ��̼����������ˮ D. ���������ﲻ��ʹ���������ܽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ����һ��2L���ܱ������У�X��Y��Z�����������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ������,����д�¿հ�:
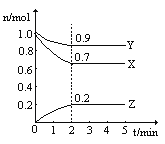
(1)�÷�Ӧ�Ļ�ѧ����ʽΪ__________��
(2)ƽ��ʱ��X��ת����Ϊ_______,Y��Ũ��Ϊ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦN2 (g) + 3H2(g) ![]() 2NH3(g)��2 min��N2Ũ�ȼ�����0.6 mol�qL��1���Դ˷�Ӧ���ʵ�������ȷ����( )
2NH3(g)��2 min��N2Ũ�ȼ�����0.6 mol�qL��1���Դ˷�Ӧ���ʵ�������ȷ����( )
A. 2min��H2�ķ�Ӧ������0.4 mol��(L�qmin)
B. 2 min��N2��H2��NH3�ķ�Ӧ����֮����1�s2�s3
C. ��2min�ڣ�N2�ķ�Ӧ������0.3 mol��(L�qmin)
D. ��2minĩNH3�ķ�Ӧ������0.2 mol��(L�qmin)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������ȤС������ͼװ�ý���ʵ�飬�Իش�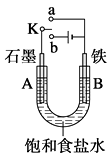
��1������ʼʱ����K��a���ӣ���A�缫��ӦʽΪ��
��2������ʼʱ����K��b���ӣ����ַ����������ڽ����ķ��������ַ�����ʩ���� �� ��A�缫��ӦʽΪ;B�缫��ӦʽΪ��
��3������K��b���ӣ�������ʳ��ˮ����CuSO4��Һ����A�缫��ӦʽΪ �� �÷�Ӧ�����ӷ���ʽΪ �����һ��ʱ�����Һ��ȻΪ��ɫ������Һ��pHֵ������������С���������䡱���������������Һ�ָ���ԭ״��Ӧ���� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com