
【题目】物质的量浓度之比为3:2:1的NaCl、MgCl2、AlCl3三种溶液,当他们的体积相同时,三种溶液中Cl-离子的物质的量浓度之比是( )
A.3:4:3B.1:2:3C.3:2:1D.1:1:1
科目:高中化学 来源: 题型:
【题目】氮的单质及其化合物性质多样,用途广泛. 完成下列填空.
(1)科学家正在研究利用催化技术将超音速飞机尾气中的NO和CO转变成CO2和N2:2NO+2CO ![]() 2CO2+N2+Q(Q>0) 某温度下测得该反应在不同时间的CO浓度如表:
2CO2+N2+Q(Q>0) 某温度下测得该反应在不同时间的CO浓度如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(CO) | 3.60×10﹣3 | 3.05×10﹣3 | 2.85×10﹣3 | 2.75×10﹣3 | 2.70×10﹣3 | 2.70×10﹣3 |
该反应平衡常数K的表达式为;温度升高,K值(选填“增大”、“减小”、“不变”);前2s内的平均反应速率v(N2)=;若上述反应在密闭容器中发生,达到平衡时能提高NO转化率的措施之一是 .
(2)工业合成氨的反应温度选择500℃左右的原因是 .
(3)实验室在固定容积的密闭容器中加入1mol氮气和3mol氢气模拟工业合成氨,反应在一定条件下已达到平衡的标志是 . a.N2、H2、NH3的浓度之比为1:3:2
b.容器内的压强保持不变
c.N2、H2、NH3的浓度不再发生变化
d.反应停止,正、逆反应的速率都等于零
(4)常温下向含1mol溶质的稀盐酸中缓缓通入1mol NH3(溶液体积变化忽略不计),反应结束后溶液中离子浓度由大到小的顺序是;在通入NH3的过程中溶液的导电能力(选填“变大”、“变小”、“几乎不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某金属氯化物MCl2质量为m克,含有0.4molCl-,则金属M的摩尔质量可表示为( )
A. (m+71) g/mol B. 5m g/mol C. (5m-71) g/mol D. (5m-35.5) g/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是 ( )
A. 电离时能产生的阳离子是氢离子的化合物一定是酸
B. 所有盐电离时一定产生酸根阴离子和金属阳离子
C. 酸性氧化物是指能与水反应生成酸的化合物,如CO2、SO3
D. 碱性氧化物一定是金属氧化物,但金属氧化物不一定是碱性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置能达到实验目的是(夹持仪器未画出)( )
A. 装置用于检验溴丙烷消去产物
装置用于检验溴丙烷消去产物
B. 装置用于石油的分馏
装置用于石油的分馏
C. 装置用于实验室制硝基苯
装置用于实验室制硝基苯
D. 装置可装置证明酸性:盐酸>碳酸>苯酚
装置可装置证明酸性:盐酸>碳酸>苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL 0.3 mol· L-1的NaOH溶液中缓慢通入一定量CO2,充分反应后得到溶液A。
(1)若溶液A中的溶质是单一成分,溶质可能是_________________________。
(2)若向溶液A中逐滴加入c mol L_1的盐酸,充分反应后得溶液B,反应过程中 产生二氧化碳(不考虑溶解于水)的体积(标准状况下)与所加盐酸的体积关系如图 所示:

①写出滴加“0~100mL”盐酸过程中发生反应的离子方程式____________________。
②判断溶液A中的溶质并计算其物质的量_____________________。
③盐酸的物质的量浓度c =________ mol L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨氮废水中的氮元素多以NH4+和NH3H2O的形式存在.某工厂处理氨氮废水的流程如下: 含NH4+的废水 ![]() 低浓度氨氮废水
低浓度氨氮废水 ![]() 含余氯废水
含余氯废水 ![]() 达标废水
达标废水
(1)I中加入NaOH溶液,调pH=11并鼓入大量空气.用离子方程式表示加NaOH溶液的作用是;鼓入大量空气的目的是 .
(2)II中加入适量NaClO溶液,控制pH在6~7,将氨氮转化为无毒物质. ①为了完全从废水中去除氨氮,加入的NaClO与水体中NH4+的物质的量之比最小是 .
②过程 II发生3个反应:
i.ClO﹣+H+═HClO
ii.NH4++HClO═NH2Cl+H++H2O (NH2Cl中Cl元素为+1价)
iii. …
已知:水体中以+1价形式存在的氯元素有消毒杀菌的作用,被称为“余氯”.图为NaClO加入量与“余氯”含量的关系示意图.其中氨氮含量最低的点是c点.
b点表示的溶液中氮元素的主要存在形式是(用化学式表示);反应iii的化学方程式是 . 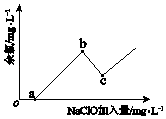
(3)III中用Na2SO3溶液处理含余氯废水,要求达标废水中剩余Na2SO3的含量小于5mgL﹣1 . 若含余氯废水中NaClO的含量是7.45mgL﹣1 , 则处理10m3含余氯废水,至多添加10% Na2SO3溶液kg(溶液体积变化忽略不计).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中乙是甲的电解池进行电解时的某个量(纵坐标x)随时间变化的曲线(各电解池都用石墨作电极,不考虑电解过程中溶液浓度变化对电极反应的影响),则x表示( ) 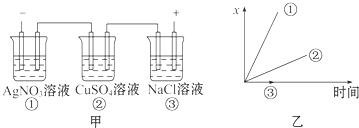
A.各电解池析出气体体积总数的变化
B.各电解池阳极质量的增加
C.各电解池阴极质量的增加
D.各电极上放电的离子总数的变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com