
����Ŀ��������ˮ�еĵ�Ԫ�ض���NH4+��NH3H2O����ʽ���ڣ�ij��������������ˮ���������£� ��NH4+�ķ�ˮ ![]() ��Ũ�Ȱ�����ˮ
��Ũ�Ȱ�����ˮ ![]() �����ȷ�ˮ
�����ȷ�ˮ ![]() ����ˮ
����ˮ
��1��I�м���NaOH��Һ����pH=11��������������������ӷ���ʽ��ʾ��NaOH��Һ�����������������������Ŀ���� ��
��2��II�м�������NaClO��Һ������pH��6��7��������ת��Ϊ�����ʣ� ��Ϊ����ȫ�ӷ�ˮ��ȥ�������������NaClO��ˮ����NH4+�����ʵ���֮����С�� ��
�ڹ��� II����3����Ӧ��
i��ClO��+H+�THClO
ii��NH4++HClO�TNH2Cl+H++H2O ��NH2Cl��ClԪ��Ϊ+1�ۣ�
iii�� ��
��֪��ˮ������+1����ʽ���ڵ���Ԫ��������ɱ�������ã�����Ϊ�����ȡ���ͼΪNaClO�������롰���ȡ������Ĺ�ϵʾ��ͼ�����а���������͵ĵ���c�㣮
b���ʾ����Һ�е�Ԫ�ص���Ҫ������ʽ�ǣ��û�ѧʽ��ʾ������Ӧiii�Ļ�ѧ����ʽ�� �� 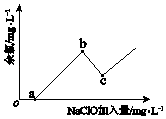
��3��III����Na2SO3��Һ���������ȷ�ˮ��Ҫ�����ˮ��ʣ��Na2SO3�ĺ���С��5mgL��1 �� �������ȷ�ˮ��NaClO�ĺ�����7.45mgL��1 �� ����10m3�����ȷ�ˮ����������10% Na2SO3��Һkg����Һ����仯���Բ��ƣ���
���𰸡�
��1��NH4++OH���TNH3?H2O���������Խ����ɵİ�������,ʹ��ѧƽ��������Ӧ�����ƶ�,�ٽ��˰�ˮ����
��2��3��1�� NH2Cl�� ClO��+2NH2Cl=N2+3Cl��+2H++H2O
��3��1.76
���������⣺��1������ܺ�ǿ�Ӧ��ʵ���ǣ�NH4++OH���TNH3H2O����ˮ�����ǿ��淴Ӧ������������������ɵİ������ߣ����������������ʹ��ѧƽ��������Ӧ�����ƶ�������������ɰ���������ٽ��˰�ˮ���룬
���Դ��ǣ�NH4++OH���TNH3H2O���������Խ����ɵİ������ߣ�ʹ��ѧƽ��������Ӧ�����ƶ����ٽ��˰�ˮ���룻��2���ٰ�����ˮ�еĵ�Ԫ�ض���NH4+��NH3H2O����ʽ���ڣ�Ϊ����ȫ�ӷ�ˮ��ȥ��������
2NH4+��N2��12e��
6ClO����6Cl����12e��
���ݵ����غ�õ������NaClO��ˮ����NH4+�����ʵ���֮��3��1��
���Դ��ǣ�3��1������a��b�㣬�����ķ�ӦΪi��ClO��+H+�THClO
ii��NH4++HClO�TNH2Cl+H++H2O ��NH2Cl��ClԪ��Ϊ+1�ۣ���b���ʾ����Һ�е�Ԫ�ص���Ҫ������ʽ��NH2Cl��
b��c�㷴Ӧ�Ǵ������ƺ�NH2Cl����������ԭ��Ӧ���ɵ�������Ӧ�����ӷ���ʽΪ��ClO��+2NH2Cl=N2+3Cl��+2H++H2O��
���Դ��ǣ�NH2Cl��ClO��+2NH2Cl=N2+3Cl��+2H++H2O����3������10m3��ˮb�к���NaClO�����ʵ���Ϊn= ![]() =1mol
=1mol
���ݷ�Ӧ��NaClO+Na2SO3�TNaCl+Na2SO4����֪��NaClO��ȫ��Ӧ���ĵ�Na2SO3Ϊ1mol��
����Ϊm=n��M=1mol��126g/mol=126g��
�������⣬���������10%Na2SO3��Һ������Ϊx
![]() =5mg/L��
=5mg/L��
��ã�x=1760g=1.76kg��
���Դ��ǣ�1.76��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȷ��ʾ���л�ѧ��Ӧ�����ӷ���ʽ���ǣ� ��
A. ��Ƭ����ϡ������Һ�� Fe + 2H+ = Fe3+ + H2��
B. ̼����������������� CO32-��2H+��CO2��H2O
C. ʯ������������Һ��Ӧ H++OH-=H2O
D. ��������ϡ����ķ�Ӧ CaO��2H+ �� Ca2++H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ���Ũ��֮��Ϊ3:2:1��NaCl��MgCl2��AlCl3������Һ�������ǵ������ͬʱ��������Һ��Cl-���ӵ����ʵ���Ũ��֮���ǣ� ��
A.3��4��3B.1��2��3C.3��2��1D.1��1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʲ������Ҵ�����������Ӧ���ǣ� ��
A.CH3COOH
B.HNO3
C.C17H35COOH
D.CH3OH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ȫ��Һ����أ�VO2++V2++2H+ ![]() VO2++H2O+V3+ �� �ڿ����е��ˮ�����������£��ķ����������Ƶó����������Ƶù������⣬����ܷ���ʽΪ3H2O+3O2�T3H2O2+O3 �� ����H2O2ֻΪ��ԭ�������˵����ȷ���ǣ� ��
VO2++H2O+V3+ �� �ڿ����е��ˮ�����������£��ķ����������Ƶó����������Ƶù������⣬����ܷ���ʽΪ3H2O+3O2�T3H2O2+O3 �� ����H2O2ֻΪ��ԭ�������˵����ȷ���ǣ� ��
A.ԭ��طŵ�ʱ������ӦΪVO2++2H++e���TVO2++H2O
B.���ʱ������ӦΪV2+��e���TV3+
C.���ص�������ӦʽΪ3O2+6H2O+6e���T3H2O2+6OH��
D.����������22.4 L O3����״����ʱ��ת��3 mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������˵����ȷ����
A. ��״���£�11.2L N2O4��NO2�Ļ����������������ԭ����ΪNA
B. lmol Na ������O2��Ӧ������Na2O��Na2O2�Ļ���ת�Ƶĵ�����ΪNA
C. ��FeI2��Һ��ͨ������Cl2������lmolFe2+������ʱ����ת�Ƶĵ�����ĿΪNA
D. �����£�0.2mol Fe������ˮ������Ӧ������H2������ĿΪ0.3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.2mol AgNO3��0.4mol Cu��NO3��2��0.6mol KCl����ˮ�����100mL��Һ���ö��Ե缫���һ��ʱ�������һ������0.3mol Cu����ʱ����һ���ϲ����������������״����Ϊ�� ��
A.3.36 L
B.4.48 L
C.5.6 L
D.6.72 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ����֤�������ʵ���ʵ�飬a��b��d��e�ǽ��������Һ����ֽ����KMnO4����μ�һ��Ũ�������������һ������������档��֪��2KMnO4��16HCl�D��2KCl��5Cl2����2MnCl2��8H2O
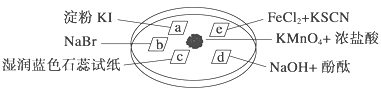
��ʵ������������ͻ��������ȷ���� (����)
ѡ�� | ʵ������ | ���ͻ���� |
A | a��������b�������ɫ | �����ԣ�Cl2>Br2>I2 |
B | c���ȱ�죬����ɫ | ������ˮ�������������� |
C | d��������ɫ | ������ˮ������Ư�������� |
D | e�����ɫ | ��ԭ�ԣ�Fe2��>Cl�� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com