
【题目】工业上常用亚硝酸钠![]() 作媒染剂、漂白剂、钢材缓蚀剂、金属热处理剂。某兴趣小组用下列装置制备
作媒染剂、漂白剂、钢材缓蚀剂、金属热处理剂。某兴趣小组用下列装置制备![]() 并探究NO、
并探究NO、![]() 的某一化学性质
的某一化学性质![]() 中加热装置已略去
中加热装置已略去![]() 。请回答下列问题:
。请回答下列问题:
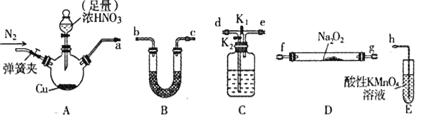
已知:①2NO+Na2O2=2NaNO2
②NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+
(1)装置A三颈烧瓶中发生反应的化学方程式为____________。
(2)用上图中的装置制备![]() ,其连接顺序为:
,其连接顺序为:![]() ___
___![]() ____
____![]() ___
___![]() ___
___![]() ___
___![]() ___
___![]() 按气流方向,用小写字母表示
按气流方向,用小写字母表示![]() ,此时活塞
,此时活塞![]() 、
、![]() 如何操作____________。
如何操作____________。
(3)![]() 装置发生反应的离子方程式是________________。
装置发生反应的离子方程式是________________。
(4)通过查阅资料,![]() 或NO可能与溶液中
或NO可能与溶液中![]() 发生反应。某同学选择上述装置并按
发生反应。某同学选择上述装置并按![]() 顺序连接,E中装入
顺序连接,E中装入![]() 溶液,进行如下实验探究。
溶液,进行如下实验探究。
步骤 | 操作及现象 |
① | 关闭K2,打开K1,打开弹簧夹通一段时间的氮气,夹紧弹簧夹,开始A中反应,一段时间后,观察到E中溶液逐渐变为深棕色。 |
② | 停止A中反应,打开弹簧夹和K2、关闭K1,持续通入N2一段时间 |
③ | 更换新的E装置,再通一段时间N2后关闭弹簧夹,使A中反应继续,观察到的现象与步骤①中相同 |
步骤②操作的目的是___________;步骤③C瓶中发生的化学方程式为_________________;通过实验可以得出:___________![]() 填“
填“![]() 、NO中的一种或两种”
、NO中的一种或两种”![]() 和溶液中
和溶液中![]() 发生反应使溶液呈深棕色。
发生反应使溶液呈深棕色。
【答案】![]() 浓
浓![]() d e b c f g 关闭
d e b c f g 关闭![]() ,打开
,打开![]()
![]() 排尽装置中残留的
排尽装置中残留的![]()
![]() NO
NO
【解析】
制备NaNO2,A装置中铜与浓硝酸反应:Cu+4HNO3(浓)=Cu(NO3)2+4NO2↑+2H2O,制备NO2,NO2与水反应3NO2+H2O=2HNO3+NO,可以在C装置中进行;根据图示,2NO+Na2O2=2NaNO2在D装置中进行,尾气中的NO不能直接排放到空气中,需要用酸性高锰酸钾吸收:3MnO4-+4H++5NO=3Mn2++5NO3-+2H2O,据此分析解答。
(1)装置A三颈烧瓶中铜与浓硝酸发生反应生成二氧化氮,化学方程式为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,故答案为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;
(2)根据上述分析,A装置制备NO2,生成的NO2在C中水反应制备NO,经过装置B干燥后在装置D中反应生成亚硝酸钠,最后用E除去尾气,因此装置的连接顺序为:a→d→e→b→c→f→g→h;此时应关闭K1,打开K2,让二氧化氮通过C装置中的水转化成一氧化氮,故答案为:d;e;b;c;f;g(b与c、f与g可以交换);关闭K1,打开K2;
(3)E装置为酸性高锰酸钾与NO的反应,NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+,离子方程式为:3MnO4-+4H++5NO=3Mn2++5NO3-+2H2O,故答案为:3MnO4-+4H++5NO=3Mn2++5NO3-+2H2O;
(4)①关闭K2,打开K1,打开弹簧夹通一段时间的氮气,夹紧弹簧夹,开始A中反应,一段时间后,观察到E中溶液逐渐变为深棕色,说明NO2或NO与溶液中Fe2+发生反应;②停止A中反应,打开弹簧夹和K2、关闭K1,持续通入N2一段时间,将装置中残留的二氧化氮排尽,并在C中与水反应,3NO2+H2O=2HNO3+NO;③更换新的E装置,再通一段时间N2后关闭弹簧夹,使A中反应继续,观察到的现象与步骤①中相同,经过步骤②,进入E装置的气体为NO,E中溶液变为深棕色,说明是NO与和溶液中Fe2+发生反应使溶液呈深棕色,故答案为:排尽装置中残留的NO2;3NO2+H2O=2HNO3+NO;NO。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】为了测定草酸晶体(H2C2O4xH2O)中的x值,进行如下实验
(1)称取Wg草酸晶体,配成100.00mL溶液
(2)取25.00mL所配溶液于锥形瓶内,加入适量稀H2SO4后,用浓度为amolL-1的KMnO4溶液滴定至KMnO4不再褪色为止,所发生的反应为:2KMnO4+5H2(C2O)4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O
①实验中,不需要的仪器有(填序号)_______________
A、托盘天平(带砝码、镊子) B、滴定管 C、100mL的量筒
D、100mL的容量瓶 E、烧杯 F、漏斗 G、锥形瓶 H、玻璃棒
I、药匙 J、烧瓶
②实验中,标准液KMnO4溶液应装在_______式滴定管中,因为________________
③若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴至终点,则所测得的x的值会_________(填偏大、偏小、无影响).
④在滴定过程中若用去amolL-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为_____________molL-1,由此,x=_____________ .
⑤若滴定终点读数时俯视刻度,则计算的x值会_______(填偏大、偏小、无影响).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O![]() Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是
Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是
A.充电时阳极反应:Ni(OH)2 -e— + OH- = NiOOH + H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钾在氧气中燃烧时得到一种钾的氧化物晶体其结构如图所示,下列有关说法正确的是
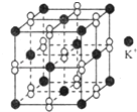
A.该氧化物属于离子晶体,其中只含离子键
B.1mol该晶体中含有的离子数目为3NA
C.晶体中与每个K+距离相等且最近的K+共有8个
D.晶体中每个K+同时吸引着6个阴离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.
(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:

4种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是__.
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示.

①写出基态Cu原子的核外电子排布式__;金属铜采用下列__(填字母代号)堆积方式.

②写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来)__.
③水分子间存在氢键,请你列举两点事实说明氢键对水的性质的影响__.
④SO42﹣的空间构型是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物![]() 是桥环烯烃类化合物,在药物合成、材料化学以及生命科学中有着重要的应用。下列关于该化合物的叙述正确的是( )
是桥环烯烃类化合物,在药物合成、材料化学以及生命科学中有着重要的应用。下列关于该化合物的叙述正确的是( )
A.分子式为C11H10
B.—氯代物有5种(不考虑立体异构)
C.不能形成高分子化合物
D.1mol该化合物最多能与3molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】立方烷结构为立方体,分子式为C8H8,其熔点比相同碳原子的辛烷高,立方烷的结构简式如图所示。下列有关立方烷的说法正确的是( )
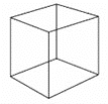
A.其一氯代物只有1种,二氯代物有2种
B.常温常压下为气体
C.与乙苯(结构简式为![]() )是同分异构体
)是同分异构体
D.与苯的含碳质量分数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同元素的原子在分子内吸引电子的能力大小可用一数值x来表示,若x越大,则原子吸引电子的能力越强,在所形成的分子中成为负电荷一方。下面是某些短周期元素的x值:

(1)通过分析x值的变化规律,确定N、Mg的x值范围: ____<x(N)<_____;_____<x(Mg)<_____。
(2)推测x值与原子半径的关系是_______________________________。
(3)某有机物结构式为C6H5SONH2,在S—N中,你认为共用电子对偏向谁?__________(写原子名称)。
(4)经验规律告诉我们当成键的两原子相应元素电负性的差值Δx>1.7时,一般为离子键,当Δx<1.7时,一般为共价键,试推断AlBr3中化学键的类型是____________。
(5)预测元素周期表中,x值最小的元素位置____________________(放射性元素除外)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验的一体化是未来化学演示实验设计的方向,它可集中解决化学实验中药品消耗量大、耗时多、污染大等系列问题。下图是二氧化硫的制备与性质的一体化实验装置图。
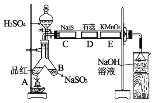
其中硫酸浓度为70%,C、D、E处分别是用Na2S溶液、紫色石蕊试液、酸性高锰酸钾溶液浸过的滤纸,按图示搭好实验装置,实验开始时由分液漏斗滴入浓硫酸即可。回答下列问题:
(1)实验室制备二氧化硫气体的化学方程式为_______。
(2)图中C、D处的实验现象分别为_______、_______。
(3)A处起始不加热,现象为_______,待全部实验结束后,用酒精灯加热,现象为_______。
(4)图中倒置漏斗的作用是_______,烧杯中NaOH溶液的作用是_______。
(5)写出E处反应的离子方程式_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com