
【题目】下列各溶液中,微粒的物质的量浓度关系正确的是( )
A.1.0 mol/L Na2CO3溶液:c(OH﹣)=c(HCO ![]() )+c(H+)+2c(H2CO3)
)+c(H+)+2c(H2CO3)
B.1.0 mol/L NH4Cl溶液:c(NH ![]() )=c(Cl﹣)
)=c(Cl﹣)
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO﹣)>c(H+)>c(OH﹣)
D.1 mol/L CH3COONa溶液,c(CH3COO﹣)=1 mol/L
【答案】A
【解析】解:A.根据Na2CO3溶液中的质子守恒可得:c(OH﹣)=c(HCO ![]() )+c(H+)+2c(H2CO3),故A正确; B.NH4Cl溶液中,铵根离子部分水解,导致铵根离子部分水解,则c(NH
)+c(H+)+2c(H2CO3),故A正确; B.NH4Cl溶液中,铵根离子部分水解,导致铵根离子部分水解,则c(NH ![]() )<c(Cl﹣),故B错误;
)<c(Cl﹣),故B错误;
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液,则c(H+)>c(OH﹣),根据电荷守恒可知:c(CH3COO﹣)>c(Na+),则正确的离子浓度大小为:c(CH3COO﹣)>c(Na+)>c(H+)>c(OH﹣),故C错误;
D.CH3COONa溶液中,醋酸根离子部分水解,导致醋酸根离子的浓度减小,则c(CH3COO﹣)<1 mol/L,故D错误;
故选A.


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】硼和氮元素在化学中有很重要的地位,回答下列问题:
(1)基态硼原子核外电子有种不同的运动状态,基态氮原子的价层电子排布图为 . 预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2].(CH3)2NNH2中N原子的杂化方式为 .
(2)化合物H3BNH3是一种潜在的储氢材料,可利用化合物B3N3H6通过如下反应制得:3CH4+2B3N3H6+6H2O═3CO2+6H3BNH3①H3BNH3分子中是否存在配位键(填“是”或“否”),B、C、N、O的第一电离能由小到大的顺序为 .
②与B3N3H6互为等电子体的分子是(填一个即可),B3N3H6为非极性分子,根据等电子原理写出B3N3H6的结构式 .
(3)“嫦娥五号”探测器采用太阳能电池板提供能量,在太阳能电池板材料中除单晶硅外,还有铜,铟,镓,硒等化学物质,回答下列问题:①SeO3分子的立体构型为 .
②金属铜投入氨水或H2O2溶液中均无明显现象,但投入氨水与H2O2的混合溶液中,则铜片溶解,溶液呈深蓝色,写出该反应的离子反应方程式为 .
③某种铜合金的晶胞结构如图所示,该晶胞中距离最近的铜原子和氮原子间的距离为 ![]() apm,则该晶体的密度为(用含a的代数式表示,设NA为阿伏伽德罗常数的值).
apm,则该晶体的密度为(用含a的代数式表示,设NA为阿伏伽德罗常数的值).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[Cu(NH3)4]SO4H2O是一种杀虫剂.
(1)Cu元素基态原子的电子排布式为 , 根据元素原子的外围电子排布特征,可将周期表分成五个区域,其中Cu属于区.
(2)元素N、O、S的第一电离能由大到小排列的顺序为 .
(3)H元素可与O元素形成H2O和H2O2 , H2O2易溶于H2O,其主要原因为 .
(4)H元素与N元素可组成化合物N2H4 , 其中N原子的轨道杂化方式为 .
(5)SO42﹣的空间构型是 , 与SO42﹣互为等电子体的一种分子的化学式为 .
(6)Cu元素与H元素可形成一种红色晶体,其结构如图,则该化合物的化学式为 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水在25℃和95℃时,其电离平衡曲线如图所示: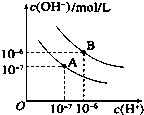
(1)则25℃时水的电离平衡曲线应为(填“A”或“B”),请说明理由
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施是为了降低化学反应速率的是( )
A.铁粉代替铁钉与稀硫酸反应制取氢气
B.双氧水制氧气时加入少量二氧化锰
C.镁和水反应时,适当进行加热
D.食品放在冰箱中贮藏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离或水解方程式书写不正确的是( )
A.碳酸氢钠的电离方程式为:NaHCO3═Na++HCO ![]() ?? HCO
?? HCO ![]() ?H++CO
?H++CO ![]()
B.偏铝酸钠的水解方程式为:AlO2﹣+2H2O═Al(OH)3↓+OH﹣
C.硫化铝溶于水的水解方程式为:Al2S3+6H2O═2Al(OH)3↓+3H2S↑
D.醋酸铵的水解方程式为:CH3COO﹣+NH ![]() +H2O?CH3COOH+NH3?H2O
+H2O?CH3COOH+NH3?H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大。A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成离子化合物,其阴阳离子个数比为1∶1。
回答下列问题:
(1)五种元素中非金属性最强的是_______________(填元素符号)。
(2)由A和B、D、E所形成的共价化合物中,热稳定性最差的是_______________(用化学工表示)。
(3)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为_______________,其中存在的化学键类型为____________________。
(4)D的最高价氧化物的水化物的化学式为____________________。
(5)由A和B形成的一种气体在工业上用途很广。其工业制法的方程式为:__________;实验室制取的方程式为____________________。
(6)单质E与水反应的离子方程式为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com