
【题目】对反应:![]()
(1)配平上述化学方程式并标出该反应中电子转移情况_____________________________
(2)该反应中的氧化剂是__________ ,被氧化的元素是_____________。
(3)1 mol Cl2参加反应,被氧化的NH3 的物质的量是_____________mol。
(4)若有68g NH3参加反应,电子转移的物质的量是_______mol。
科目:高中化学 来源: 题型:
【题目】下列说法或表示方法正确的( )
A. 在稀溶液中,![]() ;
;![]() ,若将含
,若将含![]() 的硫酸与含1molNaOH的溶液混合,放出的热一定为
的硫酸与含1molNaOH的溶液混合,放出的热一定为![]()
B. 由![]() 石墨
石墨![]() 金刚石
金刚石![]() :
:![]() 可知,金刚石比石墨稳定
可知,金刚石比石墨稳定
C. 实验测得环己烷![]() 、环己烯
、环己烯![]() 和苯
和苯![]() 的标准燃烧分别为
的标准燃烧分别为![]() 、
、![]() 和
和![]() ,可以证明在苯分子中不存在独立的碳碳双键
,可以证明在苯分子中不存在独立的碳碳双键
D. 在101kPa时,![]() 完全燃烧生成液态水,放出
完全燃烧生成液态水,放出![]() 热量,则表示氢气燃烧热的热化学方程式为:
热量,则表示氢气燃烧热的热化学方程式为:![]() ;
;![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟铝酸钠(Na3AlF6)是工业炼铝中重要的含氟添加剂。实验室以氟石(CaF2)、石英和纯碱为原料模拟工业制备氟铝酸钠的流程如下:
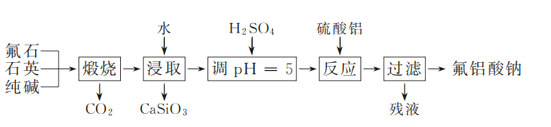
(1) “煅烧”时,固体药品混合后应置于________(填仪器名称)中加热。
(2) 通过控制分液漏斗的活塞可以调节添加液体的速率。调溶液pH接近5时,滴加稀硫酸的分液漏斗的活塞应如下图中的________(填序号)所示。

(3) 在酸性废水中加入Al2(SO4)3、Na2SO4混合溶液,可将废水中F-转换为氟铝酸钠沉淀。
① 该混合溶液中,Al2(SO4)3与Na2SO4的物质的量之比应≥________(填数值)。
②在不改变其他条件的情况下,加入NaOH调节溶液pH。实验测得溶液中残留氟浓度和氟去除率随溶液pH的变化关系如图所示。pH>5时,溶液中残留氟浓度增大的原因是________。
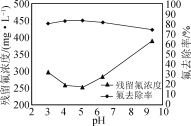
(4) 若用CaCl2作为沉淀剂除去F-,欲使F-浓度不超过0.95 mg·L-1,c(Ca2+)至少为________mol·L-1。[Ksp(CaF2)=2.7×10-11]
(5) 工业废铝屑(主要成分为铝,少量氧化铁、氧化铝)可用于制取硫酸铝晶体[Al2(SO4)3·18H2O]。
①请补充完整由废铝屑为原料制备硫酸铝晶体的实验方案:取一定量废铝屑,放入烧杯中,____________________________________________________________,得硫酸铝晶体。[已知:pH=5时,Al(OH)3沉淀完全;pH=8.5时,Al(OH)3沉淀开始溶解。须使用的试剂:3 mol·L-1 H2SO4溶液、2 mol·L-1 NaOH溶液、冰水]
②实验操作过程中,应保持强制通风,原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】冬季的降雪给交通带来了诸多不便,其中醋酸钾(CH3COOK)是融雪效果最好的融雪剂,下列关于醋酸钾的说法正确的是( )
A.1 molCH3COOK的质量为98g/mol
B.含有6.02×1023个碳原子的CH3COOK的物质的量是1mol
C.一个CH3COO-的质量约为![]() g
g
D.CH3COOK摩尔质量就是它的相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下4组实验,如图Ⅰ~Ⅳ所示。
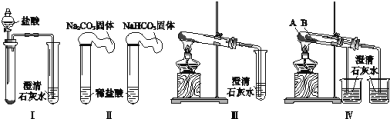
(1)Ⅱ所示的实验,若固体质量相同且稀盐酸足量时,气球鼓起较小的是___(填化学式)。
(2)Ⅲ、Ⅳ所示的实验均能鉴别这两种物质,相关反应的化学方程式是___和___。
(3)与Ⅲ相比,IV的优点是___(填选项序号)。
a.Ⅳ比Ⅲ复杂
b.Ⅳ比Ⅲ安全
c.Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
(4)若用Ⅳ验证碳酸钠和碳酸氢钠的热稳定性,则试管B中装入的固体应该是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图。
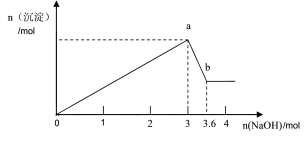
(1)a点对应的沉淀为________________(填化学式)。
(2)计算原混合液中FeCl3的物质的量浓度为多少_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列填空。
(1)在等体积的NaCl、MgCl2、AlCl3三种溶液中,分别加入等量的AgNO3溶液,恰好都完全反应,则以上三种溶液的物质的量浓度之比为______。
(2)将3.22 g芒硝(Na2SO4·10H2O)溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为________g。
(3)在干燥烧瓶中用向下排空气法收集氨气,由于空气不可能排净,所以瓶内气体对氢气的相对密度为9.5,将此瓶气体倒置于水槽中,烧瓶内液面上升的体积占烧瓶总体积的_______。
(4)100 mL 0.3 mol/L Na2SO4(密度为d1 g/cm3)和50 mL 0.2 mol/L Al2(SO4)3(密度为d2 g/cm3)混合,所得密度为d3 g/cm3的混合溶液中SO42的浓度为___________。(用含d1,d2, d3的式子表示)
(5)已知两种碱AOH和BOH的摩尔质量之比为5:7,现将7 mol AOH与5 mol BOH混合后,从中取出5.6 g,恰好可以中和100ml浓度为1.2 mol/L的盐酸,则AOH的摩尔质量为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。
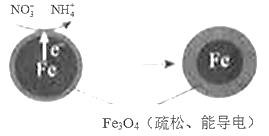
①作负极的物质是____。
②正极的电极反应式是____。
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
pH=4.5时,NO3-的去除率低。其原因是____。
(4)其他条件与(2)相同,经1小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 约10% | 约3% |
1小时pH | 接近中性 | 接近中性 |
与(2)中数据对比,解释(2)中初始pH不同时,NO3-去除率和铁的最终物质形态不同的原因:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)工业上,在Cu2O/ZnO 作催化剂的条件下发生反应:CO(g)+2H2(g)CH3OH(g) △H
(1)已知:CH3OH(l)=CH3OH(g) △H=+35.2kJmol-1,根据表:
物质 | H2(g) | CO(g) | CH3OH(l) |
燃烧热/kJmol-1 | -285.8 | -283.0 | -726.5 |
反应CO(g)+2H2(g)CH3OH(g) △H=______kJmol-1
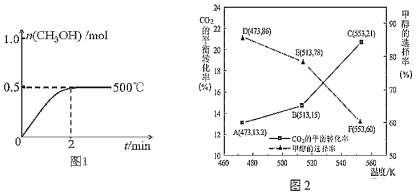
(2)向2L恒容密闭容器中通入1mol CO(g)和2mol H2(g),发生反应合成甲醇,反应过程中n(CH3OH)与时间(t)及温度的关系如图1所示。在500℃恒压条件下,请在图1中画出反应体系中n(CH3OH)与时间(t)变化总趋势图。
 ____________
____________
(二)甲醇还可用CO2与H2在催化剂CZZA(普通铜基催化剂)作用下合成,相关反应如下:
反应ⅠCO2(g)+3H2(g)CH3OH(g)+H2O(g) △H1=-49.2kJmol-1
反应ⅡCO2(g)+H2(g)CO(g)+H2O(g) △H2=41.2kJmol-1
(3)以CZZA/rGO为催化剂,在一定条件下,将1mol CO2与3mol H2通入恒容密闭容器中进行反应I和反应II,CO2的平衡转化率和甲醇的选择率(甲醇的选择率:转化的CO2中生成甲醇的物质的量分数)随温度的变化趋势如图2所示:
①在553K时,反应体系内CO的物质的量为______ mol
②随着温度的升高,CO2的平衡转化率增加但甲醇的选择率降低,请分析其原因:______
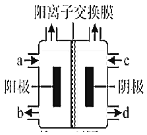
(三)(4)如图为氯碱工业的装置示意图,a端进入的物质为______,工业上还可以利用该装置,以四甲基氯化铵[(CH3)4NCl]水溶液为原料,通过电解法可制备四甲基氢氧化铵[(CH3)4NOH],则收集到(CH3)4NOH的区域是______(填a、b、c或d),
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com