
【题目】25℃时,将氨水与氯化铵溶液混合得到 c(NH3·H2O)+c(NH4+) = 0.1mol·L-1的混合溶液。溶液中c(NH3·H2O)、c(NH4+)与pH的关系如图所示。下列有关离子浓度关系叙述一定正确的是

A. W点表示溶液中:c(NH4+) +c(H+) =c(Cl-)+c(OH-)
B. pH=10.5溶液中:c(Cl-)+c(OH-)+c(NH3·H2O)<0.1mol·L-1
C. pH=9.5溶液中:c(NH3·H2O)>c(NH4+)>c(OH-)>c(H+)
D. 向W点所表示1L溶液中加入0.05molNaOH固体(忽略溶液体积变化):c(Cl-)>c(Na+)>c(OH-)>c(NH4+) >c(H+)
【答案】AC
【解析】试题分析:A、根据电荷守恒思想,应是c(NH4+)+c(H+)=c(OH-)+c(Cl-),故错误;B、溶液中存在电荷守恒c(NH4+)+c(H+)=c(Cl-)+c(OH-),则c(Cl-)+c(OH-)+c(NH3·H2O)=c(NH4+)+c(NH3·H2O)+c(NH3·H2O)>0.1mol·L-1,故错误;C、pH=9.5说明溶液显碱性,NH4+的水解小于NH3·H2O的电离,根据图像,c(NH3·H2O)>c(NH4+)因此溶液中:c(NH3·H2O)>c(NH4+)>c(OH-)>c(H+),故正确;D、W点时,c(NH3·H2O)=c(NH4+)=0.05mol·L-1,加入0.05molNaOH固体,得到0.1mol的NH3·H2O和0.05molNaCl,c(Na+)=c(Cl-),因此c(Cl-)=c(Na+)>c(OH-)>c(NH4+)>c(H+),故错误。


科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A. 离子键没有方向性和饱和性,而共价键有方向性和饱和性
B. 离子键的强弱主要决定于离子半径和离子所带电荷数
C. 配位键在形成时,由成键双方各提供一个电子形成一对共用电子
D. 金属键的实质是金属中的自由电子与金属阳离子形成的一种强烈的相互作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用铜制备CuSO 4 溶液有多种方案,某实验小组给出了以下三种方案:
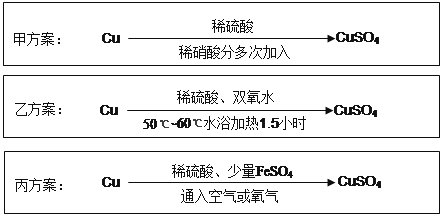
请回答有关问题:
(1)甲方案:
①写出该反应的离子方程式 ;
②为了节约原料,硫酸和硝酸的物质的量之比最佳为,n(H 2 SO 4 ):n(HNO 3 )= 。
(2)乙方案:将6.4g铜丝放到90mL 1.5mol·L -1 的稀硫酸中,控温在50℃。加入40mL 10%的H2O2,反应0.5小时,升温到60℃,持续反应1小时后,经一系列操作,得CuSO 4·5H 2O 20.0g【已知有关摩尔质量:M(Cu)=64g/mol, M(CuSO4·5H 2 O) =250g/mol】。
①反应时温度控制在50℃~60℃,不宜过高的原因是 ;
②本实验CuSO4·5H 2 O的产率为 。
(3)丙方案:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO 4 ,即发生反应,生成硫酸铜。反应完全后,加物质A调节pH至4 ,然后过滤、浓缩、结晶。
①物质A可选用以下的 (填序号);
A.CaO
B.NaOH
C.CuCO 3
D.Cu 2(OH)2CO 3
E.Fe2(SO4) 3
②反应中加入少量FeSO 4 可加速铜的氧化,FeSO 4 的作用是 ;
反应过程中的的离子方程式为: 、
(4)对比甲、乙、丙三种实验方案,丙方案的优点有(写两条): 、 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄酮类化合物具有抗肿瘤活性,6-羟基黄酮衍生物的合成路线如下:
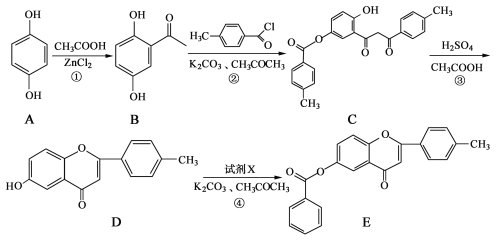
请回答下列问题:
(1)化合物B中的含氧官能团为 和 (填名称)。
(2)反应③中涉及到的反应类型有水解反应、 和 。
(3)反应④中加入的试剂X的分子式为C7H5OCl,X的结构简式为 。
(4)B的一种同分异构体满足下列条件:
Ⅰ.能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应。
Ⅱ.分子中有4种不同化学环境的氢。
写出该同分异构体的结构简式: 。
(5)已知: 。根据已有知识并结合相关信息,写出以
。根据已有知识并结合相关信息,写出以![]() 和CH3COOH为原料制备
和CH3COOH为原料制备![]() 的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:
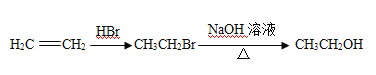
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于糖类、油脂和蛋白质的性质说法正确的是
A.糖类物质中含C、H、O元素,都有甜味
B.油脂是高分子化合物,热值较大
C.在蛋白质溶液中加入CuSO4溶液后有物质析出,加水后该物质溶解
D.葡萄糖能与银氨溶液反应,可用作制镜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃组成的混合气体0.1mol,完全燃烧得0.15mol CO2和3.6g H2O,下列关于该混合气体的说法正确的是( )
A.一定有乙烯 B.一定没有乙烯 C.一定有甲烷 D.可能有乙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子化合物①NaCl、②CaO、③NaF、④MgO中,晶格能从小到大顺序正确的是( )
A.①②③④ B.①③②④ C.③①④② D.④②①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)写出R的原子结构示意图:________________
(2)五种元素原子半径由大到小的顺序是(写元素符号) .
(3)X与Y能形成多种化合物其中既含极性键又含非极性键,且相对分子质量最小的物质是(写分子式) ,X和Z组成的化合物的化学式为___________________
(4)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A![]() B(在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的化学式 ;D的电子式 .
B(在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的化学式 ;D的电子式 .
①如果A、B均由三种元素组成,B为两性不溶物,则A![]() B离子反应方程式为_________
B离子反应方程式为_________
②A、B均为盐溶液,如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性.用离子方程式表示A溶液显碱性的原因 ;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】贵州凤岗的“富锌富硒”茶已享誉全国,因富含硒元素,有延年益寿、抗衰老等作用。但研究表明单质硒可能成为环境污染物,通过与浓盐酸、浓H2SO4反应可回收Se。在回收过程中涉及到如下两个化学反应:①SeO2+4KI+4HCl=Se+2I2+4KCl+2H2O;②Se+2H2SO4(浓)=2SO2![]() + SeO2+2H2O。下列叙述正确的是( )
+ SeO2+2H2O。下列叙述正确的是( )
A. 反应①中Se是氧化产物,I2是还原产物
B. 反应②中浓H2SO4是氧化剂,SeO2是还原产物
C. 反应①中每有1.0mol I2生成,转移电子数目为4 NA
D. SeO2、H2SO4(浓)、I2的氧化性由强到弱的顺序是H2SO4(浓)> SeO2> I2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com