
【题目】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)写出R的原子结构示意图:________________
(2)五种元素原子半径由大到小的顺序是(写元素符号) .
(3)X与Y能形成多种化合物其中既含极性键又含非极性键,且相对分子质量最小的物质是(写分子式) ,X和Z组成的化合物的化学式为___________________
(4)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A![]() B(在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的化学式 ;D的电子式 .
B(在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的化学式 ;D的电子式 .
①如果A、B均由三种元素组成,B为两性不溶物,则A![]() B离子反应方程式为_________
B离子反应方程式为_________
②A、B均为盐溶液,如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性.用离子方程式表示A溶液显碱性的原因 ;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有 .
【答案】(1) ;
;
(2)Na>Al>C>O>H
(3)C2H2; H2O和H2O2 ;
(4)CO2;![]() ;
;
①AlO2-+CO2+2H2O==Al(OH)3↓+HCO3-;②CO32-+H2O![]() HCO3-+OH-;NaCl H2CO3NaHCO3
HCO3-+OH-;NaCl H2CO3NaHCO3
【解析】试题分析:X、Y、Z、Q、R是五种短周期元素,原子序数依次增大,Z、R分别是地壳中含量最高的非金属元素和金属元素,则Z为O元素、R为Al;X、Y两元素最高正价与最低负价代数和均为0,原子序数均小于O元素,为ⅠA族元素、ⅣA族元素,故X为H元素、Y为C元素;Q与X同主族,结合原子序数可知,Q为Na元素。
(1)R为Al,原子结构示意图为 ,故答案为:
,故答案为: ;
;
(2)同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径Na>Al>C>O>H,故答案为:Na>Al>C>O>H;
(3)H与C形成多种化合物,属于烃类物质,其中既含极性键又含非极性键,且相对分子质量最小是C2H2,H与O形成的化合物有H2O和H2O2,故答案为:C2H2;H2O和H2O2;
(4)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A![]() B(在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。则D是Na2O2,C是CO2,D的电子式为
B(在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。则D是Na2O2,C是CO2,D的电子式为![]() ,故答案为:CO2;
,故答案为:CO2;![]() ;
;
①如果A、B均由三种元素组成,B为两性不溶物,则B是Al(OH)3,D是过氧化钠、C是二氧化碳,则A是偏铝酸钠,其化学式为NaAlO2,偏铝酸钠和过量二氧化碳反应生成氢氧化铝和碳酸氢根离子,离子反应方程式为:AlO2-+2H2O+CO2=Al(OH)3+HCO3-,故答案为:AlO2-+2H2O+CO2=Al(OH)3+HCO3-;
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性,B和氢氧化钠反应生成A,A和二氧化碳反应生成B,所以B是碳酸氢钠、A是碳酸钠,碳酸根离子水解导致碳酸钠溶液呈碱性,水解方程式为CO32-+H2O![]() HCO3-+OH-;常温下,A、B浓度均为0.1molL-1的混合溶液中,滴加盐酸,生成NaCl,但溶液中溶解二氧化碳,溶液呈中性时,应有部分NaHCO3,则溶液中的溶质为NaHCO3、NaCl、CO2或者碳酸,故答案为:CO32-+H2O
HCO3-+OH-;常温下,A、B浓度均为0.1molL-1的混合溶液中,滴加盐酸,生成NaCl,但溶液中溶解二氧化碳,溶液呈中性时,应有部分NaHCO3,则溶液中的溶质为NaHCO3、NaCl、CO2或者碳酸,故答案为:CO32-+H2O![]() HCO3-+OH-; NaHCO3、NaCl、CO2或者碳酸
HCO3-+OH-; NaHCO3、NaCl、CO2或者碳酸


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,将SO2和O2充入一密闭容器中,发生如下反应:2SO2(g)+O2(g)![]() 2SO3(g)(正反应放热)反应过程中SO2、O2、SO3物质的量变化如图所示。回答下列问题:
2SO3(g)(正反应放热)反应过程中SO2、O2、SO3物质的量变化如图所示。回答下列问题:

(1)降低温度,化学反应速度_________。(填“增大”“减小”或“不变”)
(2)反应处于平衡状态的时间是____ _____。
(3)反应进行至20 min时,曲线发生变化的原因是______________________(用文字表达)。10 min到15 min的曲线变化的原因可能是_________(填写编号)。
a.加了催化剂
b.缩小容器体积
c.降低温度
d.增加SO3的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将氨水与氯化铵溶液混合得到 c(NH3·H2O)+c(NH4+) = 0.1mol·L-1的混合溶液。溶液中c(NH3·H2O)、c(NH4+)与pH的关系如图所示。下列有关离子浓度关系叙述一定正确的是

A. W点表示溶液中:c(NH4+) +c(H+) =c(Cl-)+c(OH-)
B. pH=10.5溶液中:c(Cl-)+c(OH-)+c(NH3·H2O)<0.1mol·L-1
C. pH=9.5溶液中:c(NH3·H2O)>c(NH4+)>c(OH-)>c(H+)
D. 向W点所表示1L溶液中加入0.05molNaOH固体(忽略溶液体积变化):c(Cl-)>c(Na+)>c(OH-)>c(NH4+) >c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾严重影响人们的生活与健康。某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-。某同学收集了该地区的雾霾,经必要的预处理后得试样溶液,设计并完成了如下的实验:

已知:3NO3-+ 8Al + 5OH-+ 18H2O = 3NH3+ 8[Al(OH)4]-
根据以上的实验操作与现象,该同学得出的结论不正确的是( )
A. 试样中一定不含Al3+
B. 试样中肯定存在NH4+、Mg2+、SO42-和NO3-
C. 试样中可能存在Na+、Cl-
D. 该雾霾中可能存在NaNO3、NH4Cl和MgSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】

请回答下列问题:
(1)对青蒿进行干燥破碎的目的是_____________。
(2)操作I需要的玻璃仪器主要有:烧杯、_________,操作Ⅱ的名称是_______________。
(3)操作Ⅲ的主要过程可能是_____________(填字母)。
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(4)用下列实验装置测定青蒿素分子式的方法如下:将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。

①装置E中盛放的物质是______________,装置F中盛放的物质是________________。
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是_______________。
③用合理改进后的装置进行试验,称得:

则测得青蒿素的最简式是__________________。
(5)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与____________(填字母)具有相同的性质。
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
(6)某科研小组经多次提取青蒿素实验认为用石油醚做溶剂较为适宜,实验中通过控制其他实验条件不变,来研究原料的粒度、提取时间和提取温度对青蒿素提取速率的影响,其结果如下图所示:

由上图可知控制其他实验条件不变,采用的最佳粒度、时间和温度为_______________。
A.80目、100分钟、50℃ B.60目、120分钟、50℃ C.60目、120分钟、55℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有以下几种有机物:
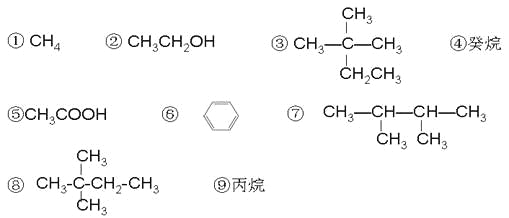
请利用上述给出的物质按要求回答下列问题:
(1)相对分子质量为44的烷烃的结构简式为 ;
(2)分子中含有14个氢原子的烷烃的分子式是 ;
(3)与③互为同分异构体的是 (填序号);
(4)具有特殊气味,常作萃取剂的有机物在铁作催化剂的条件下与液溴发生一取代反应的化学方程式 ;
(5)用“>”表示①③④⑨熔沸点高低顺序: (填序号);
(6)有机物②在加热条件下和CuO反应的化学方程式 ;
(7)在120℃,1.01×105Pa条件下,某种气态烃与足量的O2完全反应后,测得反应前后气体的体积没有发生改变,则该烃是 (填序号);它与⑧互为 关系;
(8)有机物⑤和②在一定条件下发生反应的化学方程式是 ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com