
【题目】某元素的原子最外层只有一个电子,它跟卤素相结合时,可形成的化学键( )
A.一定是共价键B.一定是离子键
C.可能是共价键,也可能是离子键D.上述说法都不正确
 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】Bodensteins研究反应H2(g)+I2(g)![]() 2HI(g),温度为T时,在两个体积均为1 L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w (HI)与反应时间t的关系如下表:
2HI(g),温度为T时,在两个体积均为1 L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w (HI)与反应时间t的关系如下表:
容器编号 | 起始物质 | t/min | 0 | 20 | 40 | 60 | 80 | 100 |
I | 0.5 mol I2、0.5 mol H2 | w (HI)/% | 0 | 50 | 68 | 76 | 80 | 80 |
II | x mol HI | w (HI)/% | 100 | 91 | 84 | 81 | 80 | 80 |
研究发现上述反应中:v正=ka·w(H2)·w(I2),v逆=kb·w2(HI),其中ka、kb为常数。下列说法正确的是:
A. 温度为T时,该反应![]() = 64
= 64
B. 容器I中在前20 min的平均速率v(HI)=0.0125 mol·L-1·min-1
C. 若起始时向容器I中加入物质的量均为0.1 mol的H2、I2、HI,反应逆向进行
D. 若两容器中存在kaⅠ=kaⅡ且kbⅠ=kbⅡ,则x的值一定为1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以A为原料可制备C(丹皮酚)和D(树脂),其合成路线如下:

(1)A在空气中会缓慢变成粉红色,其原因是_____________________________________。
(2)A→B的反应类型为______________________;A生成D的反应中,试剂X(烃的含氧衍生物)为____________________(写结构简式)。
(3)只含有两个取代基的芳香化合物E是C的同分异构体,E既能与FeCl3溶液发生显色反应又能发生银镜反应和水解反应,则E共有________种(不考虑立体结构),其中核磁共振氢谱为六组峰且峰面积比为1:1:2:2:2:2 的结构简式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸牛奶中的乳酸可增进食欲、促进胃液分泌、增强肠胃的消化功能,对人体具有保健作用,乳酸分子的结构简式为![]() 。工业上可由乙烯来合成乳酸,方法如下:
。工业上可由乙烯来合成乳酸,方法如下:

(1)乳酸所含的官能团的名称是_________________________。
(2)写出下列物质转化的化学方程式:
①A→B______________________________________。
②B→CH3CHO____________________________________。
③![]() __________________________________。
__________________________________。
(3)A在一定条件下可发生消去反应,写出其发生消去反应的化学方程式:_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 金属铜与硝酸银溶液反应:Cu+Ag+ =Cu2++Ag
B. Ba(OH)2溶液和H2SO4溶液反应:Ba2+ + OH- + H+ + SO42- = BaSO4↓+ H2O
C. 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
D. 石灰乳与盐酸反应:Ca(OH)2+2H+ = Ca2++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应不能设计成原电池的是( )
A.2CH3OH+3O2→2CO2+4H2O
B.NaOH+HCl=NaCl+H2O
C.Zn+2HCl=ZnCl2+H2↑
D.4Al+3O2+6H2O=4Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国科学家威廉·诺尔斯、柏利·沙普利斯和日本化学家野依良治因通过使用快速和可控的重要化学反应来合成某些手性分子的方法而获得2001年的诺贝尔化学奖。所谓手性分子是指在分子中,当一个碳原子上连有彼此互不相同的四个原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子。凡是有一个手性碳原子的物质一定具有光学活性。例如,有机化合物: 有光学活性。则该有机化合物分别发生如下反应后,生成的有机物仍有光学活性的是( )
有光学活性。则该有机化合物分别发生如下反应后,生成的有机物仍有光学活性的是( )
A. 与乙酸发生酯化反应 B. 与NaOH水溶液共热
C. 在催化剂存在下与氢气作用 D. 与银氨溶液作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为周期表的一部分,其中的编号代表对应的元素,用化学用语回答以下问题。
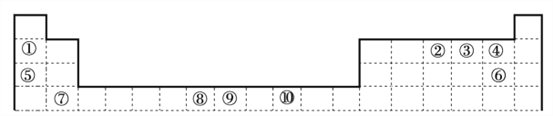
(1)其中属于过渡元素的是_____________,比较②的氢化物与同族第3、4周期元素所形成的氢化物沸点高低并说明理由_____________
(2)②与③中第一电离能较小的元素是_____________;①和④形成的物质与⑤和⑥形成的物质晶体中熔点较高的是_____________。
(3)①形成的有机试剂在有机合成中有重要应用,但极易与O2、CO2等反应。下列说法不正确的是_____________(填字母序号)
a.CO2中键σ与π键的数目之比为1:1
b.游离态和化合态①元素均可由特征发射光谱检出
c.叔丁基锂([(CH3)3C]Li)中碳原子的杂化轨道类型为sp3和sp2
(4)如图一是上述元素形成的物质晶胞结构示意图,其化学式为_____________,其中Fen+的基态电子排布式为_____________,PO43-的空间构型为_____________
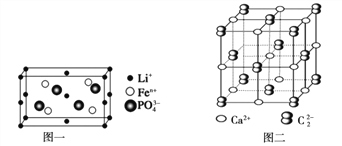
(5)金属①的晶体为体心立方晶胞,其配位数为_____________;若其晶胞边长为a pm,则锂晶体中原子的空间占有率是_____________
(6)上述元素形成的CaC2晶体的晶胞结构与NaCl晶体的相似(如图二所示),但CaC2晶体中哑铃形C22-的存在,使晶胞沿一个方向拉长(粒子间距增加)。CaC2晶体中1个Ca2+周围距离最近的C22-数目为_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】塑料废弃物又称“白色污染”,它的危害有
① 难以分解,破坏土壤结构,影响植物生长 ② 污染海洋 ③ 危及海洋生物的生存 ④ 破坏环境卫生,污染地下水
A. ①②③ B. ①③④ C. ②③④ D. ①②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com