
【题目】下图的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C、D、E为无色气体,C能使湿润的红色石蕊试纸变蓝,B常温下为无色液体,Fe遇浓的G溶液钝化。

(1)写出下列各物质的化学式:
B:____________;F:____________;G:___________。
(2)写出下列变化的反应方程式:
A→D:________________________________________;
G→E:________________________________________。
(3)实验室里,常用加热_____________________的混合物的方法制取气体C,常采用____________法来收集。
【答案】H2O NO2 HNO3 2CO2+2Na2O2==2Na2CO3+O2 3Cu+8HNO3(稀)==3Cu(NO3)2+2NO↑+4H2O NH4Cl和Ca(OH)2 向下排空气
【解析】
常温下A、C、D、E为无色气体,C能使湿润的红色石蕊试纸变蓝,则C为NH3;X就是铵盐;气体A能与过氧化钠反应生成气体D,则A为CO2,D为O2.氨气催化氧化生成的气体E是NO,F是NO2, G可以与铜反应产生F,则G为硝酸,F为NO2;无色液体B为H2O,X受热分解生成CO2、NH3、H2O,故X为NH4HCO3或(NH4)2CO3;据此分析。
常温下A、C、D、E为无色气体,C能使湿润的红色石蕊试纸变蓝,则C为NH3;A能与过氧化钠反应生成D,则A为CO2,D为O2.氨气催化氧化生成NO,不同浓度的G可以与铜反应,则G为硝酸,F为NO2;无色液体B为H2O,X受热分解生成CO2、NH3、H2O,故X为NH4HCO3或(NH4)2CO3。
(1)由上述分析可知,B为H2O,F为NO2,G为HNO3;
(2) CO2与Na2O2反应,产生碳酸钠和氧气,所以A→D的反应方程式为:2CO2+2Na2O2 ==2Na2CO3+O2;
稀硝酸与铜反应,产生硝酸铜、一氧化氮和水,所以G→E的反应方程式为:3Cu+8HNO3(稀)==3Cu(NO3)2+2NO↑+4H2O;
(3)实验室里通常是用铵盐NH4Cl与碱Ca(OH)2共热制取氨气,实验室制取气体氨气的化学方程式为:2NH4Cl+Ca(OH)2![]() CaCl2+ 2NH3↑+2H2O;氨气极易溶于水,不能用排水法收集;根据其密度比空气小的性质,用向下排空气的方法收集。
CaCl2+ 2NH3↑+2H2O;氨气极易溶于水,不能用排水法收集;根据其密度比空气小的性质,用向下排空气的方法收集。


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】实验室要配制100 mL 2 mol/L NaCl溶液,请回答下列问题:
(1)配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、胶头滴管、量筒和___________。
(2)用托盘天平称取氯化钠固体,其质量为__________ g。
(3)下列主要操作步骤的正确顺序是___________(填序号)。
①称取一定质量的氯化钠,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③将溶液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)如果实验过程中缺少步骤⑤,会造成所配溶液的物质的量浓度_______(填“偏高”或“偏低”或“无影响”,)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B为常见的非金属单质且常温下均为气体,甲、乙为金属单质,乙在I的浓溶液中发生钝化,C为极易溶于水的气体而且水溶液呈碱性,而H为一种强碱,各物质间的转化关系如下图(部分生成物末给出,且未注明反应条件):

(1)已知D为无色气体遇氧气随即变为红棕色气体G,则上述转化关系的反应④中,每反应消耗3mol G,转移电子的物质的量为___________mol。
(2)实验室制取C物质的化学方程式为:__________________。
(3)已知上述转化关系中反应⑥的发生一般是将H溶于水得到强碱溶液再与金属乙混合,此时看到金属乙溶解且表面冒气泡,请写出反应⑥的离子方程式:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,二元弱酸H2X溶液中含X微粒的分布分数如图所示。下列叙述正确的是
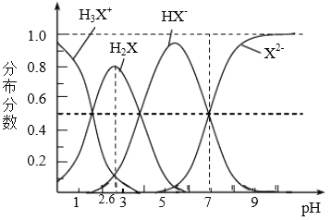
A. 溶液pH由l升至2.6时主要存在的反应是:H3X++OH-=H2X+H20
B. H2X的第二步电离平衡常数Ka2(H2X)为10-4
C. NaHX溶液中c(H+)<c(OH-)
D. 当溶液呈中性时:c(Na+)=2c(X2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
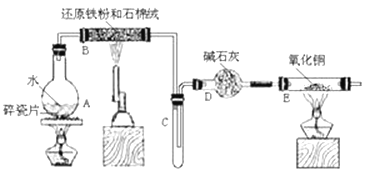
【题目】某校化学小组学生利用下图所列装置进行“铁与水反应”的实验。(图中夹持及尾气处理装置均已略去)
(1)烧瓶底部放置了几片碎瓷片,碎瓷片的作用是_________________________________。
装置B中发生反应的化学方程式是___________________________________。
(2)如果要在C处玻璃管处点燃该气体,则必须对该气体进行________________________, 装置E中的现象是_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 节日里燃放的五彩缤纷的烟花是某些金属元素化学性质的展现
B. 将等物质的量的氧化钠和过氧化钠分别投入到足量且等质量的水中,得到溶质质量分数分别是 a%和 b%的两种溶液,则a 和 b 的关系是 a=b
C. 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来, 说明金属铝的熔点较低
D. 用如图装置进行实验,将装置①中的 AlCl3 溶液滴入装置②浓氢氧化钠溶液,溶液中可观察到有大量白色沉淀产生

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000mol/L的NaOH溶液滴定20mL同浓度的一元弱酸HA,滴定过程溶液pH随NaOH溶液的体积的变化曲线如图所示(忽略中和热效应)。下列说法不正确的是

A. 常温下,HA的电离常数K(HA)约为10-5
B. v1<20
C. 溶液中水的电离程度:a点>b点
D. 滴定过程为了确定滴定终点,最合适的指示剂是酚酞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)25℃时,0.1 mol L-1 HCl溶液中,Kw=__________________,c(Cl-)=____________,c(OH-)=______________, pH=_______。
(2)25℃时,将等体积、等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈______(填“酸性”,“中性”或“碱性”),溶液中c(Na+ ) ______c(CH3COO-)(填“ >”,“=”或“<” )。
(3)25℃时, pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈__________(填“酸性”,“中性”或“碱性”),溶液中c(Na+ ) ______c(CH3COO-) (填“ >” ,“=”或“<” )。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH2OH(羟胺)是一种无色针状结晶,羟胺及其盐类常用作有机合成的还原剂。回答下列问题:
(1) NH2OH的电子式为________________。
(2)拉西法制备羟胺的总反应为2NO2-+4SO2+6H2O+6NH3=4SO42-+6NH4++2NH2OH。该反应中NH3__________(填“作氧化剂”“作还原剂”或“既不作氧化剂又不作还原剂”)。
(3)室温时,NH2OH会发生分解反应,分解产生的无色气体遇浓盐酸产生白烟,与空气接触变为红棕色;且其分解产物会使无水CuSO4变蓝色,则NH2OH分解反应的化学方程式为______________________。
(4)催化还原NO是制备盐酸羟胺的一种方法,其反应原理如下:2NO+3H2+2HCl![]() 2NH2OH·HCl,某校合作学习小组的同学设计了如图所示装置制备盐酸羟胺:
2NH2OH·HCl,某校合作学习小组的同学设计了如图所示装置制备盐酸羟胺:

①该实验适宜的加热方式为______________。
②装置中导管X的作用是_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com