
【题目】对于下列化学平衡在一定条件下发生移动的描述,不正确的是
A.Cl2+H2O![]() HCl+HClO,氯水中加入碳酸钙,漂白性增强
HCl+HClO,氯水中加入碳酸钙,漂白性增强
B.ZnS + Cu2+![]() CuS + Zn2+,闪锌矿(ZnS)遇CuSO4溶液转化为铜蓝(CuS)
CuS + Zn2+,闪锌矿(ZnS)遇CuSO4溶液转化为铜蓝(CuS)
C.2NO2![]() N2O4 ΔH<0,将装有NO2的玻璃球浸入热水中,红棕色变浅
N2O4 ΔH<0,将装有NO2的玻璃球浸入热水中,红棕色变浅
D.Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色) +2H+,K2Cr2O7溶液中滴加几滴浓硫酸,橙色加深
2CrO42-(黄色) +2H+,K2Cr2O7溶液中滴加几滴浓硫酸,橙色加深
科目:高中化学 来源: 题型:
【题目】工业用黄铜矿(主要成分CuFeS2,含少量锌、铅的硫化物)冶炼铜的一种方法如下:
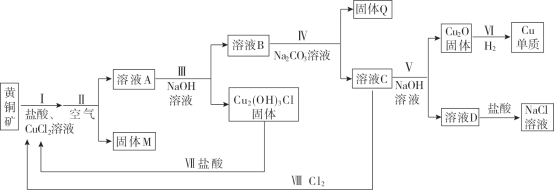
(1)Ⅰ中发生下列反应。ⅰ.CuFeS2 + 3Cu2+ + 4Cl- = 4CuCl+ Fe2+ +2Sⅱ. CuCl + Cl-![]() CuCl2-,I中盐酸的作用是________。
CuCl2-,I中盐酸的作用是________。
(2)Ⅱ中通入空气,将Fe2+转化FeOOH沉淀。
①Fe2+转化为FeOOH的离子方程式是__________。
②溶液A中含金属元素的离子有:Zn2+、Pb2+和________。
(3)Ⅲ中需控制NaOH溶液的用量,其原因是________。
(4)Ⅳ中加入Na2CO3溶液的目的是________。
(5)V中反应的离子方程式是________。
(6)从物质循环利用的角度分析,如何处理NaCl溶液才能更好地服务于该冶炼铜的工艺,并说明理由:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容容器中进行如下反应:N2+3H2![]() 2NH3 △H<0,温度一定时,若将平衡体系中各物质的浓度都增加到原来的2倍,不会产生的结果是( )
2NH3 △H<0,温度一定时,若将平衡体系中各物质的浓度都增加到原来的2倍,不会产生的结果是( )
A. 平衡向正反应方向移动B. 平衡向逆反应方向移动
C. NH3的百分含量增加D. 正、逆反应速率都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含Cr2O72-废水用硫酸亚铁铵[FeSO4(NH4)2SO46H2O]处理,反应中铁元素和铬元素完全转化为沉淀,该沉淀干燥后得到nmolFeOFeyCrxO3(提示:其中Cr为+3价)。不考虑处理过程中的实际损耗,下列叙述错误的是
A.消耗硫酸亚铁铵的物质的量为n(3x+l)mol
B.处理废水中Cr2O72-的物质的量为(nx/2)mol
C.反应中发生转移的电子的物质的量为6nxmol
D.在FeOFeyCrxO3中3x=y
查看答案和解析>>
科目:高中化学 来源: 题型:
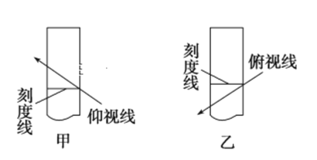
【题目】配制250mL0.10mol·L-1的NaOH溶液时,下列实验操作会使配得的溶液浓度偏大的是
A.转移溶液后未洗涤烧杯和玻璃棒就直接定容
B.在容量瓶中定容时仰视刻度线
C.在容量瓶中定容时俯视刻度线
D.定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇(CH3OH)的合成与应用具有广阔的发展前景。
Ⅰ.合成甲醇的部分工艺流程如下:
![]()
(1)甲烷与水蒸气反应制备合成甲醇的原料气CO、CO2和H2。CH4(g)+H2O(g)=CO(g)+3H2(g) 、H =+206.2 kJ·mol-1,CO(g) + H2O(g) =CO2(g) + H2(g)H =41.0 kJ·mol-1,甲烷与水蒸气反应生成CO2和H2的热化学方程式为________。
(2)在催化剂的作用下,200~300℃时,合成反应器内发生反应:ⅰ. CO(g)+2H2(g)![]() CH3OH(g)H<0,ⅱ.CO2(g)+3H2(g)
CH3OH(g)H<0,ⅱ.CO2(g)+3H2(g)![]() CH3OH(g) + H2O(g)H<0。
CH3OH(g) + H2O(g)H<0。
①一段时间内,记录合成反应器出、入口样品的温度,数据如图所示。曲线_________是合成反应器出口样品的温度。
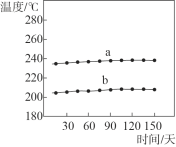
②如果你是工程师,请对合成反应器中压强的控制提出建议并说明理由:_______。合成反应器中有少量的副反应,会生成二甲醚(CH3OCH3)、甲酸甲酯等。已知沸点:甲醇 64.7℃;二甲醚 -24.9℃;甲酸甲酯32.0℃。
③CO和H2生成二甲醚的化学方程式是_________。
④从合成反应器出来的产品经分离提纯可以得到甲醇,请简述该方法_______。
Ⅱ.下图为甲醇燃料电池的示意图。
(3)①负极的电极反应式是_______。
②质子交换膜材料的合成是燃料电池的核心技术。我国科研人员研发的一种质子交换膜材料的结构片段如下,它由三种单体缩聚而成。
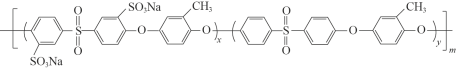
已知:ROH + R’Cl → R—O—R’ + HCl,单体的结构简式是: 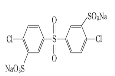 、 _____、___。
、 _____、___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象描述错误的是
编号 | 实验 | 现象 |
A | 加热放在坩埚中的小块钠 | 钠先熔化成光亮的小球,燃烧时,火焰为黄色,燃烧后,生成淡黄色固体 |
B | 在酒精灯上加热用砂纸打磨过的铝箔 | 铝箔变软,失去光泽,熔化的铝并不滴落 |
C | 在FeCl2溶液中滴入NaOH溶液 | 生成白色沉淀,沉淀很快变为灰绿色,最后变为红褐色 |
D | 将水蒸气通过灼热的铁粉 | 黑色粉末变为红褐色 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式书写错误的是( )
A.NaHCO3水解的离子方程式:HCO3-+ H2O![]() CO32-+H3O+
CO32-+H3O+
B.NH4Cl水解的化学方程式:NH4Cl+H2O![]() NH3·H2O+HCl
NH3·H2O+HCl
C.Al(OH)3的两性电离方程式:H++AlO2-+H2O![]() Al(OH)3
Al(OH)3![]() Al3++3OH
Al3++3OH
D.NaHSO3的电离方程式:NaHSO3=Na++HSO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com