
【题目】下列说法正确的是
A. CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,1H-NMR谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,故不能用1H-NMR来鉴别
B. 苯、苯酚、己烯只用一种试剂就可以鉴别
C.  用系统命名法叫2-甲基-1-丙醇
用系统命名法叫2-甲基-1-丙醇
D. 按系统命名法, 的名称为2,5,6-三甲基-4-乙基庚烷
的名称为2,5,6-三甲基-4-乙基庚烷
【答案】B
【解析】
A、CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,1H-NMR谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,但是二者的核磁共振氢谱中峰的位置不相同,可以用1H-NMR来鉴别,故A错误;
B、直接用溴水即可鉴别。苯和溴水发生萃取,分层后上层为红棕色苯层,下层为淡黄色水层;苯酚和浓溴水反应生成白色不溶于水的三溴苯酚沉淀;己烯和溴水反应,首先发生分层,上层为红棕色有机层,下层为淡黄色水层,随后振荡或者微微加热,上层褪色(溴和己烯发生加成作用),故B正确;
C、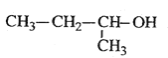 用系统命名法叫2-丁醇,故C错误;
用系统命名法叫2-丁醇,故C错误;
D、按系统命名法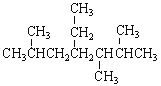 的名称为2,3,6-三甲基-4-乙基庚烷,故D错误;
的名称为2,3,6-三甲基-4-乙基庚烷,故D错误;
综上所述,本题应选B。


科目:高中化学 来源: 题型:
【题目】下列有机合成设计中,所涉及的反应类型有错误的是
A. 由丙醛制 1,2﹣丙二醇:第一步还原,第二步消去,第三步加成,第四步取代
B. 由1-溴丁烷制1,3-丁二烯:第一步消去,第二步加成,第三步消去
C. 由乙炔合成苯酚:第一步三聚,第二步取代,第三步水解,第四步中和
D. 由![]() 制
制![]() :第一步加成,第二步消去,第三步加成,第四步取代
:第一步加成,第二步消去,第三步加成,第四步取代
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100mL溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如下:(所加试剂均过量,气体全部逸出)
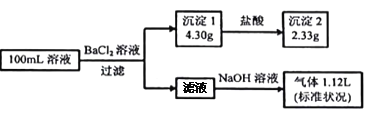
下列说法不正确的是
A. 原溶液一定存在CO32-和SO42-,一定不存在Fe3+
B. 若原溶液中不存在Na+,则c(Cl-)<0.1mol·L-1
C. 原溶液中c(Cl-)≥0.1mol·L-1
D. 原溶液一定存在Cl-,可能存在Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为周期表中短周期的一部分。已知a原子的最外层上的电子数目是次外层电子数目的一半,下列说法中不正确的是( )

A. 元素a的最高价氧化物的水化物的酸性比b弱
B. 元素a的原子半径比d的大
C. 元素a的单质在空气中燃烧会导致“温室效应”
D. 元素a单质是一种良好的半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环戊二烯(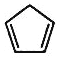 )是一种重要的化工原料。
)是一种重要的化工原料。
(1)工业上可用环戊二烯制备金刚烷
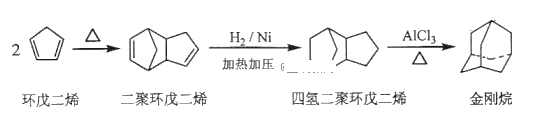
①环戊二烯分子中最多有_____________个原子共平面;
②金刚烷的分子式为___________,其二氯代物有________种。
③已知烯烃能发生如下反应:
![]()
请写出下列反应产物的结构简式:__________
![]()
(2)Diels-Alder反应为共轭双烯与含有烯键或炔键的化合物相互作用生成六元环状化合物的反应,最简单的反应是 由环戊二烯和A经Diels-Alder反应制得
由环戊二烯和A经Diels-Alder反应制得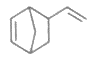 。
。
①Diels-Alder反应属于_______反应(填反应类型):A的结构简式为________________。
②写出与 互为同分异构,且一溴代物只有两种的芳香烃的名称_______,
互为同分异构,且一溴代物只有两种的芳香烃的名称_______,
写出生成这两种一溴代物所需要的反应试剂和反应条件_______________、______________。
③写出实验室由![]() 的属于芳香烃的同分异构体的同系物制备
的属于芳香烃的同分异构体的同系物制备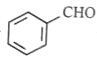 的合成路线流程图,合成路线流程图示例如下:
的合成路线流程图,合成路线流程图示例如下:
![]()
_______________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含锰矿物的主要成分有MnCO3、MnO2、FeCO3、SiO2、Al2O3等。已知FeCO3、MnCO3难溶于水。一种运用阴离子膜电解法的新技术可用于从碳酸锰矿中提取金属锰,主要流程如下:

(1)为提高含锰矿物浸出速率,可采取的措施有______________(至少写出两条)。
(2)设备1中反应后,滤液1里锰元素只以Mn2+的形式存在,且滤渣1中也无MnO2。设备1中发生氧化还原反应的离子方程式是______________________________________。
(3)设备2中加足量双氧水的作用是________________________。设计实验方案检验滤液2中是否存在Fe2+________________________。
(4)已知金属离子的氢氧化物开始沉淀和完全沉淀的pH如下表,加氨水调节溶液的pH等于6,滤渣2的主要成分为_____________ (填化学式)。
金属离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe3+ | 1.8 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 5.8 | 8.8 |
Mn2+ | 7.8 | 9.8 |
(5)设备4中加入过量氢氧化钠溶液,用离子方程式表示发生的反应______________。
(6)保持其他条件不变,在不同温度下对含锰矿物进行酸浸,锰浸出率随时间变化如图。酸浸的最佳温度与时间分别为________℃、______min。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁溶液与氢氧化铁胶体的共同点是( )
A.分散质颗粒直径都在l~100 nm之间
B.颜色都呈红褐色
C.一束平行光照射溶液时,从侧面都可以看到一束光束
D.都是分散系
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com