
【题目】现有下列短周期元素的数据(已知Be的原子半径为0.089 nm):
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径 (nm) | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 |
最高正化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
最低负化合价 | 2 | 3 | 1 | 3 |
(1)⑧号元素的在周期表中的位置是________________;上述元素处于同一主族的有_________________________。(用元素符号表示!)
(2)上表中某两种元素形成的共价化合物中,每个原子都满足最外层为8电子的稳定结构,写出其电子式:__________________________(任写一种
(3)元素①和⑥能形成两种化合物,写出其中较稳定的化合物与水反应的离子方程式_____________________________________________________。
(4)含锂材料在社会中广泛应用,如各种储氢材料(Li2NH等)、便携式电源材料(LiCoO2等)。根据下列要求回答问题:
①![]() 和
和![]() 作核反应堆最佳热载体,
作核反应堆最佳热载体,![]() 和
和![]() 用作高温堆减速剂。下列说法正确的是________
用作高温堆减速剂。下列说法正确的是________
A. ![]() 和
和![]() 互为同位素 B.
互为同位素 B. ![]() 和
和![]() 属于同种核素
属于同种核素
C. ![]() 和
和![]() 的化学性质不同 D.
的化学性质不同 D. ![]() 和
和![]() 是同种物质
是同种物质
②下列说法不正确的是_________
A. 碱性:Be(OH)2 < LiOH < NaOH < KOH
B. 半径:K > Na > Li > Li+
C. 氧化性:Li+ < Na+ < K+ < Rb+ < Cs+
D. 金属性:Cs > Rb > K > Na > Li > Be
【答案】 第2周期,第ⅢA族 Li,Na和N,P ![]() 2Na2O2 + 2H2O == 4Na+ + 4OH + O2↑ AD C
2Na2O2 + 2H2O == 4Na+ + 4OH + O2↑ AD C
【解析】试题分析:由题中及表中数据可知,①②③④⑤⑥⑦⑧分别位于第VIA、第IIA、第IA、第VA、第VIIA、第IA、第VA、第IIIA族。Be的原子半径为0.089 nm,Be的最高价为2,②的最高价也是+2、半径比Be大,则②为Mg;③是最高价为+1、半径比Mg小,则③是Li;⑥是最高价为+1、半径比Mg大,则⑥为Na;④和⑦的最高价都是+5、最低价都是-3,则它们为第VA族元素,因为④的半径较大,故④为P、⑦为N;根据同周期元素的原子半径逐渐减小,可知⑧为B、①为O、⑤为Cl。综上所述,①②③④⑤⑥⑦⑧分别为O、Mg、Li、P、Cl、Na、N、B。
(1)⑧号元素的在周期表中的位置是第2周期,第ⅢA族;上述元素处于同一主族的有两组,分别是Li,Na和N,P。
(2)上表中某两种元素形成的共价化合物中,每个原子都满足最外层为8电子的稳定结构,这样的化合物有多种,如PCl3等,其电子式为![]() 。
。
(3)元素①和⑥能形成两种化合物,其中较稳定的是过氧化钠,过氧化钠与水反应的离子方程式为2Na2O2 + 2H2O == 4Na+ + 4OH + O2↑。
(4)①A. ![]() 和
和![]() 互为同位素,A正确; B.
互为同位素,A正确; B. ![]() 和
和![]() 属于不同的核素,B不正确;C.
属于不同的核素,B不正确;C. ![]() 和
和![]() 的化学性质几乎完全相同,C不正确;D.
的化学性质几乎完全相同,C不正确;D. ![]() 和
和![]() 是同种物质(都是氢化锂),D正确。综上所述,说法正确的是AD。
是同种物质(都是氢化锂),D正确。综上所述,说法正确的是AD。
②A. Be、Li、Na、K的金属性依次增加,故其最高价氧化物的水化物的碱性从弱到强的顺序为Be(OH)2 <LiOH<NaOH <KOH,A正确;B. 同一主族元素的原子半径随原子序数的增大而增大,同一元素的原子半径大于其阳离子半径,故半径K> Na >Li >Li+,B正确;
C. Li、Na、K、Rb、Cs的金属性依次增加,故其阳离子的氧化性从强到弱的顺序为Li+ > Na+ > K+ >Rb+>Cs+,C不正确;D. 金属性由强到弱的顺序为Cs >Rb >K>Na >Li >Be,D正确。综上所述,说法不正确的是C 。


科目:高中化学 来源: 题型:
【题目】苯分子中不存在C—C键和C=C键交替结构,下列事实不能说明的是
A.苯不能使酸性高锰酸钾溶液褪色
B.苯分子中碳碳键的键长都相等
C.苯在加热和催化剂存在条件下与氢气反应生成环己烷
D.苯能与液溴发生取代反应,但不能与溴水发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种物质之间有下图所示的转化关系.已知:A是空气中的主要成分,B、C、D均为化合物,且C为红棕色气体. 
请回答下列问题:
(1)写出A和C的名称或化学式:A , C;
(2)在上图D→C的过程中,D表现出强(填“氧化性”或“还原性”);
(3)在D的稀溶液中滴入NaOH溶液,其反应的离子方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸钠可用于制备高氯酸.以精制盐水等为原料制备高氯酸钠晶体(NaClO4H2O)的流程如下: 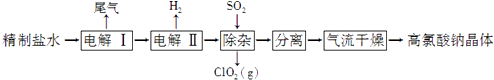
(1)由粗盐(含Ca2+、Mg2+、 ![]() 、Br﹣等杂质)制备精制盐水时需用到NaOH、BaCl2、Na2CO3等试剂.Na2CO3的作用是;除去盐水中的Br﹣可以节省电解过程中的电能,其原因是 .
、Br﹣等杂质)制备精制盐水时需用到NaOH、BaCl2、Na2CO3等试剂.Na2CO3的作用是;除去盐水中的Br﹣可以节省电解过程中的电能,其原因是 .
(2)“电解Ⅰ”的目的是制备NaClO3溶液,产生的尾气除H2外,还含有(填化学式).“电解Ⅱ”的化学方程式为 .
(3)“除杂”的目的是除去少量的NaClO3杂质,该反应的离子方程式为 . “气流干燥”时,温度控制在80~100℃的原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是比较过氧化钠和氧化钠性质异同的有关叙述,其中错误的是( )
A. 过氧化钠和氧化钠长期置于空气中最终产物相同
B. 过氧化钠和氧化钠都能与二氧化碳或水发生化合反应
C. 过氧化钠和氧化钠与水反应都有氢氧化钠生成
D. 过氧化钠是强氧化剂,而氧化钠是一种碱性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学技术名词审定委员会已确定第116号元素Lv的名称为鉝。关于![]() 的叙述错误的是
的叙述错误的是
A. 原子序数116 B. 中子数177
C. 核外电子数116 D. 相对原子质量293
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种短周期元素, 它们的原子序数由A到D依次增大, 已知A和B原子有相同的电子层数, 且A的L层电子数是K层电子数的两倍, C在空气中燃烧时呈现黄色火焰, C的单质在加热下与B的单质充分反应, 可以得到与D单质颜色相同的淡黄色固态化合物, 试根据以上叙述回答:
(1)元素名称: A ______ B _____ C _____ D ______
(2)D元素位于周期表中___________周期____________族
(3)写出AB2与C2B2反应的化学方程式:________________________________________。
(4)电子式表示化合物 C2D 的形成过程:________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1mol O=O键完全断裂时吸收热量496kJ,水蒸气中1mol H﹣O键形成时放出热量463kJ,则氢气中1mol H﹣H键断裂时吸收热量为( )
A.920kJ
B.557kJ
C.436kJ
D.181kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com