
【题目】在2 L恒容密闭容器中充入![]() 、
、![]() ,在一定条件下发生如下反应:
,在一定条件下发生如下反应:![]()
![]() ;CO的平衡转化率与温度、压强之间的关系如图所示。下列推断正确的是( )
;CO的平衡转化率与温度、压强之间的关系如图所示。下列推断正确的是( )
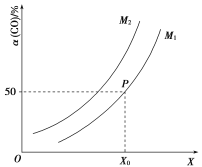
A.工业上,利用上述反应合成甲醇,温度越高越好
B.图象中X代表温度,![]()
C.图象中P点代表的平衡常数K为![]()
D.温度和容积不变,再充入![]() 、1 mol CO,达到平衡时CO的转化率减小
、1 mol CO,达到平衡时CO的转化率减小
【答案】C
【解析】
A.该反应的正反应是放热反应,温度升高,平衡向左移动,甲醇的产率降低,应根据催化剂来选择合适的温度,A项错误;
B.该反应的正反应是放热反应,又是气体分子数减小的反应,从图象看出,随着X增大,CO的转化率增大,所以X代表压强,M代表温度,温度越高,CO的平衡转化率越低,所以![]() ,B项错误;
,B项错误;
C.P点时CO的转化率为50%,用“三段式”法进行计算:
![]()
起始浓度/(![]() ) 1 0.5 0
) 1 0.5 0
变化浓度/(![]() ) 0.5 0.25 0.25
) 0.5 0.25 0.25
平衡浓度/(![]() ) 0.5 0.25 0.25
) 0.5 0.25 0.25
![]() (单位可省),C项正确;
(单位可省),C项正确;
D.温度不变,平衡常数不变,容积不变,再充入![]() 、1 mol CO,相当于增大压强,平衡向右移动,
、1 mol CO,相当于增大压强,平衡向右移动,![]() 、CO的转化率都增大,D项错误。
、CO的转化率都增大,D项错误。
答案选C。


科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,W、Y同主族,Y是地壳中含量最多的金属元素,Z原子最外层电子数是其内层电子数的![]() 。若自然界存在游离态的X,则下列说法正确的是
。若自然界存在游离态的X,则下列说法正确的是
A.元素非金属性的顺序为W>X>ZB.X的氢化物分子中可能含有非极性键
C.工业上通常采用热分解法冶炼Y的单质D.Z的最高价氧化物的水化物属于强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,科学家通过对稻壳进行控制性焚烧热解,从中提取一种叫做生物质纳米结构二氧化硅的超高活性材料,将少量这种材料掺入混凝土中,即可轻易制备出超高强度和超高耐久性能的高性能混凝土。关于二氧化硅下列说法中正确的是( )
A.二氧化硅溶于水显酸性,所以二氧化硅属于酸性氧化物
B.二氧化碳通入硅酸钠溶液中可以得到硅酸
C.由CaCO3+SiO2![]() CaSiO3+CO2↑可知硅酸的酸性比碳酸强
CaSiO3+CO2↑可知硅酸的酸性比碳酸强
D.二氧化硅是酸性氧化物,它不溶于任何酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是
A. HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol
B. CO(g)的燃烧热是283.0kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的ΔH=+2×283.0kJ/mol
C. 需要加热才能发生的反应一定是吸热反应
D. 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应m A(g)+n B(g) ![]() p C(g)在密闭容器中进行,下图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是( )
p C(g)在密闭容器中进行,下图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是( )

A.T1<T2 p1>p2 m+n>p 放热反应B.T1>T2 p1<p2 m+n>p 吸热反应
C.T1<T2 p1>p2 m+n<p 放热反应D.T1>T2 p1<p2 m+n<p 吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)汽车尾气中的 NO和CO可在催化剂作用下生成无污染的气体而除去。在密闭容器中充入10 mol CO和8 mol NO发生反应,测得平衡时NO的体积分数与温度、压强的关系如图。
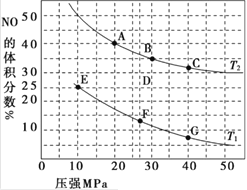
①已知该反应在较低温度下能自发进行,则反应 2NO(g)+2CO(g)![]() N2(g)+2CO2 (g),ΔH______0(填“>” “=”或“<”)。
N2(g)+2CO2 (g),ΔH______0(填“>” “=”或“<”)。
②该反应达到平衡后,为同时提高反应速率和CO的转化率,可采取的措施有______ (填字母序号)
a.改用高效催化剂 b.缩小容器的体积 c.增加 NO 的浓度 d.升高温度
(2)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2,将一定比例的O2、NH3 和NOx的混合气体匀速通入装有催化剂M的反应器中反应,反应相同时间,NOx的去除率随反应温度的变化曲线如图所示。
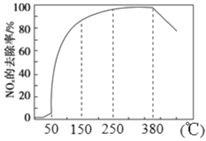
解释在50 ℃~150 ℃范围内随温度升高,NOx 的去除率迅速上升的原因是_______
(3)NH3催化还原氮氧化物技术是目前应用最广泛的烟气脱氮技术:4NH3(g)+6NO(g) ![]() 5N2(g)+6H2O(g) ΔH<0。密闭容器中,在相同时间内,在催化剂 A作用下脱氮率随温度变化如图所示。
5N2(g)+6H2O(g) ΔH<0。密闭容器中,在相同时间内,在催化剂 A作用下脱氮率随温度变化如图所示。
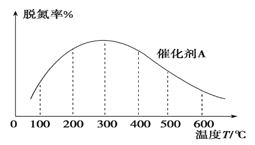
现改用催化能力稍弱的催化剂B进行实验,请在上图中画出在催化剂 B作用下的脱氮率随温度变化的曲线_________(不考虑温度对催化剂活性的影响)。
(4)某研究小组利用反应:C(s)+2NO(g)![]() N2(g)+CO2(g) △ H= -34.0 kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得 NO的转化率随温度的变化如图所示:
N2(g)+CO2(g) △ H= -34.0 kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得 NO的转化率随温度的变化如图所示:
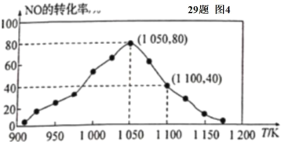
①由图可知,在 1050 K 前,反应中 NO的转化率随温度升髙而增大,其原因为____________; 在 1100 K 时,N2的体积分数为____________。
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作 Kp )。在 1050 K、1.1×106 Pa 时,该反应的化学平衡常数 Kp=____________(已知:气体分压(P分) =气体总压(Pa)×体积分数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠可由亚硫酸钠和硫粉通过化合反应制得:Na2SO3+S=Na2S2O3。常温下溶液中析出晶体为Na2S2O35H2O。Na2S2O3·5H2O 于 40~45℃熔化,48℃分解;
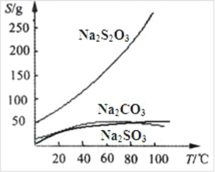
Na2S2O3 易溶于水,不溶于乙醇。在水中有关物质的溶解度曲线如图所示。
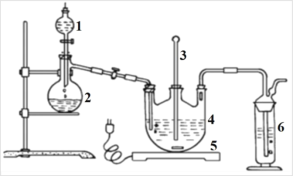
Ⅰ.现按如下方法制备Na2S2O3·5H2O:将硫化钠和碳酸钠按反应要求比例一并放入三颈烧瓶中,注入150 mL蒸馏水使其溶解,在分液漏斗中,注入浓盐酸,在装置2中加入亚硫酸钠固体,并按上右图安装好装置。
(1)仪器2的名称为_____________,装置6中可放入_____________。
A.BaCl2溶液 B.浓H2SO4 C.酸性KMnO4溶液 D.NaOH溶液
(2)打开分液漏斗活塞,注入浓盐酸使反应产生的二氧化硫气体较均匀的通入Na2S和Na2CO3的混合溶液中,并用磁力搅拌器搅动并加热,反应原理为:
①Na2CO3+SO2=Na2SO3+CO2 ② Na2S+SO2+H2O=Na2SO3+H2S
③2H2S+SO2=3S↓+2H2O ④ Na2SO3+S![]() Na2S2O3
Na2S2O3
随着SO2气体的通入,看到溶液中有大量浅黄色固体析出,继续通入SO2气体,反应约半小时。当溶液中pH接近或不小于7时,即可停止通气和加热。溶液pH要控制不小于7的理由是:_____________(用文字和相关离子方程式表示)。
Ⅱ.分离Na2S2O3·5H2O 并测定含量:

(3)从热的反应混合液中获得 Na2S2O3·5H2O粗晶体,需经过下列实验步骤,请选择正确的选项:热的反应混合液→活性炭脱色并保温→________→________→________→________→获得Na2S2O3·5H2O粗晶体。
a.用冰水浴冷却结晶,抽滤; b.用少量水洗涤晶体、烘干;
c.80℃蒸发浓缩滤液至溶液表面出现晶膜; d.用乙醇洗涤晶体、晾干;
e.45℃蒸发浓缩滤液至溶液呈微黄色浑浊; f.趁热过滤。
(4)制得的粗晶体中往往含有少量杂质。为了测定粗产品中 Na2S2O3·5H2O的含量, 一般采用在酸性条件下用 KMnO4标准液滴定的方法(假定粗产品中杂质与酸性KMnO4溶液不反应)。称取1.280 g的粗样品溶于水,用 0.4000 mol/LKMnO4溶液(加入适量硫酸酸化)滴定,当溶液中S2O32-全部被氧化时,消耗 KMnO4溶液体积20.00 mL。 试回答:
①对于上述实验操作,下列说法正确的是_____。
A.用电子天平称量粗样品时,若电子天平未进行调平,则纯度偏高
B.装 KMnO4标准液的酸式滴定管洗涤后若未润洗,则纯度偏高
C.滴定至锥形瓶内溶液刚好由无色变为浅红色立即进行读数,则纯度偏高
D.滴定时若滴定速度过慢或摇晃锥形瓶过于剧烈,则纯度偏高
②产品中Na2S2O3·5H2O的质量分数为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应原理是:2NaCl(熔融)![]() 2Na+Cl2↑。回答下列有关单质钠的问题:
2Na+Cl2↑。回答下列有关单质钠的问题:
(1)下列各项中属于保存金属钠的正确方法是(______)
A.放在棕色瓶中 B.放在细沙中 C.放在水中 D.放在煤油中
(2)钠长时间放在空气中,最后的产物主要成分是(______)
A.Na2O B.Na2O2 C.NaOH D.Na2CO3
(3)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应(如图Ⅰ所示),生成物的颜色为___,请写出该反应的化学方程式___。将该试管冷却后直立,滴加几滴水(如图Ⅱ所示),发生反应的离子方程式为___,若有0.5molNa氧化生成氧化钠和过氧化钠的混合物,转移电子的数目为___。
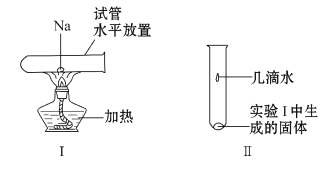
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦锑酸钠(NaSbO3·3H2O)可用于搪瓷的乳白剂及铁皮、钢板的抗酸漆。一种利用高砷锑烟灰(主要成分为Sb2O3、As2O3,还含Ag、Cu、Fe的氧化物)生产焦锑酸钠的工艺流程如下:
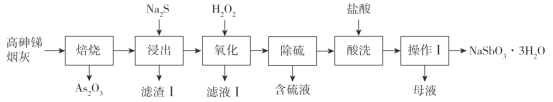
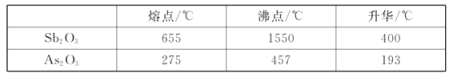
已知:i.Sb2O3、As2O3部分性质如下表:
ii.Ag、Cu、Fe的氧化物不溶于Na2S溶液
iii.Na2SbO4不溶于水;NaSbO3﹒3H2O既不溶于水,也不溶于酸。
请回答下列问题:
(1)“焙烧”的最低温度为_________(填标号)
a.655℃ b.400℃ c.275℃ d.193℃
(2)“浸出”时,往往采取比常温稍高的浸液温度,且选用较高浓度的Na2S溶液,采取这些措施的目的是_________________________________________。“浸出”时,Sb2O3转化为Na3SbS3的化学方程式为__________________________________________,滤渣Ⅰ是____________。
(3)“氧化”时所用H2O2的电子式为___________,氧化产物为Na3SbO4和____________.
(4)“酸洗”的作用是______________________。(用化学方程式表示)
(5)As2O3对应的酸为H3AsO3,测得某工业酸性废液中含H3AsO3和Fe2+,其浓度如表:

已知:iV.Ksp(FeAsO3)>Ksp(FeAsO4)=5.70×10-21。
V.H3AsO3的还原性比Fe2+强。
根据题目信息,则可采用______________方法除去该废水中的砷,除去砷后的废液中c(AsO43-)=__________________(不考虑反应过程中溶液体积的微小变化)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com